题目内容
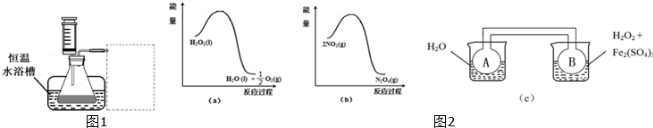
下列实验操作或装置符合实验要求的是( )


| A、装置Ⅰ可用于测定中和热 |
| B、装置Ⅱ装置放置一段时间后,饱和CuSO4溶液中不出现蓝色晶体 |
| C、装置Ⅲ中的石英坩埚可用于熔化氢氧化钠 |
| D、装置Ⅳ可用于吸收易溶于水的尾气 |
考点:化学实验方案的评价
专题:实验评价题
分析:A.缺少环形搅拌器;
B.CaO具有吸水性,可使饱和溶液析出晶体;
C.二氧化硅与氢氧化钠反应;
D.球形结构可防止倒吸.
B.CaO具有吸水性,可使饱和溶液析出晶体;
C.二氧化硅与氢氧化钠反应;
D.球形结构可防止倒吸.
解答:
解;A.图中缺少环形玻璃搅拌棒,测定中和热的数值不准确,故A错误;
B.CaO具有吸水性,饱和溶液溶剂减少析出晶体,则装置Ⅱ装置放置一段时间后,饱和CuSO4溶液中出现蓝色晶体,故B错误;
C.二氧化硅与氢氧化钠反应,加热易导致坩埚炸裂,故C错误;
D.球形结构可防止倒吸,则装置Ⅳ可用于吸收易溶于水的尾气,故D正确;
故选D.
B.CaO具有吸水性,饱和溶液溶剂减少析出晶体,则装置Ⅱ装置放置一段时间后,饱和CuSO4溶液中出现蓝色晶体,故B错误;
C.二氧化硅与氢氧化钠反应,加热易导致坩埚炸裂,故C错误;
D.球形结构可防止倒吸,则装置Ⅳ可用于吸收易溶于水的尾气,故D正确;
故选D.
点评:本题考查化学实验方案的评价,涉及中和热的测定、防倒吸装置、饱和溶液及物质的性质等,侧重基础知识的考查,题目难度不大,选项C为易错点.

练习册系列答案
相关题目
下列化学用语表示正确的是( )
A、原子核中有6个中子的硼原子:
| ||
B、HCl的电子式: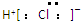 | ||
C、K+结构示意图: | ||
| D、HClO的结构式:H-O-Cl |
 高铁酸盐在能源环保领域有广泛用途.用镍(Ni)、铁作电极电解浓NaOH溶液制备高铁酸钠(Na2FeO4)的装置如图所示.下列说法正确的是( )
高铁酸盐在能源环保领域有广泛用途.用镍(Ni)、铁作电极电解浓NaOH溶液制备高铁酸钠(Na2FeO4)的装置如图所示.下列说法正确的是( )| A、铁是阳极,电极反应为Fe-2e-+2OH-═Fe(OH)2 |
| B、电解一段时间后,镍电极附近溶液的pH减小 |
| C、若离子交换膜为阴离子交换膜,则电解过程中氢氧根向阳极移动 |
| D、每制得1mol Na2FeO4,理论上可以产生67.2L气体 |
化学无处不在,下面说法正确的是( )
| A、“地沟油”禁止食用,但可用于制造生物柴油 |
| B、“PM2.5”是指大气中直径小于或等于2.5μm(1μm=1×10-6m)的颗粒,“PM2.5”与空气形成的分散系属于胶体 |
| C、红宝石、水晶、玻璃、陶瓷等都是硅酸盐制品 |
| D、分馏、裂化、裂解是利用化学变化来炼制加工石油的三种重要方法 |
对下列与化学有关的社会和生活问题作出判断,其中正确的是( )
| A、煤经过气化和液化等物理变化可以转化为清洁燃料 |
| B、大型制冷设备的液氨大量泄漏不会对操作人员造成伤害 |
| C、Al(SO4)3可用于对自来水进行杀菌消毒 |
| D、静电除尘与胶体的基本性质有一定联系 |
用NA表示阿伏加德罗常数的值,下列叙述正确的是( )
| A、0.1mol?L-1 Na2S溶液中含有的Na+离子数为0.2NA |
| B、50mL 18.4mol/L浓硫酸与足量铜微热反应,生成SO2分子数目为0.46NA |
| C、标准状况下,22.4L以任意比例混合的氢气和氯气混合气中含有的原子总数为2NA |
| D、0.10mol Fe粉与足量水蒸气反应生成的H2分子数为0.10NA |
下列有关的离子方程式正确的是( )
| A、向FeCl3溶液中加入Mg(OH)2:3Mg(OH)2+2Fe3+═2Fe(OH)3+3Mg2+ | ||||
B、铜片接电源正极,碳棒接电源负极,电解硫酸铜溶液:Cu+2H+
| ||||
| C、在100mL浓度为1mol?L-1的Fe(NO3)3的溶液中通入足量SO2 2Fe3++SO2+2H2O═2Fe2++SO42-+4H+ | ||||
| D、实验室配制的亚铁盐溶液在空气中被氧化:4Fe2++O2+2H2O═4Fe3++4OH- |
N2O俗称“笑气”,医疗上曾用作可吸入性麻醉剂,下列反应能产生N2O:3CO+2NO2═3CO2+N2O.下列关于N2O的说法一定正确的是( )
| A、上述反应中,每消耗2mol NO2,就会生成22.4L N2O |
| B、CO2是氧化产物,且为H2CO3的酸酐 |
| C、等质量的N2O和CO2含有相等的电子数 |
| D、N2O会迅速与人体血红蛋白结合,使人中毒 |