题目内容
某兴趣小组成员发现在超市购买的“旺旺雪饼”袋内有一个小纸袋,上面写着“干燥剂,主要成分是生石灰,请勿食用”.该兴趣小组对干燥剂的有关问题进行相关探究:
(1)问题1:为什么生石灰(CaO)可作干燥剂?(用化学方程式表示) .
(2)兴趣小组甲同学又对它作了一系列探究,其有关实验方案如下:
(3)问题4:样品中碳酸钙的含量如何?乙同学按如下流程进行实验:用盐酸溶解该干燥剂样品→干燥所得气体→用NaOH溶液吸收气体→根据NaOH溶液的增重计算该样品的含量,实验过程中所取该干燥剂样品的质量为10.0g.实验装置如下图所示.
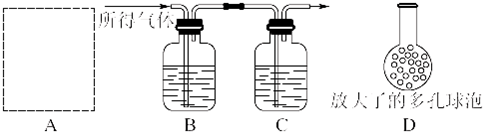
①A为溶解该干燥剂样品的装置,若已准备了长颈漏斗、双孔橡胶塞、导气管,为完成溶解至少还需要的实验仪器是 .
②A中发生反应的化学方程式为 .
③将插入溶液C中管子的下端改成具有多孔的球泡(如图中的D),有利于提高实验的准确度,其理由是 .
④当改进实验装置并进行正确操作后可以准确测定出干燥剂样品的含量(假设生成气体没有损失,并完全吸收).若此时C装置在实验前后其质量增加了3.6g,则该干燥剂样品中CaCO3的百分含量为 .
(1)问题1:为什么生石灰(CaO)可作干燥剂?(用化学方程式表示)
(2)兴趣小组甲同学又对它作了一系列探究,其有关实验方案如下:
| 问题与猜想 | 实验步骤 | 实验现象 | 实验结论 |
| 问题2:小纸袋中的物质能否继续作干燥剂? | 取足量小纸袋中固体放入烧杯中,加入适量水,触摸杯壁 | 不能继续作干燥剂 | |
| 问题3:甲猜想变质后的物质可能含有碳酸钙,该如何验证甲的猜想? | 该干燥剂样品中含有碳酸钙 |

①A为溶解该干燥剂样品的装置,若已准备了长颈漏斗、双孔橡胶塞、导气管,为完成溶解至少还需要的实验仪器是
②A中发生反应的化学方程式为
③将插入溶液C中管子的下端改成具有多孔的球泡(如图中的D),有利于提高实验的准确度,其理由是
④当改进实验装置并进行正确操作后可以准确测定出干燥剂样品的含量(假设生成气体没有损失,并完全吸收).若此时C装置在实验前后其质量增加了3.6g,则该干燥剂样品中CaCO3的百分含量为
考点:探究物质的组成或测量物质的含量,常见的食品添加剂的组成、性质和作用
专题:实验探究和数据处理题
分析:(1)生石灰易和水反应生成氢氧化钙;
(2)因为CaO溶于水会放出大量的热,根据结论不能再作干燥剂,所以现象为杯壁不发烫;如果是CaCO3,则可以加盐酸看是否有气泡产生即可;
(3)从所给的仪器看缺少盛放样品的容器,可选用锥形瓶等,A中的反应为CaCO3+2HCl═CaCl2+CO2↑+H2O,多孔的球泡有利于CO2的吸收,C装置增重是吸收了CO2,即CO2为0.0818 mol,相当于CaCO3为8.18 g,百分含量为81.8%.
(2)因为CaO溶于水会放出大量的热,根据结论不能再作干燥剂,所以现象为杯壁不发烫;如果是CaCO3,则可以加盐酸看是否有气泡产生即可;
(3)从所给的仪器看缺少盛放样品的容器,可选用锥形瓶等,A中的反应为CaCO3+2HCl═CaCl2+CO2↑+H2O,多孔的球泡有利于CO2的吸收,C装置增重是吸收了CO2,即CO2为0.0818 mol,相当于CaCO3为8.18 g,百分含量为81.8%.
解答:
解:(1)生石灰易和水反应生成氢氧化钙,反应的方程式为:CaO+H2O═Ca(OH)2;故答案为:CaO+H2O═Ca(OH)2;
(2)氧化钙溶于水放出大量的热,故取足量小纸袋中固体放入烧杯中,加入适量水,触摸杯壁,若不发烫,说明已经失效,不能继续作干燥剂使用;
甲猜想变质后的物质可能含有碳酸钙,碳酸钙和盐酸反应生成二氧化碳气体,故可取固体,滴加盐酸,若有气泡冒出,证明含碳酸钙;故答案为:
;
(3)A为制备二氧化碳的装置,从所给的仪器看缺少盛放样品的容器,可选用锥形瓶等;碳酸钙和盐酸反应生成二氧化碳、氯化钙和水,反应的方程式为:CaCO3+2HCl═CaCl2+CO2↑+H2O;将插入溶液C中管子的下端改成具有多孔的球泡(如图中的D),增大了气体和氢氧化钠的接触面积,有利于二氧化碳的吸收;C装置在实验前后其质量增加了3.6g为二氧化碳的质量,物质的量为:
=0.0818mol,即碳酸钙的物质的量为:0.0818mol,碳酸钙的质量为:0.0818mol×100g/mol=8.18g,
样品中碳酸钙的百分含量为:
×100%=81.8%;故答案为:锥形瓶或广口瓶;CaCO3+2HCl═CaCl2+CO2↑+H2O;增大气体和溶液的接触面积,有利于二氧化碳的吸收;81.8%.
(2)氧化钙溶于水放出大量的热,故取足量小纸袋中固体放入烧杯中,加入适量水,触摸杯壁,若不发烫,说明已经失效,不能继续作干燥剂使用;
甲猜想变质后的物质可能含有碳酸钙,碳酸钙和盐酸反应生成二氧化碳气体,故可取固体,滴加盐酸,若有气泡冒出,证明含碳酸钙;故答案为:
| 问题与猜想 | 实验步骤 | 实验现象 | 实验结论 |
| 问题2:小纸袋中的物质能否继续作干燥剂? | 取足量小纸袋中固体放入烧杯中,加入适量水,触摸杯壁 | 不发烫 | 不能继续作干燥剂 |
| 问题3:甲猜想变质后的物质可能含有碳酸钙,该如何验证甲的猜想? | 取该固体,滴加稀盐酸 | 有气泡产生 | 该干燥剂样品中含有碳酸钙 |
(3)A为制备二氧化碳的装置,从所给的仪器看缺少盛放样品的容器,可选用锥形瓶等;碳酸钙和盐酸反应生成二氧化碳、氯化钙和水,反应的方程式为:CaCO3+2HCl═CaCl2+CO2↑+H2O;将插入溶液C中管子的下端改成具有多孔的球泡(如图中的D),增大了气体和氢氧化钠的接触面积,有利于二氧化碳的吸收;C装置在实验前后其质量增加了3.6g为二氧化碳的质量,物质的量为:
| 3.6g |
| 44g/mol |
样品中碳酸钙的百分含量为:
| 8.18g |
| 10g |
点评:本题考查了常用干燥剂的成分、干燥原理及失效后成分的检验,中等难度,解答本题关键是熟悉物质之间的相互转化关系及物质的性质.

练习册系列答案
相关题目
过滤后的食盐水仍含有可溶性的CaCl2、MgCl2、Na2SO4 等杂质,通过如下几个实验步骤,可制得纯净的食盐水:①加入稍过量的Na2CO3溶液;②加入稍过量的NaOH溶 液; ③加入稍过量的BaCl2溶液;④滴入适量的稀盐酸;⑤过滤.正确的操作顺序是( )
| A、②③①⑤④ |
| B、①②③⑤④ |
| C、②③①④⑤ |
| D、③⑤②①④ |
下表中物质的分类组合完全正确的是( )
| 选项 | A | B | C | D |
| 强电解质 | KNO3 | H2SO4 | BaSO4 | HClO4 |
| 弱电解质 | HF | CaCO3 | HClO | CH3COONH4 |
| 非电解质 | SO2 | 金属Al | H2O | C2H5OH |
| A、A | B、B | C、C | D、D |
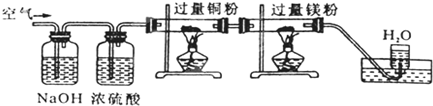
已知在一定条件下能发生下列反应:N2+3Mg
Mg3N2(固),空气缓缓通过下图装置时,依次除去的气体是( )
| ||

| A、CO2、H2O、O2、N2 |
| B、N2、O2、CO2、H2O |
| C、H2O、CO2、N2、O2 |
| D、CO2、N2、H2O、O2 |
以下是一些常用的危险品标志,装运乙醇的包装箱应贴的图标是( )
A、 |
B、 |
C、 |
D、 |
