题目内容
4.NA表示阿伏加德罗常数的值,下列说法正确的是( )| A. | 1molMg变成Mg2+时失去的电子数为NA | |
| B. | 标准状况下,22.4L氮气含有的氮原子数为NA | |
| C. | 48gO3所含氧原子数为3NA | |
| D. | 18gH2O中所含的电子数我8NA |
分析 A、镁变为镁离子后,由0价变为+2价;
B、求出氮气的物质的量,然后根据氮气为双原子分子来分析;
C、臭氧由氧原子构成;
D、求出水的物质的量,然后根据1mol水中含10mol电子来分析.
解答 解:A、镁变为镁离子后,由0价变为+2价,故1mol镁变为离子时失去2NA个电子,故A错误;
B、标况下22.4L氮气的物质的量为1mol,而氮气为双原子分子,故1mol氮气中含2NA个原子,故B错误;
C、臭氧由氧原子构成,故48g臭氧中含3mol氧原子,即3NA个,故C正确;
D、18g水的物质的量为1mol,而1mol水中含10mol电子,故含10NA个电子,故D错误.
故选C.
点评 本题考查了阿伏伽德罗常数的有关计算,熟练掌握公式的使用和物质的结构是解题关键,难度不大.

练习册系列答案
相关题目
15.NA表示阿伏加德罗常数的值.下列叙述正确的是( )
| A. | 48gO3和O2的混合气体中有NA个分子 | |
| B. | 常温常压下,4.6g的NO2气体含有0.3NA个原子 | |
| C. | 1L 0.5mol/L的CuCl2中含有0.5NA个Cu2+ | |
| D. | 标准状况下,3.36L H2O中含有1.5NA个水分子 |
12.百服宁口服液为解热镇痛药,主要用于治疗头痛、发烧.其主要化学成分的结构简式为: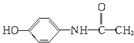 .下列有关该有机物叙述正确的是( )
.下列有关该有机物叙述正确的是( )
 .下列有关该有机物叙述正确的是( )
.下列有关该有机物叙述正确的是( )| A. | 分子式为C8H10NO2 | |
| B. | 其属于α-氨基酸的同分异构体有3种 | |
| C. | 该有机物属于α-氨基酸 | |
| D. | 该有机物可与FeCl3溶液发生显色反应 |
19.人造光卤石(KCl•MgCl2•6H2O)是盐化工的中间产物.以光卤石为原料制得金属镁,可有下列步骤,正确的顺序是( )
①过滤②溶解③加入适量Ca(OH)2④蒸发结晶⑤用盐酸溶解⑥电解熔融MgCl2⑦MgCl2•6H2O脱水.
①过滤②溶解③加入适量Ca(OH)2④蒸发结晶⑤用盐酸溶解⑥电解熔融MgCl2⑦MgCl2•6H2O脱水.
| A. | ⑤③①②④⑥⑦ | B. | ②③①⑤④⑦⑥ | C. | ②④①③⑦⑤⑥ | D. | ⑤③①④②⑦⑥ |
9.某实验室用的蒸馏水,可以被某种酸严重污染,采用下列几种方法进行检验,其中不可行的是( )
| A. | 取样品,向其中滴加石蕊试液 | B. | 取样品,向其中加入CaCO3粉末 | ||
| C. | 取样品,向其中滴加Ba(NO3)2溶液 | D. | 取样品,向其中滴加Na2CO3溶液 |
4.下列微粒的核外电子排布式书写违反泡利原理的是( )
| A. | C:1s22s22p2 | B. | Na+:1s22s22p43s2 | ||
| C. | S2-:1s22s22p23s23p4 | D. | K:1s22s22p63s23p7 |
2.如图装置可以组成原电池的是( )
| A. |  | B. |  | C. |  | D. |  |

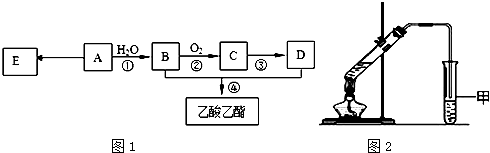
 .
.