题目内容
9.对于反应CO(g)+H2O(g)?H2(g)+CO2(g)正反应是放热反应,在其他条件不变的情况下,下列说法正确的是( )| A. | 加入催化剂,改变了反应的途径,反应放出的热量也一定发生变化 | |
| B. | 改变压强,平衡不发生移动,反应放出的热量不变 | |
| C. | 升高温度,反应速率加快,反应放出的热量不变 | |
| D. | 若在原电池中进行,反应放出的热量不变 |
分析 A、反应的热效应与催化剂的使用无关,反应物和生成物的总能量的高低有关;
B、两边气体计量数相等产,压强改变平衡不移动;
C、升高温度,反应速率加快,平衡向着吸热方向进行;
D、在原电池中进行的反应还会伴随电能的转化,能量是守恒的.
解答 解:A、加入催化剂,改变了反应的途径,反应的△H和反应物以及生成物的能量有关,反应的△H不会改变,故A错误;
B、改变压强,对于反应前后气体系数和相等的平衡,不会发生移动,反应放出的热量不变,故B正确;
C、升高温度,反应速率加快,反应向着吸热方向进行,原来反应放出的热量是不变的,故C错误;
D、在原电池中进行的反应还会伴随电能的转化,并且能量是守恒的,所以反应放出的热量变小,故D错误.
故选B.
点评 本题涉及化学反应中的焓变和反应条件之间的关系,注意原电池中化学能和电能之间的转化,难度中等.

练习册系列答案
相关题目
20.下列实验能达到实验目的且符合安全要求的是( )
| A. | 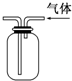 利用排空气法收集CO2 | B. |  收集氧气 | ||
| C. | 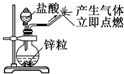 制备并检验氢气的可燃性 | D. | 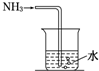 氨水溶于水 |
4.下列说法正确的是( )
| A. | 该 有机物的系统命名为:3-乙基-5-甲基庚烷 有机物的系统命名为:3-乙基-5-甲基庚烷 | |
| B. | 等质量的某烷烃a和某烯烃b,两者完全烧烧后产生的CO2的量有可能a>b | |
| C. | 该 有机物属于单糖,在一定条件下能发生取代、消去、加成、氧化、还原等反应 有机物属于单糖,在一定条件下能发生取代、消去、加成、氧化、还原等反应 | |
| D. | 1mol该 有机物在一定条件下与足量NaOH溶液完全反应,最多可消耗NaOH 10mol 有机物在一定条件下与足量NaOH溶液完全反应,最多可消耗NaOH 10mol |
14.互为同分异构体的物质不可能具有( )
| A. | 相同的式量 | B. | 相同的结构 | C. | 相同的通式 | D. | 相同的分子式 |
1.下列依据相关实验得出的结论正确的是( )
| A. | 用铂丝蘸取某溶液进行焰色反应,火焰呈黄色,证明该溶液中一定不含有K+ | |
| B. | 将某气体通入淀粉碘化钾溶液中,溶液变蓝色,该气体一定是Cl2 | |
| C. | 向无色溶液中加入氯水,再加CCl4,振荡静置后CCl4层呈紫色,则原溶液中含I- | |
| D. | 向某稀溶液中加入少量NaOH溶液,未产生使湿润的红色石蕊试纸变蓝的气体,该溶液中一定不含NH4+ |
18.已知,在2min内某反应物的浓度由3mol/L变成1.5mol/L,则在这段时间内该反应物的化学反应速率为( )
| A. | 3mol/(L•min) | B. | 2mol/(L•min) | C. | 1.5mol/(L•min) | D. | 0.75mol/(L•min) |
19.下列说法正确的是( )
| A. | 煤的干馏和石油的分馏都是物理变化 | |
| B. | 1-氯丙烷和2-氯丙烷的消去产物相同 | |
| C. | 正戊烷、异戊烷、新戊烷的沸点逐渐升高 | |
| D. | 利用油脂在酸性条件下水解,可以生产甘油和肥皂 |
 .
.