题目内容
10.按C、N、O的顺序,下列递变规律不正确的是( )| A. | 原子半径逐渐减小 | B. | 元素原子得电子能力逐渐增强 | ||
| C. | 气态氢化物稳定性逐渐增强 | D. | 最高化合价逐渐增高 |
分析 A.同一周期元素的原子半径逐渐减小;
B.同一周期中,随着原子序数的递增,非金属性逐渐增强,得电子能力逐渐增强;
C.非金属性越强,对应氢化物稳定性越强;
D.氧元素没有最高正化合价.
解答 解:A.C、N、O都位于第二周期,其原子序数逐渐增大,原子半径逐渐减小,故A正确;
B.C、N、O位于同一周期,且原子序数逐渐增大,非金属性逐渐增强,则元素原子得电子能力逐渐增强,故B正确;
C.C、N、O的非金属性逐渐增强,则气态氢化物的稳定性逐渐增强,故C正确;
D.C、N元素的最高化合价逐渐升高,而O没有最高正价,故D错误;
故选D.
点评 本题考查了原子结构与元素周期律的关系,题目难度不大,明确元素周期律内容为解答关键,注意掌握原子结构与元素周期表、元素周期律的关系,试题侧重基础知识的考查,培养了学生的灵活应用能力.

练习册系列答案
 快乐小博士巩固与提高系列答案
快乐小博士巩固与提高系列答案
相关题目
10.在溶液中能大量共存的一组离子或分子是( )
| A. | NH4+、H+、NO3-、HCO3- | B. | K+、AlO2-、SO42-、NH3•H2O | ||
| C. | Na+、K+、SO32-、ClO- | D. | Na+、CH3COO-、SO42-、H+ |
1.设NA为阿伏加德罗常数的数值,下列说法正确的是( )
| A. | 1mol Na与乙醇完全反应,失去2NA电子 | |
| B. | 标准状况下,22.4L苯含NA个C6H6分子 | |
| C. | 0.5mol-OH和0.5mol OH-均含有5NA电子 | |
| D. | 常温常压,8gCH4含5NA个电子 |
18.下列说法正确的是( )
| A. | 油脂属于高分子化合物 | B. | 糖类都能水解 | ||
| C. | 酶是一类具有催化作用的蛋白质 | D. | 淀粉和纤维素属于同分异构体 |
5.元素在周期表中的位置,反映了元素的原子结构和元素的性质,下列说法正确的是( )
| A. | 主族金属元素和非金属元素在不同化合物中都可能呈不同的化合价 | |
| B. | 同一元素不可能既表现金属性,又表现非金属性 | |
| C. | 除氢外的短周期元素形成最高价化合物时,最外层都达到8电子稳定结构 | |
| D. | 同一主族的元素,化学性质也可能差异很大 |
2.下列有关物质的表达式不正确的是( )
| A. | 1,3-丁二烯的分子式:C4H6 | B. | 溴乙烷的电子式: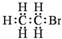 | ||
| C. | 甲醛的结构式: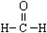 | D. | 葡萄糖的结构简式:CH2OH(CHOH)4CHO |
19.设NA表示阿伏加德罗常数,下列说法正确的是( )
| A. | 常温常压下的33.6L氯气与27g铝充分反应,转移电子数为3NA | |
| B. | 标准状况下,22.4LNO和11.2L氧气混合,气体的分子总数为1.5 NA | |
| C. | 7.8 g Na2O2含有的阴离子数目为0.1 NA | |
| D. | 80mL10mol/L的浓盐酸与足量MnO2反应,转移电子数为0.4NA |