题目内容
17.工业上合成氨的反应:N2(g)+3H2(g)?2NH3(g)△H=-92.60kJ•mol-1(1)下列说法能说明上述反应向正反应方向进行的是bd(填序号).
a.单位时间内生成2a mol NH3的同时生成3a mol H2
b.单位时间内生成6a mol N-H键的同时生成2a mol H-H键
c.用N2、H2、NH3的物质的量浓度变化表示的反应速率之比为1:3:2
d.混合气体的平均摩尔质量增大
e.容器内的气体密度不变
(2)已知合成氨反应在某温度下2L的密闭容器中进行,测得如表数据:根据表中数据计算:
| 时间(h) 物质的量(mol) | 0 | 2 | 4 | 6 |
| N2 | 1.50 | 1.20 | 1.00 | 1.00 |
| H2 | 4.50 | 3.60 | 3.00 | 3.00 |
| NH3 | 0 | m | 1.00 | 1.00 |
②根据计算可得m=0.6,0~2h内NH3的平均反应速率为0.15mol/(L•h),.
③此温度下反应:2NH3?N2+3H2的化学平衡常数K=6.75.
分析 (1)根据化学平衡状态的特征解答,当反应达到平衡状态时,正逆反应速率相等,各物质的浓度、百分含量不变,以及由此衍生的一些量也不发生变化,解题时要注意,选择判断的物理量,随着反应的进行发生变化,当该物理量由变化到定值时,说明可逆反应到达平衡状态;
(2)①依据反应的焓变结合化学方程式计算放出的热量;
②根据氨气的物质的量计算出消耗的氮气的物质的量,再根据v=$\frac{△c}{△t}$计算出0~2小时内N2的平均反应速度率;
③根据3、4小时的时间段氨气的物质的量不变,说明达到了平衡状态,根据氨气的物质的量计算出消耗的氮气和氢气的物质的量及平衡时的浓度,
再根据平衡常数表达式K=$\frac{{c}^{2}(N{H}_{3})}{c({N}_{2}){c}^{3}({H}_{2})}$计算出该温度下的平衡常数,逆反应的平衡常数为正反应平衡常数的倒数;
解答 解:(1)a.单位时间内生成2n mol NH3的同时生成3n mol H2,说明正逆反应速率相等,达到了平衡状态,故a不符合;
b.若达到平衡状态时,单位时间内生成6n mol N-H键的同时会生成3n mol H-H键,说明正反应速率大于逆反应速率,此时没有达到平衡状态,故b符合;
c.用N2、H2、NH3的物质的量浓度变化表示的反应速率之比为1:3:2,为正反应速率之比,但不能说明反应正向进行,与故c不符合;
d.混合气体的平均摩尔质量不变,说明总物质的量不变,正逆反应速率相等,达到化学平衡状态,故d符合;
e.混合气体的密度不变,反应发生到平衡这个量一直不变,故e不符合;
故答案为:bd;
(2)①N2(g)+3H2(g)?2NH3(g)△H=-92.20kJ•mol-1,生成2mol氨气放热92.30kJ,反应进行到4小时时,氮气的物质的量变化了1.5mol-1mol=0.5mol,则生成氨气1mol,放出的热量为$\frac{92.6}{2}$kJ/mol×1mol=46.30kJ,
故答案为:46.30;
②0~2小时内,反应氮气物质的量=1.5mol-1.2mol=0.3mol,生成了0.6mol氨气,根据反应N2(g)+3H2(g)?2NH3(g),0~2小时内N2的平均反应速度率为:v(NH3)=$\frac{\frac{0.6mol}{2L}}{2h}$0.15mol/(L•h),
故答案为:0.6,0.15mol/(L•h);
③根据表中数据可知,反应在第3和4小时时间段内氨气的物质的量不变,说明达到了平衡状态,此时生成了1.00mol氨气,
列出化学平衡的三段式为
N2(g)+3H2(g)?2NH3(g),
反应开始前(mol) 1.5 4.5 0
变化量(mol) 0.5 1.5 1
平衡时(mol) 1 3 1
平衡时浓度(mol/L) 0.500 1.500 0.5
此温度下该反应的化学平衡常数K=$\frac{{c}^{2}(N{H}_{3})}{c({N}_{2}){c}^{3}({H}_{2})}$=$\frac{0.{5}^{2}}{1.{5}^{3}×0.5}$=$\frac{1}{6.75}$,
此温度下反应:2NH3?N2+3H2的化学平衡常数K=6.75,
故答案为:6.75;
点评 本题考查了化学平衡状态的判断、反应热的计算、化学平衡常数的计算与应用、化学反应速率与化学计量数的关系等知识,涉及的知识点较多,试题综合性强,难度较大,有利于培养学生的逻辑思维能力和发散思维能力,提高学生的应试能力和学习效率.

 阅读快车系列答案
阅读快车系列答案| A. | 蒸馏操作时,应使温度计水银球靠近蒸馏烧瓶的支管口处 | |
| B. | 蒸发操作时,应使混合物中的水分完全蒸干后,才能停止加热 | |
| C. | 分液操作时,上层液体从下口放出 | |
| D. | 萃取操作时,应选择有机萃取剂,且萃取剂的密度必须比水大 |
 ,下列Ⅰ、Ⅱ、Ⅲ反应的类型正确的是( )
,下列Ⅰ、Ⅱ、Ⅲ反应的类型正确的是( )| A. | 加成、加成、氧化 | B. | 加成、氧化、氧化 | C. | 加成、取代、氧化 | D. | 取代、取代、加成 |
(1)CO可用于炼铁,
已知:Fe2O3(s)+3C(s)=2Fe(s)+3CO(g)△H1=+489.0kJ•mol-1
C(s)+CO2(g)=2CO(g)△H2=+172.5kJ•mol-1
则CO还原Fe2O3(s)的热化学方程式为Fe2O3(s)+3CO(g)=2Fe(s)+3CO2(g)△H=-28.5kJ/mol.
(2)分离高炉煤气得到的CO与空气可设计成燃料电池(以KOH溶液为电解液).写出该电池的正极反应式:O2+4e-+2H2O=4OH-.
(3)CO2和H2充人一定体积的密闭容器中,在两种温度下发生反应:
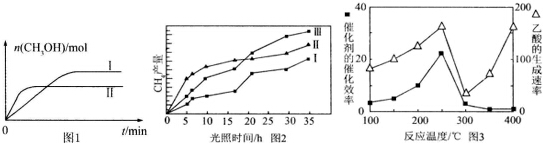
CO2(g)+3H2(g)?CH3OH(g)+H2O(g) 测得CH3OH的物质的量随时间的变化见图1.
①线Ⅰ、Ⅱ对应的平衡常数大小关系为KI>KⅡ (填“>”或“=”或“<”).
②一定温度下,在容积相同且固定的两个密闭容器中,按如下方式加入反应物,一段时间后达到平衡.
| 容器 | 甲 | 乙 |
| 反应物投入量 | 1mol CO2、3mol H2 | a mol CO2、b mol H2、 c mol CH3OH(g)、c molH2O(g) |
(4)利用光能和光催化剂,可将CO2和H2O(g)转化为CH4和O2.紫外光照射时,在不同催化
剂(Ⅰ、Ⅱ,Ⅲ)作用下,CH4产量随光照时间的变化见图2.在O~15小时内,CH4的平均生成速率Ⅰ、Ⅱ和Ⅲ从大到小的顺序为II>III>I(填序号).
(5)以TiO2/Cu2Al2O4 为催化剂,可以将CO2和CH4直接转化成乙酸.在不同温度下催化剂的催化效率与乙酸的生成速率的关系见图3.
①乙酸的生成速率主要取决于温度影响的范围是300℃~400℃.
②Cu2Al2O4可溶于稀硝酸,写出有关的离子方程式:3Cu2Al2O4+32H++2NO3-=6Cu2++6Al3++2NO↑+16H2O.
| A. | 配制溶液时,如果试样是液体,用量筒量取试样后直接倒入容量瓶中,缓慢加入蒸馏水到接近标线1cm~2cm处,用滴管滴加蒸馏水到标线 | |
| B. | 容量瓶用蒸馏水洗净后,再用待配溶液润洗 | |
| C. | 配制溶液时,如果试样是固体,把称好的试样用纸条小心倒入容量瓶中,缓慢加入蒸馏水到接近标线1cm~2cm处,用滴管滴加蒸馏水到标线 | |
| D. | 使用容量瓶前检查它是否漏水 |
⑦氨水 ⑧稀硝酸 ⑨KI
(1)按物质的分类方法填写表格的空白处(填物质编号)
| 分类标准 | 电解质 | 盐 | 非电解质 | 混合物 |
| 属于该类 的物质 |
| 装置 | 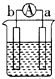 CuSO4溶液 | 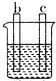 稀硫酸 |  稀硫酸 |
| 现象 | a极质量减小 b极质量增大 | b极有气泡 c极无明显现象 | 电流从a极流向d极 |
| A. | d>a>b>c | B. | b>c>d>a | C. | a>b>c>d | D. | a>b>d>c |