题目内容
下列离子方程式正确的是( )
| A、足量的CO2通入饱和碳酸钠溶液中:CO2+CO32-+H2O→2HCO3- |
| B、FeSO4溶液在空气中变质:4Fe2++O2+2H2O→4Fe3++4OH- |
| C、向NaAlO2溶液中通入过量CO2:2AlO2-+CO2+3H2O→2Al(OH)3↓+CO32- |
| D、碳酸氢镁溶液中加入过量石灰水:Mg2++2HCO3-+2Ca2++4OH-→2CaCO3↓+Mg(OH)2↓+2H2O |
考点:离子方程式的书写
专题:离子反应专题
分析:A.碳酸钠与CO2和水反应生成NaHCO3,NaHCO3溶解度小于Na2CO3;
B.FeSO4中Fe为+2价,所以极易被氧气氧化为+3价;
C.二氧化碳过量,偏铝酸钠溶液与二氧化碳反应生成了氢氧化铝和碳酸氢钠;
D.因氢氧化镁的溶解度小于碳酸镁,所以碳酸氢镁溶液中加入过量石灰水,碳酸氢根离子与氢氧根离子反应生成碳酸根离子,和钙离子结合生成沉淀,镁离子和氢氧根离子反应生成氢氧化镁的沉淀.
B.FeSO4中Fe为+2价,所以极易被氧气氧化为+3价;
C.二氧化碳过量,偏铝酸钠溶液与二氧化碳反应生成了氢氧化铝和碳酸氢钠;
D.因氢氧化镁的溶解度小于碳酸镁,所以碳酸氢镁溶液中加入过量石灰水,碳酸氢根离子与氢氧根离子反应生成碳酸根离子,和钙离子结合生成沉淀,镁离子和氢氧根离子反应生成氢氧化镁的沉淀.
解答:
解:A.碳酸钠与CO2和水反应生成酸式盐NaHCO3,NaHCO3溶解度小于Na2CO3,并且反应生成的NaHCO3固体质量比原来Na2CO3多,溶剂质量减少,溶液中有浑浊出现,反应的离子方程式为2Na++CO32-+H2O+CO2=2NaHCO3↓,故A错误;
B.FeSO4中Fe为+2价,具有还原性易被空气中的氧气氧化,发生4FeSO4 +O2 +2H2SO4═2Fe2(SO4)3 +2H2O,离子反应为4Fe2++O2+4H+═4Fe3++2H2O,故B错误;
C.偏铝酸钠溶液中通入过量二氧化碳,反应生成了氢氧化铝沉淀和碳酸氢钠,反应的离子方程式为:AlO2-+CO2+2H2O=Al(OH)3↓+HCO3-,故C错误;
D.碳酸氢镁溶液中加入过量石灰水n[Mg(HCO3)2]:n[Ca(OH)2]=1:2反应,所以离子反应为:Mg2++2HCO3-+2Ca2++4OH-═2CaCO3↓+Mg(OH)2↓+2H2O,故D正确;
故选D.
B.FeSO4中Fe为+2价,具有还原性易被空气中的氧气氧化,发生4FeSO4 +O2 +2H2SO4═2Fe2(SO4)3 +2H2O,离子反应为4Fe2++O2+4H+═4Fe3++2H2O,故B错误;
C.偏铝酸钠溶液中通入过量二氧化碳,反应生成了氢氧化铝沉淀和碳酸氢钠,反应的离子方程式为:AlO2-+CO2+2H2O=Al(OH)3↓+HCO3-,故C错误;
D.碳酸氢镁溶液中加入过量石灰水n[Mg(HCO3)2]:n[Ca(OH)2]=1:2反应,所以离子反应为:Mg2++2HCO3-+2Ca2++4OH-═2CaCO3↓+Mg(OH)2↓+2H2O,故D正确;
故选D.
点评:本题考查离子方程式的书写,解题时注意从化学式、离子符号、电荷守恒、是否符合反应实际的角度分析离子方程式的书写是否正确,注意ANaHCO3溶解度小于Na2CO3,题目难度中等.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
用铂电极电解CuSO4和KNO3的混合溶液1L,经过一段时间后,两极均得到标准状况下22.4L的气体,则原混合溶液中CuSO4的物质的量浓度为( )
| A、1.0mol/L |
| B、0.8mol/L |
| C、1.5mol/L |
| D、0.5mol/L |
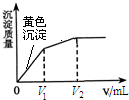 向10mL含等浓度的I-和Cl-的溶液中逐滴加入0.1mol?L-1的AgNO3溶液,沉淀的质量与加入AgNO3溶液体积的关系如图所示.下列说法不正确的是( )
向10mL含等浓度的I-和Cl-的溶液中逐滴加入0.1mol?L-1的AgNO3溶液,沉淀的质量与加入AgNO3溶液体积的关系如图所示.下列说法不正确的是( )| A、该实验可以证明AgI比AgCl更难溶 |
| B、加入V2 mL AgNO3溶液后,溶液中不含I- |
| C、V1=V2-V1 |
| D、向最终的沉淀中加入Na2S溶液,沉淀变成黑色 |
将下列溶液分别蒸干并灼烧,能得到溶质的是( )
| A、FeCl3 |
| B、AlCl3 |
| C、Na2CO3 |
| D、NaHCO3 |
关于钠原子和钠离子,下列叙述的正确是( )
| A、它们的化学性质相似 |
| B、它们电子层数相同 |
| C、钠原子半径比钠离子半径小 |
| D、钠原子、钠离子均为同一元素 |
若NA表示阿伏加德罗常数,下列说法正确的是( )
| A、在Na2O、Na2O2中,阳离子和阴离子个数比分别是2:1和1:1 |
| B、常温常压下,11.2L SO2气体中含有的分子数为0.5NA |
| C、一定条件下,密闭容器充入1mol N2和3mol H2充分反应,转移电子的数目为6NA |
| D、Na2CO3溶液中,若CO32-数目为NA,则Na+数目大于2NA |
 已知甲、乙、丙、X、Y为中学化学常见物质,其中甲、乙、丙中均含有元素A,其转化关系如图所示(反应条件已省略):
已知甲、乙、丙、X、Y为中学化学常见物质,其中甲、乙、丙中均含有元素A,其转化关系如图所示(反应条件已省略):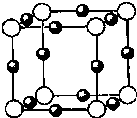 【化学--选修3:物质结构与性质】
【化学--选修3:物质结构与性质】