题目内容
下列溶液中物质的量浓度肯定为1mol/L的是( )
| A、将40gNaOH固体溶解于1L水中 |
| B、将22.4L氯化氢气体溶于水配成1L溶液 |
| C、4gNaOH固体溶解在水中配成100mL溶液 |
| D、将1L10mol/L浓盐酸与10L水混合 |
考点:物质的量浓度的相关计算
专题:物质的量浓度和溶解度专题
分析:A.溶液的体积不等于溶剂的体积;
B.22.4L氯化氢气体的物质的量不一定等于1mol;
C.4g NaOH的物质的量为0.1mol,溶液的体积为0.1L;
D.混合溶液的体积不等于10L.
B.22.4L氯化氢气体的物质的量不一定等于1mol;
C.4g NaOH的物质的量为0.1mol,溶液的体积为0.1L;
D.混合溶液的体积不等于10L.
解答:
解;A.40g NaOH的物质的量为1mol,溶液的体积不等于溶剂的体积,溶液的体积不是1L,因此溶液中物质的量浓度不是1mol/L,故A错误;
B.22.4L氯化氢气体的物质的量不一定等于1mol,因此溶液中物质的量浓度不是1mol/L,故B错误;
C.4g NaOH的物质的量为0.1mol,溶液的体积为0.1L,则c=
=1moL/L,故C正确;
D.混合溶液的体积不等于10L,根据稀释定律可知混合液的物质的量浓度不是1mol/L,故D错误.
故选C.
B.22.4L氯化氢气体的物质的量不一定等于1mol,因此溶液中物质的量浓度不是1mol/L,故B错误;
C.4g NaOH的物质的量为0.1mol,溶液的体积为0.1L,则c=
| 0.1mol |
| 0.1L |
D.混合溶液的体积不等于10L,根据稀释定律可知混合液的物质的量浓度不是1mol/L,故D错误.
故选C.
点评:本题考查了物质的量浓度,为高频考点,侧重于学生的分析能力和计算能力的考查,题目难度不大,注意溶液的体积不等于溶剂的体积,不等于溶剂的体积加上溶质的体积.

练习册系列答案
相关题目
在一定条件下,NO能跟H2发生如下反应:2NO+2H2═N2+2H2O.经研究,上述反应是按以下三步反应依次进行的总反应(括号中是该条件下反应的相对速率):(Ⅰ)2NO+H2═N2O+H2O(慢);(Ⅱ)2N2O═2N2+O2(快);(Ⅲ)2H2+O2═2H2O(更快).以上总反应的速率主要取决于三步反应中的( )
| A、(Ⅰ) | B、(Ⅱ) |
| C、(Ⅲ) | D、(Ⅱ)和(Ⅲ) |
X、Y、Z为中学化学常见的物质,其转化关系如图所示(“→”表示一步转化),下列组合不正确的是( )

| 选项 | X | Y | Z |
| A | NaCl | NaHCO3 | NaOH |
| B | SiO2 | H2SiO3 | Na2SiO3 |
| C | H2SO3 | SO2 | H2SO4 |
| D | HClO | Cl2 | HCl |
| A、A | B、B | C、C | D、D |
已知火箭燃料二甲基肼(CH3-NH-NH-CH3)的燃烧热为-6 000kJ?mol-1,则30g二甲基肼完全燃烧放出的热量为( )
| A、3000 kJ |
| B、1500 KJ |
| C、6 000 kJ |
| D、12 000 kJ |
将4g NaOH溶于水配成50mL溶液,取出5mL,这5mL溶液的物质的量浓度是( )
| A、2 mol/L |
| B、1 mol/L |
| C、0.1 mol/L |
| D、0.05 mol/L |
下列反应中属吸热反应的是( )
| A、Zn与稀硫酸反应放出氢气 |
| B、酸碱中和反应 |
| C、硫在空气或氧气中燃烧 |
| D、Ba(OH)2?8H2O与NH4Cl反应 |

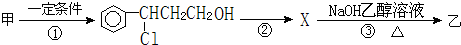
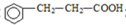 ).写出同时符合下列要求的丙的同分异构体结构简式
).写出同时符合下列要求的丙的同分异构体结构简式