题目内容
工业上从铝土矿(含氧化铝、氧化铁等)制取铝的部分流程如下:

滤液经处理得到Al2O3,再电解得到Al:2Al2O3
4Al+3O2↑经分析原料和残渣的部分成分见下表:
已知铝土矿中Fe2O3全部转入赤泥,则:
(1)生产中每消耗1t铝土矿,将产生多少t赤泥?
(2)若由滤液到制得产品铝的过程中原料均没有损失,则整个生产过程中Al2O3的转化率为多少?
(3)每炼出1t铝理论上需铝土矿的质量为多少t?

滤液经处理得到Al2O3,再电解得到Al:2Al2O3
| ||
| Al2O3 | Fe2O3 | |
| 铝土矿 | 55% | 16% |
| 赤 泥 | 15% | 48% |
(1)生产中每消耗1t铝土矿,将产生多少t赤泥?
(2)若由滤液到制得产品铝的过程中原料均没有损失,则整个生产过程中Al2O3的转化率为多少?
(3)每炼出1t铝理论上需铝土矿的质量为多少t?
考点:化学方程式的有关计算
专题:计算题
分析:(1)计算铝土矿中氧化铁的质量,反应中Fe2O3的质量不变,结合赤泥中氧化铁的质量分数,进而计算赤泥的质量;
(2)计算铝土矿中氧化铝的质量,再计算赤泥中氧化铝的质量,进而计算整个生产过程中Al2O3的转化率;
(3)根据方程式计算生成1t铝需要氧化铝的质量,结合氧化铝的转化率计算铝土矿中氧化铝的总质量,结合其质量分数计算铝土矿的质量.
(2)计算铝土矿中氧化铝的质量,再计算赤泥中氧化铝的质量,进而计算整个生产过程中Al2O3的转化率;
(3)根据方程式计算生成1t铝需要氧化铝的质量,结合氧化铝的转化率计算铝土矿中氧化铝的总质量,结合其质量分数计算铝土矿的质量.
解答:
解:(1)1t铝土矿中氧化铁的质量为1t×16%,
赤泥中氧化铁的质量分数为48%,反应中Fe2O3的质量不变,
则赤泥的质量为:
=
t,
答:生产中每消耗1t铝土矿,将产生赤泥
t;
(2)1t铝土矿中氧化铝的质量为1t×55%,赤泥中氧化铝的质量为
t×15%,
故氧化铝的转化率为:[(1t×55%)-(
t×15%)]÷1t×55%=90.9%,
答:整个生产过程中Al2O3的转化率为90.9%;
(3)设生成1t铝需要氧化铝的质量为x,则:
2Al2O3
4Al+3O2↑
204 108
x 1t
故x=
t
故铝土矿中氧化铝的质量为
t÷90.9%=2.078t
故需要铝土矿的质量为2.078t÷55%=3.78t
答:每炼出1t铝理论上需铝土矿的质量为3.78t.
赤泥中氧化铁的质量分数为48%,反应中Fe2O3的质量不变,
则赤泥的质量为:
| 1t×16% |
| 48% |
| 1 |
| 3 |
答:生产中每消耗1t铝土矿,将产生赤泥
| 1 |
| 3 |
(2)1t铝土矿中氧化铝的质量为1t×55%,赤泥中氧化铝的质量为
| 1 |
| 3 |
故氧化铝的转化率为:[(1t×55%)-(
| 1 |
| 3 |
答:整个生产过程中Al2O3的转化率为90.9%;
(3)设生成1t铝需要氧化铝的质量为x,则:
2Al2O3
| ||
204 108
x 1t
故x=
| 204 |
| 108 |
故铝土矿中氧化铝的质量为
| 204 |
| 108 |
故需要铝土矿的质量为2.078t÷55%=3.78t
答:每炼出1t铝理论上需铝土矿的质量为3.78t.
点评:本题考查混合物计算、化学方程式有关计算,难度中等,关键是明确整个过程中氧化铁的质量不变.

练习册系列答案
相关题目
肼(N2H4)-空气燃料电池是一种环保型碱性燃料电池,电解质溶液是20%~30%的KOH溶液.电池总反应为:N2H4+O2=N2↑+2H2O.下列关于该燃料电池工作时的说法正确的是( )
| A、负极的电极反应式是:N2H4+4OH--4e-=4H2O+N2↑ |
| B、正极的电极反应式是:O2+4H++4e-=2H2O |
| C、溶液中阴离子向正极移动 |
| D、溶液中C﹙OH-﹚保持不变 |
自然科学史中很多发现和发明都是通过类比推理法提出来的.现有化合物A的结构简式
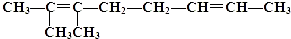 .它与过量的酸性高锰酸钾溶液作用得到下列三种化合物:
.它与过量的酸性高锰酸钾溶液作用得到下列三种化合物: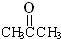 ,
,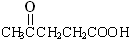 ,CH3COOH.若化合物B与A互为同分异构体,且A、B分别与酸性高锰酸钾溶液反应得到的产物相同,则化合物B的结构简式正确的是( )
,CH3COOH.若化合物B与A互为同分异构体,且A、B分别与酸性高锰酸钾溶液反应得到的产物相同,则化合物B的结构简式正确的是( )
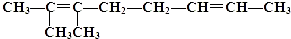 .它与过量的酸性高锰酸钾溶液作用得到下列三种化合物:
.它与过量的酸性高锰酸钾溶液作用得到下列三种化合物: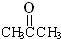 ,
,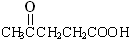 ,CH3COOH.若化合物B与A互为同分异构体,且A、B分别与酸性高锰酸钾溶液反应得到的产物相同,则化合物B的结构简式正确的是( )
,CH3COOH.若化合物B与A互为同分异构体,且A、B分别与酸性高锰酸钾溶液反应得到的产物相同,则化合物B的结构简式正确的是( )| A、CH3CH=C(CH3)-(CH2)2-C(CH3)=CHCH3 |
| B、(CH3)2C=CH-(CH2)2-C(CH3)=CHCH3 |
| C、(CH3)2C=C(CH3)-(CH2)2-CH=CHCH3 |
| D、( CH3)2C=CH-(CH2)2-CH=C(CH3)2 |
下列溶液中物质的量浓度肯定为1mol/L的是( )
| A、将40gNaOH固体溶解于1L水中 |
| B、将22.4L氯化氢气体溶于水配成1L溶液 |
| C、4gNaOH固体溶解在水中配成100mL溶液 |
| D、将1L10mol/L浓盐酸与10L水混合 |
下列说法正确的是( )
| A、将 100g10%的盐酸加热蒸发,得到 50 g溶液,其浓度为20% |
| B、把3mol/L的硫酸与等体积的水混合,所得溶液的浓度大于1.5 mol/L |
| C、把200mL3mol/L的BaCl2溶液跟100mL3mol/L的KCl溶液混合后,溶液中的c(Cl-)仍然是3 mol/L |
| D、已知某温度下KNO3的溶解度是 31.6 g/100 g水,在该温度下将 20 g的KNO3溶于 50 g的水中,所得溶液的质量分数是28.6% |
下列有关摩尔质量的描述或应用中,正确的是( )
| A、1 mol OH-的质量为17 g |
| B、二氧化碳的摩尔质量为44 g |
| C、铁原子的摩尔质量等于它的相对原子质量 |
| D、摩尔是表示物质的数量单位 |