题目内容
从樟科植物枝叶提取的精油中含有下列甲、乙两种成分:③

(1)乙中所含官能团的名称为 ;
(2)由甲转化为乙需经下列过程(已略去各步反应的无关产物,下同):
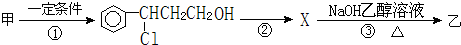
设计步骤①的目的是 ;反应②的化学方程式为 (注明反应条件).
(3)写出用银氨溶液检验乙中含氧官能团的方程式:
(4)乙经过氢化、氧化得到丙(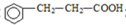 ).写出同时符合下列要求的丙的同分异构体结构简式 、
).写出同时符合下列要求的丙的同分异构体结构简式 、
①能发生银镜反应;②能与FeCl3溶液发生显色反应;③核磁共振氢谱图上产生4个吸收峰.

(1)乙中所含官能团的名称为
(2)由甲转化为乙需经下列过程(已略去各步反应的无关产物,下同):
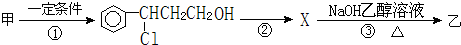
设计步骤①的目的是
(3)写出用银氨溶液检验乙中含氧官能团的方程式:
(4)乙经过氢化、氧化得到丙(
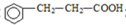 ).写出同时符合下列要求的丙的同分异构体结构简式
).写出同时符合下列要求的丙的同分异构体结构简式①能发生银镜反应;②能与FeCl3溶液发生显色反应;③核磁共振氢谱图上产生4个吸收峰.
考点:有机物的结构和性质,有机物分子中的官能团及其结构
专题:有机物的化学性质及推断
分析:(1)乙中的官能团有C=C、-CHO;
(2)C=C易被氧化,反应①为甲与HCl加成反应,反应②为催化氧化;
(3)检验乙中的醛基,与银氨溶液发生反应生成银镜;
(4)丙为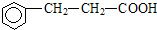 ,其同分异构体中①能发生银镜反应,则含-CHO;②能与FeCl3溶液发生显色反应,则含酚-OH;③分子中有四种不同化学环境的H原子,则苯环上和甲基中各有1种位置的H,以此来解答.
,其同分异构体中①能发生银镜反应,则含-CHO;②能与FeCl3溶液发生显色反应,则含酚-OH;③分子中有四种不同化学环境的H原子,则苯环上和甲基中各有1种位置的H,以此来解答.
(2)C=C易被氧化,反应①为甲与HCl加成反应,反应②为催化氧化;
(3)检验乙中的醛基,与银氨溶液发生反应生成银镜;
(4)丙为
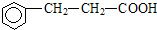 ,其同分异构体中①能发生银镜反应,则含-CHO;②能与FeCl3溶液发生显色反应,则含酚-OH;③分子中有四种不同化学环境的H原子,则苯环上和甲基中各有1种位置的H,以此来解答.
,其同分异构体中①能发生银镜反应,则含-CHO;②能与FeCl3溶液发生显色反应,则含酚-OH;③分子中有四种不同化学环境的H原子,则苯环上和甲基中各有1种位置的H,以此来解答.解答:
解:(1)乙中的官能团有-CHO、C=C,其名称为醛基、碳碳双键,故答案为:醛基、碳碳双键;
(2)反应①为甲与HCl加成反应,在催化氧化羟基时,C=C也能被氧化,所以要把双键转化为饱和键,加以保护;反应②为羟基的催化氧化反应,该反应为 ,
,
故答案为:保护碳碳双键; ;
;
(3)醛基与银氨溶液发生银镜反应来检验,反应为C6H5CH=CHCHO+2Ag(NH3)2OH
C6H5CH=CHCOONH4+NH3+2Ag+3H2O,
故答案为:C6H5CH=CHCHO+2Ag(NH3)2OH
C6H5CH=CHCOONH4+NH3+2Ag+3H2O;
(4)丙为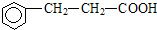 ,其同分异构体中①能发生银镜反应,则含-CHO;②能与FeCl3溶液发生显色反应,则含酚-OH;③分子中有四种不同化学环境的H原子,则苯环上和甲基中各有1种位置的H,符合条件的同分异构体为
,其同分异构体中①能发生银镜反应,则含-CHO;②能与FeCl3溶液发生显色反应,则含酚-OH;③分子中有四种不同化学环境的H原子,则苯环上和甲基中各有1种位置的H,符合条件的同分异构体为 、
、 ,
,
故答案为: ;
; .
.
(2)反应①为甲与HCl加成反应,在催化氧化羟基时,C=C也能被氧化,所以要把双键转化为饱和键,加以保护;反应②为羟基的催化氧化反应,该反应为
 ,
,故答案为:保护碳碳双键;
 ;
;(3)醛基与银氨溶液发生银镜反应来检验,反应为C6H5CH=CHCHO+2Ag(NH3)2OH
| △ |
故答案为:C6H5CH=CHCHO+2Ag(NH3)2OH
| △ |
(4)丙为
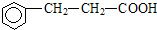 ,其同分异构体中①能发生银镜反应,则含-CHO;②能与FeCl3溶液发生显色反应,则含酚-OH;③分子中有四种不同化学环境的H原子,则苯环上和甲基中各有1种位置的H,符合条件的同分异构体为
,其同分异构体中①能发生银镜反应,则含-CHO;②能与FeCl3溶液发生显色反应,则含酚-OH;③分子中有四种不同化学环境的H原子,则苯环上和甲基中各有1种位置的H,符合条件的同分异构体为 、
、 ,
,故答案为:
 ;
; .
.
点评:本题考查有机物的结构与性质,明确有机物中的官能团及其性质的关系即可解答,注意(4)中同分异构体的分析为解答的易错点,题目难度中等.

练习册系列答案
相关题目
在温度不变的条件下,密闭容器中发生如下反应:2SO2+O2?2SO3,下列叙述能够说明反应已经达到平衡状态的是( )
| A、反应容器中压强不随时间变化 |
| B、容器中SO2、O2、SO3的物质的量之比为2:1:2 |
| C、SO2与SO3的浓度相等 |
| D、容器中SO2、O2、SO3共存 |
下列说法正确的是( )
| A、放热反应发生时不必加热,吸热反应在加热后才能发生 |
| B、反应热指的是反应过程中放出的热量 |
| C、反应热的大小与反应的途径有关,无论是一步完成还是分几步完成,其反应热基本相同 |
| D、依据盖斯定律,热化学方程式具有加合性,也可以进行加、减、乘、除四则运算 |
下列说法正确的是( )
| A、汽油、柴油和植物油都是碳氢化合物 |
B、β-月桂烯的结构如图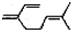 ,一分子该物质与两分子溴发生加成反应的产物(只考虑位置异构)理论上最多有3种 ,一分子该物质与两分子溴发生加成反应的产物(只考虑位置异构)理论上最多有3种 |
| C、植物油通过加氢可以变为脂肪 |
| D、煤中含有苯、甲苯、二甲苯等芳香烃,可通过干馏制取 |
肼(N2H4)-空气燃料电池是一种环保型碱性燃料电池,电解质溶液是20%~30%的KOH溶液.电池总反应为:N2H4+O2=N2↑+2H2O.下列关于该燃料电池工作时的说法正确的是( )
| A、负极的电极反应式是:N2H4+4OH--4e-=4H2O+N2↑ |
| B、正极的电极反应式是:O2+4H++4e-=2H2O |
| C、溶液中阴离子向正极移动 |
| D、溶液中C﹙OH-﹚保持不变 |
下列溶液中物质的量浓度肯定为1mol/L的是( )
| A、将40gNaOH固体溶解于1L水中 |
| B、将22.4L氯化氢气体溶于水配成1L溶液 |
| C、4gNaOH固体溶解在水中配成100mL溶液 |
| D、将1L10mol/L浓盐酸与10L水混合 |
下列有关离子方程式书写正确的( )
| A、在强碱溶液中次氯酸钠与Fe(0H)3反应生成Na2FeO4:3ClO-+2Fe(0H)3=2FeO42-+3Cl-+H2O+4H+ |
| B、从酸化的海带灰浸出液中提取碘:2I-+H2O2=I2+2OH- |
| C、以金属银为阳极电解饱和硫酸铜溶液:Cu2++2 H2O=2Cu+O2 ↑+4H+ |
| D、过氧化氢能使酸性KMnO4溶液褪色:5H2O2+2MnO4-+6H+=2Mn2++5O2↑+8H2O |