题目内容
16.有机物甲、乙的结构如图所示.下列说法错误的是( )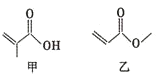
| A. | 甲、乙互为同分异构体 | |
| B. | 一定条件下,甲、乙均能发生取代反应 | |
| C. | 甲、乙都能与金属钠反应生成氢气 | |
| D. | 甲、乙都能使酸性KMnO4溶液褪色 |
分析 A.分子式相同结构不同的有机物互称同分异构体;
B.甲含有羧基、乙含有酯基,甲能发生酯化反应、乙能发生水解反应;
C.羧基、羟基能和钠反应生成氢气;
D.碳碳双键能被酸性高锰酸钾溶液氧化而使酸性高锰酸钾溶液褪色.
解答 解:A.分子式相同结构不同的有机物互称同分异构体,甲、乙分子式相同、结构不同,属于同分异构体,故A正确;
B.甲含有羧基、乙含有酯基,甲能发生酯化反应、乙能发生水解反应,酯化反应和水解反应都属于取代反应,所以甲乙都能发生取代反应,故B正确;
C.羧基、羟基能和钠反应生成氢气,甲含有羧基,乙不含羧基或羟基,所以甲能和钠反应、乙不能和钠反应,故C错误;
D.碳碳双键能被酸性高锰酸钾溶液氧化而使酸性高锰酸钾溶液褪色,甲乙都含有碳碳双键,所以都能被酸性高锰酸钾溶液氧化而使酸性高锰酸钾溶液褪色,故D正确;
故选C.
点评 本题考查有机物结构和性质,为高频考点,明确官能团及其性质关系是解本题关键,涉及反应类型、基本概念、物质性质等知识点,侧重考查烯烃、羧酸、酯的性质.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
7.根据杂化轨道理论判断下列分子的空间构型是V形的是 ( )(填写序号)
| A. | BeCl2 | B. | H2O | C. | HCHO | D. | CS2 |
4.设NA为阿伏伽德罗常数的值.下列说法正确的是( )
| A. | 5.6g铁与足量稀硝酸反应,转移电子的数目为0.2NA | |
| B. | 标准状况下,22.4 L二氯甲烷的分子数约为NA | |
| C. | 8.8g乙酸乙酯中含共用电子对数为1.4NA | |
| D. | 1L 0.1mol•L-1氯化铜溶液中铜离子数为0.1NA |
11.实验:
①0.005mol•L-1 FeCl3溶液和0.015mol•L-1 KSCN溶液各1mL混合得到红色溶液
a,均分溶液a置于b、c两支试管中;
②向b中滴加3滴饱和FeCl3溶液,溶液颜色加深;
③再向上述b溶液中滴加3滴1mol•L-1 NaOH溶液,溶液颜色变浅且出现浑浊;
④向c中逐渐滴加1mol•L-1 KSCN溶液2mL,溶液颜色先变深后变浅.
下列分析不正确的是( )
①0.005mol•L-1 FeCl3溶液和0.015mol•L-1 KSCN溶液各1mL混合得到红色溶液
a,均分溶液a置于b、c两支试管中;
②向b中滴加3滴饱和FeCl3溶液,溶液颜色加深;
③再向上述b溶液中滴加3滴1mol•L-1 NaOH溶液,溶液颜色变浅且出现浑浊;
④向c中逐渐滴加1mol•L-1 KSCN溶液2mL,溶液颜色先变深后变浅.
下列分析不正确的是( )
| A. | 实验②中增大Fe3+浓度使平衡Fe3++3SCN-?Fe(SCN)3正向移动 | |
| B. | 实验③中发生反应:Fe3++3OH-═Fe(OH)3↓ | |
| C. | 实验③和④中溶液颜色变浅的原因相同 | |
| D. | 实验②、③、④均可说明浓度改变对平衡移动的影响 |
8.X、Y、Z、W是原子序数依次增大的四种短周期主族元素,Y、Z是金属元素,Y的单质能与水剧烈反应,Z可形成含氧酸根离子;X与W同主族,且可形成原子个数比为2:l、3:1的两种常见物质.下列说法正确的是( )
| A. | Y的单质可从Z的盐溶液中置换出Z | |
| B. | 简单氮化物的热稳定性:X<W | |
| C. | 简单离子的半径:W>X>Y>Z | |
| D. | X分别与Y、Z形成的化合物中只含有离子键 |
5.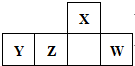 短周期元素X、Y、Z、W在周期表中的位置如图所示,其中Y所处的周期数和族序数相等,下列判断错误的是( )
短周期元素X、Y、Z、W在周期表中的位置如图所示,其中Y所处的周期数和族序数相等,下列判断错误的是( )
 短周期元素X、Y、Z、W在周期表中的位置如图所示,其中Y所处的周期数和族序数相等,下列判断错误的是( )
短周期元素X、Y、Z、W在周期表中的位置如图所示,其中Y所处的周期数和族序数相等,下列判断错误的是( )| A. | 最简单气态氢化物的热稳定性:X>Z | |
| B. | 最高价氧化物对应水化物的酸性:Z<W | |
| C. | 原子半径:Y>Z>X | |
| D. | 含Y的盐溶液一定呈酸性 |
 某有机物X的键线式为
某有机物X的键线式为 .
. ,
, .
.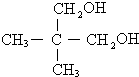 .
.
