题目内容
4.设NA为阿伏伽德罗常数的值.下列说法正确的是( )| A. | 5.6g铁与足量稀硝酸反应,转移电子的数目为0.2NA | |
| B. | 标准状况下,22.4 L二氯甲烷的分子数约为NA | |
| C. | 8.8g乙酸乙酯中含共用电子对数为1.4NA | |
| D. | 1L 0.1mol•L-1氯化铜溶液中铜离子数为0.1NA |
分析 A.铁和硝酸反应后,最终可能变为+3价,也可能变为+2价;
B.气体摩尔体积使用对象为气体;
C.乙酸乙酯分子中含有14对共用电子对,根据n=$\frac{m}{M}$计算乙酸乙酯的物质的量,再根据N=nNA计算共用电子对数;
D.铜离子为弱碱阳离子,水溶液中部分水解.
解答 解:A.5.6g铁的物质的量为0.1mol,而铁和硝酸反应后,最终可能变为+3价,也可能变为+2价,故0.1mol铁反应后转移的电子数可能为0.2NA个,也可能为0.3NA个,故A错误;
B.标准状况下,二氯甲烷为液体,不能使用气体摩尔体积,故B错误;
C.乙酸乙酯分子中含有14对共用电子对,8.8g乙酸乙酯的物质的量为$\frac{8.8g}{88g/mol}$=0.1mol,8.8g乙酸乙酯中共用电子对数为0.1mol×14×NAmol-1=1.4NA,故C正确;
D.铜离子为弱碱阳离子,水溶液中部分水解,1L 0.1mol•L-1氯化铜溶液中铜离子数小于0.1NA,故D错误;
故选:C.
点评 本题考查了阿伏伽德罗常数的有关计算,掌握物质的量的计算公式和物质结构是解题关键,注意气体摩尔体积使用条件和对象,注意盐类水解规律,题目难度中等.

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目
14.化学与环境、生活密切相关,下列与化学有关的说法正确的是( )
| A. | 春节燃放爆竹对环境无污染 | |
| B. | “酸雨”是由大气中的碳、氮、硫的氧化物溶于雨水造成 | |
| C. | 雾霾是一种分散系,分散剂是空气,带活性炭口罩防雾霾的原理是吸附原理 | |
| D. | 光化学烟雾的产生与人为排放大气污染物氮氧化物无关 |
19.处于固体状态的下列物质,其晶体类型按照离子晶体、分子晶体、原子晶体顺序排列的是( )
| A. | CH3COONH4、H2O、水晶 | B. | H2SO4、硫磺、石墨 | ||
| C. | KOH、SO3、Ar | D. | Ba(OH)2、玻璃、金刚石 |
9.下列解释事实的方程式不正确的是( )
| A. | 硝酸型酸雨的形成:3NO2+H2O═2HNO3+NO | |
| B. | 用Fe2(SO4)3做净水剂:Fe3++3H2O?Fe(OH)3+3H+ | |
| C. | 水垢中的CaSO4用Na2CO3溶液处理:Ca2++CO32-═CaCO3↓ | |
| D. | 向5 mL 0.1mol•L-1的K2Cr2O7溶液中滴加5滴浓硫酸,溶液橙色变深:Cr2O72-(橙色)+H2O?2CrO42-(黄色)+2H+ |
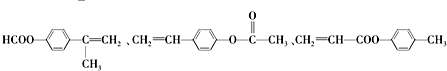
16.有机物甲、乙的结构如图所示.下列说法错误的是( )
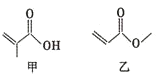
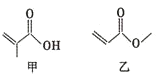
| A. | 甲、乙互为同分异构体 | |
| B. | 一定条件下,甲、乙均能发生取代反应 | |
| C. | 甲、乙都能与金属钠反应生成氢气 | |
| D. | 甲、乙都能使酸性KMnO4溶液褪色 |
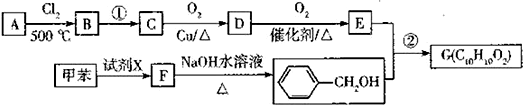
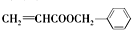 .
. .
. .
. .
.