题目内容
19.在甲酸的下列性质中,可以证明它是弱电解质的是( )| A. | 在相同条件下,甲酸的导电性比强酸溶液的导电性弱 | |
| B. | 甲酸能与水以任意比互溶 | |
| C. | 10mL 1mol/L甲酸恰好跟10 mL 1mol/L NaOH溶液完全反应 | |
| D. | 1mol/L甲酸溶液中c(H+)约为1×10-2mol/L |
分析 A、溶液的导电性取决于自由移动离子浓度和自由移动离子带电数目;
B、甲酸与水以任意比例互溶,这是甲酸的物理性质,不能证明是弱电解质;
C、是中和反应,按照反应方程式进行;
D、甲酸是弱电解质,不能完全电离.
解答 解:A、溶液的导电性取决于自由移动离子浓度和自由移动离子带电数目,与电解质的强弱无关,故A错误;
B.甲酸水溶性是物理性质,不能证明是弱电解质,故B错误;
C.根据方程式可知不论酸碱强弱,只有一元酸与一元碱物质的量相等则恰好发生酸碱中和,完全反应,故C错误;
D、1mol•L-1的甲酸溶液的c(H+)约为0.01mol•L-1说明甲酸不能完全电离,可以证明是弱电解质,故D正确;
故选D.
点评 本题考查了弱电解质的判断,题目难度不大,注意把握住弱电解质的定义“部分电离”的特点.

练习册系列答案
相关题目
16.如图为元素周期表前四周期的一部分,下列有关R、W、X、Y、Z五种元素的叙述中,正确的是( )


| A. | 常压下五种元素的单质中Z单质的沸点最高 | |
| B. | X和W的常见单质的分子式分别为X2和W2 | |
| C. | W的氢化物沸点比X的氢化物的沸点低 | |
| D. | R最高氧化物水化物的酸性最强 |
17.下列说法中,不正确的是( )
| A. | 利用焰色反应可鉴别K2CO3溶液和Na2CO3溶液 | |
| B. | 利用丁达尔效应可鉴别溶液和胶体 | |
| C. | 运用蒸馏的方法,可以分离沸点相差较大的液体混合物 | |
| D. | 广范pH试纸测得某碱性溶液的pH为12.5 |
7.(1)将不同物质的量的H2O(g)和CO(g)分别通入体积为2L的恒容密闭容器中,进行反应:H2O(g)+CO(g)?CO2(g)+H2(g),得到如下三组数据:
①实验组i中以v(CO2)表示的反应速率为0.16mol•L-1•min-1,温度升高时平衡常数会减小(填“增大”、“减小”或“不变”).
②若a=2,b=1,则c=0.6,达平衡时实验组ii中H2O(g)和实验组iii中CO的转化率的关系为αii (H2O)=αiii (CO)(填“<”、“>”或“=”).
(2)CO分析仪的传感器可测定汽车尾气是否符合排放标准,该分析仪的工作原理类似于
燃料电池,其中电解质是氧化钇(Y2O3)和氧化锆(ZrO2)晶体,能传导O2-.
①则负极的电极反应式为CO+2O2--2e-=CO32-.
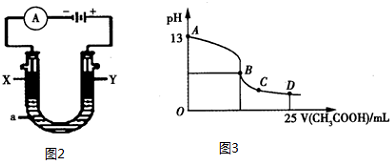
②以上述电池为电源,通过导线连接成图2.若X、Y为石墨,a为2L 0.1mol/L KCl溶液,写出电解总反应的离子方程式2Cl-+2H2O$\frac{\underline{\;电解\;}}{\;}$Cl2↑+H2↑+2OH-.电解一段时间后,取25mL上述电解后的溶液,滴加0.4mol/L醋酸得到图3曲线(不考虑能量损失和气体溶于水,溶液体积变化忽略不计).根据图二计算,上述电解过程中消耗一氧化碳的质量为2.8g.
| 实验组 | 温度/℃ | 起始量/mol | 平衡量/mol | 达到平衡所需时间/min | ||
| H2O | CO | CO | H2 | |||
| i | 650 | 2 | 4 | 2.4 | 1.6 | 5 |
| ii | 900 | 1 | 2 | 1.6 | 0.4 | 3 |
| iii | 900 | a | b | c | d | t |
②若a=2,b=1,则c=0.6,达平衡时实验组ii中H2O(g)和实验组iii中CO的转化率的关系为αii (H2O)=αiii (CO)(填“<”、“>”或“=”).
(2)CO分析仪的传感器可测定汽车尾气是否符合排放标准,该分析仪的工作原理类似于
燃料电池,其中电解质是氧化钇(Y2O3)和氧化锆(ZrO2)晶体,能传导O2-.
①则负极的电极反应式为CO+2O2--2e-=CO32-.
②以上述电池为电源,通过导线连接成图2.若X、Y为石墨,a为2L 0.1mol/L KCl溶液,写出电解总反应的离子方程式2Cl-+2H2O$\frac{\underline{\;电解\;}}{\;}$Cl2↑+H2↑+2OH-.电解一段时间后,取25mL上述电解后的溶液,滴加0.4mol/L醋酸得到图3曲线(不考虑能量损失和气体溶于水,溶液体积变化忽略不计).根据图二计算,上述电解过程中消耗一氧化碳的质量为2.8g.

14.等物质的量的下列有机物完全燃烧,消耗O2最多的是( )
| A. | C2H4 | B. | CH3CH2OH | C. | C6H6 | D. | CH3COOH |
4.用铁片与2mol/L稀硫酸反应制取氢气时,下列措施不能使氢气生成速率减小的是( )
| A. | 加少量CH3COONa固体 | B. | 加水 | ||
| C. | 加少量CuSO4固体 | D. | 加等量等浓度Na2SO4溶液 |
11.元素化合价一般决定于原子的( )
| A. | 核内质子数 | B. | 核外电子数 | C. | 核外电子层数 | D. | 最外层电子数 |