题目内容
11.元素化合价一般决定于原子的( )| A. | 核内质子数 | B. | 核外电子数 | C. | 核外电子层数 | D. | 最外层电子数 |
分析 元素在形成化合物时,原子结构中最外层电子多于4个易得电子,最外层少于4个易失去电子可知,元素的最外层电子数决定元素的化合价,以此解答该题.
解答 解:主族元素(包括金属元素)原子的价电子就是最外层电子,故化合价决定于最外层电子数,过渡元素的化合价不仅与最外层电子有关,还与次外层电子有关,甚至与倒数第三层电子有关,比较复杂,中学阶段不做要求,但元素的化合价与核内质子数、核外电子层数无关.
故选D.
点评 本题考查原子结构与元素的性质,为高频考点,侧重于学生的分析能力的考查,题目难度不大,本题注意原子核外电子数与元素的性质的关系.

练习册系列答案
 小学期末标准试卷系列答案
小学期末标准试卷系列答案
相关题目
8.下列事实或性质与胶体没有直接关系的是( )
| A. | 肥皂水遇Ca2+、Mg2+ 含量较高的水有白色沉淀生成 | |
| B. | 水稻田使用NH4NO3的肥效较差 | |
| C. | 肾功能衰竭等疾病引起的血液中毒,要利用血液渗析进行治疗,渗析原理与胶体的渗析类似 | |
| D. | 在冶金厂和水泥厂常用高压电对气溶胶作用以除去大量烟尘,减小对空气的污染 |
2.某地污水中含有Zn2+、Hg2+、Fe3+和Cu2+四种阳离子.甲、乙、丙三位同学设计的从该污水中回收金属铜的方案如下:
已知:Zn2++2OH-═Zn(OH)2↓ Zn(OH)2+2OH-═ZnO${\;}_{2}^{2-}$+2H2O↓
甲:[污水]$→_{①}^{+过量NaOH溶液,过滤}$[沉淀]$→_{②}^{△}$[CuO]$→_{③}^{+H_{2},△}$[Cu]
乙:[污水]$→_{①}^{+过量铁粉,过滤}$[滤渣]$→_{②}^{△}$[CuO]$\stackrel{+H_{2},△}{→}$[Cu]
丙:[污水]$→_{①}^{+过量铁粉,过滤}$[滤渣]$→_{②}^{+稀盐酸,过滤}$[滤渣]$→_{③}^{△}$[CuO]$→_{④}^{+H_{2},△}$[Cu]
下列判断正确的是( )
已知:Zn2++2OH-═Zn(OH)2↓ Zn(OH)2+2OH-═ZnO${\;}_{2}^{2-}$+2H2O↓
甲:[污水]$→_{①}^{+过量NaOH溶液,过滤}$[沉淀]$→_{②}^{△}$[CuO]$→_{③}^{+H_{2},△}$[Cu]
乙:[污水]$→_{①}^{+过量铁粉,过滤}$[滤渣]$→_{②}^{△}$[CuO]$\stackrel{+H_{2},△}{→}$[Cu]
丙:[污水]$→_{①}^{+过量铁粉,过滤}$[滤渣]$→_{②}^{+稀盐酸,过滤}$[滤渣]$→_{③}^{△}$[CuO]$→_{④}^{+H_{2},△}$[Cu]
下列判断正确的是( )
| A. | 三种实验方案中都能制得纯净的铜 | |
| B. | 甲方案中的反应涉及置换、分解、复分解三种反应类型 | |
| C. | 乙方案中加过量铁粉只能还原其中的二种阳离子 | |
| D. | 丙方案不会产生环境污染 |
19.在甲酸的下列性质中,可以证明它是弱电解质的是( )
| A. | 在相同条件下,甲酸的导电性比强酸溶液的导电性弱 | |
| B. | 甲酸能与水以任意比互溶 | |
| C. | 10mL 1mol/L甲酸恰好跟10 mL 1mol/L NaOH溶液完全反应 | |
| D. | 1mol/L甲酸溶液中c(H+)约为1×10-2mol/L |
6.下列说法正确的是( )
| A. | 最外层有两个电子的原子都是金属原子 | |
| B. | 最外层有五个电子的原子都是非金属原子 | |
| C. | 非金属元素呈现的最高化合价不超过该元素原子的最外层电子 | |
| D. | 非金属元素呈现的最低化合价,其绝对值等于该元素原子的最外层电子数 |
16.某固体混合物可能由Al、(NH4)2SO4、MgCl2、FeCl2、AlCl3中的两种或多种组成,现对该混合物做如下实验,所得现象和有关数据如图所示(气体体积数据已换算成标准状况下的体积),关于该固体混合物,下列说法正确的是( )
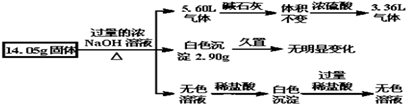

| A. | 一定含有Al,其物质的量为$\frac{5}{3}$mol | |
| B. | 一定不含FeCl2,可能含有MgCl2和AlCl3 | |
| C. | 一定含有(NH4)2SO4和FeCl2 | |
| D. | 一定含有(NH4)2SO4和MgCl2,且物质的量相等 |
3.为了检验某晶体中是否含有NH4+、SO42-、Fe2+和结晶水,设计了下列操作步骤:
①取少量该晶体于试管中,加热,发现试管口处有液体,且该液体能使无水硫酸铜变蓝;
②取少量该晶体的溶液于试管中,加入KSCN溶液,没有明显的变化,滴加几滴氯水,溶液显红色;
③取少量该晶体的溶液于试管中,再加入盐酸,没有明显的变化.再加入BaCl2溶液,有白色沉淀产生;
④取少量该晶体的溶液于试管中,加入浓NaOH溶液,微热有使湿润的红色石蕊试纸变蓝的气体产生,同时还有白色沉淀产生,该沉淀很快变成灰绿色沉淀最终变为红褐色沉淀.下列说法正确的是( )
①取少量该晶体于试管中,加热,发现试管口处有液体,且该液体能使无水硫酸铜变蓝;
②取少量该晶体的溶液于试管中,加入KSCN溶液,没有明显的变化,滴加几滴氯水,溶液显红色;
③取少量该晶体的溶液于试管中,再加入盐酸,没有明显的变化.再加入BaCl2溶液,有白色沉淀产生;
④取少量该晶体的溶液于试管中,加入浓NaOH溶液,微热有使湿润的红色石蕊试纸变蓝的气体产生,同时还有白色沉淀产生,该沉淀很快变成灰绿色沉淀最终变为红褐色沉淀.下列说法正确的是( )
| A. | 实验②中发生反应的离子方程式为:Fe2++Cl2═Fe3++2Cl-;Fe3++3SCN-═Fe(SCN)3 | |
| B. | 通过上述实验可确定该化合物的化学式为:(NH4)2Fe(SO4)2•6H2O | |
| C. | 只做实验①③④,也能达到实验目的 | |
| D. | 为了检验SO42-,可以将③中的试剂换为HNO3酸化的Ba(NO3)2 |
20.下列溶液中各微粒的浓度关系正确的是( )
| A. | c(NH4+)相等的NH4HCO3、NH4HSO4、NH4Cl三种溶液的物质的量浓度关系为c(NH4HSO4)>c(NH4HCO3)>c(NH4Cl) | |
| B. | 将10mL0.1mol•L-1Na2CO3溶液逐滴滴加到10mL0.1mol•L-1盐酸中:c(Na+)>c(Cl-)>c(HCO3-)>c(CO32-)>c(OH-) | |
| C. | 室温下,向100mL0.1mol/LNaOH溶液中滴加0.1mol/LNH4HSO4溶液至溶液呈中性,溶液中各离子浓度大小关系:c(Na+)>c(NH4+)>c(SO42-)>c(OH-)=c(H+) | |
| D. | 0.2mol•L-1的某一元弱酸HA溶液和0.1mol•L-1NaOH溶液等体积混合后的溶液:2c(OH-)+c(A-)═2c(H+)+c(HA) |
1.在如图装置中,若通电一段时间后乙装置左侧电极质量增加,则下列说法错误的是( )
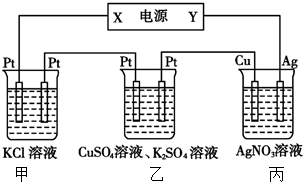

| A. | 当甲装置中共产生标准状况下4.48 L气体时,Cu电极上质量增加43.2g | |
| B. | 电解过程中装置丙的pH无变化 | |
| C. | 向甲中通人适量的HCl气体,可使溶液恢复到电解前的状态 | |
| D. | 乙中左侧电极反应式:Cu2++2e-=Cu |