题目内容
20.下列说法中正确的是( )| A. | NH4Cl中含有共价键,又全部由非金属元素组成,属于共价化合物 | |
| B. | 氮气和氦气都是非金属单质,都不存在化学键 | |
| C. | H2O2和Na2O2 都属于氧化物,两种物质中所含的化学键的类型完全相同 | |
| D. | KOH中既含有离子键也含有共价键,属于离子化合物 |
分析 一般来说,活泼金属与非金属形成离子键,非金属之间形成共价键,含离子键的一定为离子化合物,以此来解答.
解答 解:A.NH4Cl中含有共价键、铵根离子与氯离子之间的离子键,为离子化合物,故A错误;
B.氮气存在N≡N共价键,故B错误;
C.H2O2和Na2O2 都属于氧化物,H2O2中含共价键,Na2O2中含共价键和离子键,故C错误;
D.KOH中含离子键和O-H共价键,为离子化合物,故D正确;
故选D.
点评 本题考查化学键,为高考常见题型,侧重于学生的分析、应用能力的考查,把握化学键的形成及判断的一般规律为解答的关键,注意特殊物质中的化学键,题目难度不大.

练习册系列答案
相关题目
10.将0.2mol•L-1的CH3COONa溶液与0.1mol•L-1的HCl溶液等体积混合后,溶液中下列微粒的物质的量浓度的关系中,正确的是( )
| A. | C(CH3COO-)=C(Cl-)=C(H+)>C(CH3COOH) | B. | C(CH3COO-)=C(Cl-)>C(CH3COH)>C(H+) | ||
| C. | C(CH3COO-)>C(Cl-)>C(H+)>C(CH3COOH) | D. | C(CH3COO-)>C(Cl-)>C( CH3COOH)>C(H+) |
11.空气是人类生存所必需的重要资源.2015年2月28日,知名媒体人柴静向多家视频网站免费奉献了大型空气污染深度公益调查-《柴静雾霾调查:穹顶之下》,唤起了新一轮关注环保的热情.下列措施不利于环保的是( )
| A. | 推广使用燃煤脱硫技术,防治SO2污染 | |
| B. | 实施绿化工程,防治扬尘污染 | |
| C. | 研制开发燃料电池汽车,消除机动车尾气污染 | |
| D. | 加大石油、煤炭的开采速度,增加化石燃料的供应量 |
8.25℃时,在浓度为1mol•L-1的(NH4)2SO4、(NH4)2CO3、(NH4)2Fe(SO4)2的溶液中,测得c(NH4+)分别为a、b、c(单位为mol•L-1).下列判断正确的是( )
| A. | a=b=c | B. | a>b>c | C. | a>c>b | D. | c>a>b |
12.下列说法正确的是( )
| A. | 增加反应物的用量一定能增大反应速率 | |
| B. | 化学反应速率只能加快不能减慢 | |
| C. | 决定化学反应速率的主要因素是浓度 | |
| D. | 参加反应物质的性质是决定化学反应速率的主要因素 |
9. 将烧喊吸收H2S后的溶液加入到如图所示的电解池的阳极区进行电解,以实现H2S转化为S的目的.下列判断错误的是( )
将烧喊吸收H2S后的溶液加入到如图所示的电解池的阳极区进行电解,以实现H2S转化为S的目的.下列判断错误的是( )
 将烧喊吸收H2S后的溶液加入到如图所示的电解池的阳极区进行电解,以实现H2S转化为S的目的.下列判断错误的是( )
将烧喊吸收H2S后的溶液加入到如图所示的电解池的阳极区进行电解,以实现H2S转化为S的目的.下列判断错误的是( )| A. | 电解过程中阳极区发生如下反应:S2--2e-=S,(n-l)S+S2-=Sn2- | |
| B. | 电解时阴极的电极反应式:2H20+2e-═H2↑+20H- | |
| C. | 电解后阳极区的溶液用稀硫酸酸化得到硫单质,其离子方程式可写成Sn2-+2H+═nS↓+H2↑ | |
| D. | 该装置的离子交换膜为阳离子交换膜 |
10.下列化合物在一定条件下能发生取代、还原、加成、消去四种反应的是( )
| A. | CH3-CHCl-CHO | B. | CH3-CHBr-CHBr-CH3 | ||
| C. | CH3-C≡C-CHO | D. | 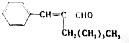 |
 .
. 已知相邻的短周期元素A、B、C、D原子核外共有56个电子,在周期表中的位置如图所示.请画出C原子和A离子的结构示意图:
已知相邻的短周期元素A、B、C、D原子核外共有56个电子,在周期表中的位置如图所示.请画出C原子和A离子的结构示意图: 、
、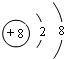 .
.