��Ŀ����
8��25��ʱ����Ũ��Ϊ1mol•L-1�ģ�NH4��2SO4����NH4��2CO3����NH4��2Fe��SO4��2����Һ�У����c��NH4+���ֱ�Ϊa��b��c����λΪmol•L-1���������ж���ȷ���ǣ�������| A�� | a=b=c | B�� | a��b��c | C�� | a��c��b | D�� | c��a��b |
���� ��NH4��2CO3��Һ�е�̼������Ӻ�笠�������ٽ�ˮ�⣬����笠�����Ũ�ȼ�С��
��NH4��2Fe��SO4��2��Һ�е���������ˮ����Һ��ʾ���ԣ�笠�����ˮ����Һ��ʾ���ԣ��������ӵ�ˮ��������笠�����ˮ�⣻
��NH4��2SO4��Һ笠���������ˮ�⣻
笠�����ˮ��̶�Խ����ͬ���ʵ���Ũ��c��NH4+������Һ�����ʵ�Ũ��Խ�ݴ˽��н��
��� �⣺��NH4��2SO4����NH4��2CO3����NH4��2Fe��SO4��2������Һ����NH4��2CO3��Һ��CO32-���Ӵٽ�NH4+ˮ�⣬��NH4��2Fe ��SO4��2��Һ��Fe2+����NH4+����ˮ�⣬
��ͬŨ�ȵģ�NH4��2SO4����NH4��2CO3����NH4��2Fe��SO4��2��Һ�У�笠�����Ũ�ȴ�СΪ����NH4��2Fe ��SO4��2����NH4��2SO4����NH4��2CO3��
�ʣ�NH4��2SO4����NH4��2CO3����NH4��2Fe��SO4��2��Һ��c��NH4+��Ũ�ȴ�С˳��Ϊ��c��a��b��
��ѡD��
���� ���⿼������Һ������Ũ�ȴ�С�Ƚϡ��ε�ˮ��ԭ������Ŀ�Ѷ��еȣ�ע�������ε�ˮ��ԭ������ȷ����֮��ˮ��̶ȵ�Ӱ������ǽⱾ��ؼ���

��ϰ��ϵ�д�
 �Ķ��쳵ϵ�д�
�Ķ��쳵ϵ�д�
�����Ŀ
18����ѧ��ȤС��Ϊ���о�����ijɷּ�����ȡ�õ�������Ʒ������pH�IJⶨ����ʱ�����ƣ��õ�������ʵ�����ݣ�
��1����ˮ��Ʒ����ʱ��pH�仯����Ҫԭ��Ϊ��2H2SO3+O2=2H2SO4���û�ѧ����ʽ��ʾ�����ɴ˿��Եó������γɹ��̿����ǣ��û�ѧ����ʽ��ʾ��SO2+H2O=H2SO3��
��2�����и�ѡ���������������ɵ�Σ�������в���ȷ����C��
A����ʴ��������ܵ� B����ȾˮԴ C�������������� D����ׯ��
��3���������¼��ִ�ʩ��
�ٶ�ȼ��úʱ������β�����г�������
������ԭú��ȼ�ϣ�
��ȼ��ʱ��������������
�ܿ��������Դ��
�����ܼ�����������Ĵ�ʩ��C��
A���٢ڢ�B���ڢۢ�C���٢ڢ�D���٢ۢ�
| ʱ�䣨h�� | ��ʼ | 8 | 16 | 24 | 32 | 40 | 48 |
| pH | 5.0 | 4.8 | 4.5 | 4.3 | 4.2 | 4.0 | 4.0 |
��2�����и�ѡ���������������ɵ�Σ�������в���ȷ����C��
A����ʴ��������ܵ� B����ȾˮԴ C�������������� D����ׯ��
��3���������¼��ִ�ʩ��
�ٶ�ȼ��úʱ������β�����г�������
������ԭú��ȼ�ϣ�
��ȼ��ʱ��������������
�ܿ��������Դ��
�����ܼ�����������Ĵ�ʩ��C��
A���٢ڢ�B���ڢۢ�C���٢ڢ�D���٢ۢ�
13����ͼװ����ʾ���Զ�����Ϊȼ���γɵ�ȼ�ϵ�أ������й�˵����ȷ���ǣ�������
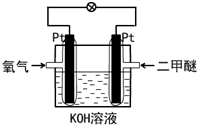

| A�� | ���������ұ�Pt�缫�����ߡ����Pt�缫 | |
| B�� | ͨ��������ߵ�Pt�缫Ϊ���� | |
| C�� | ��Һ��OH-���ұ�Pt�缫�ƶ� | |
| D�� | ͨ������ѵĵ缫��Ӧʽ��12OH-+CH3OCH3-12e-=2CO2+9H2O |
20������˵������ȷ���ǣ�������
| A�� | NH4Cl�к��й��ۼ�����ȫ���ɷǽ���Ԫ����ɣ����ڹ��ۻ����� | |
| B�� | �����ͺ������Ƿǽ������ʣ��������ڻ�ѧ�� | |
| C�� | H2O2��Na2O2 ��������������������������Ļ�ѧ����������ȫ��ͬ | |
| D�� | KOH�мȺ������Ӽ�Ҳ���й��ۼ����������ӻ����� |
17������ÿ���е��������ʶ����÷�Һ©�����з�����ǣ�������
| A�� | ����������ˮ���ƾ���ˮ�����Ӻ�ˮ | |
| B�� | ���������ˮ���屽��ˮ����������ˮ | |
| C�� | ���ͺ�ˮ����ȩ��ˮ��������Ҵ� | |
| D�� | �����ˮ���ױ���ˮ�������ˮ |
18�����ж��л���������У���ȷ���ǣ�������
| A�� | 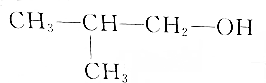 2-������ 2-������ | B�� | 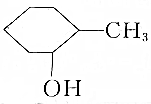 �ڼ����� �ڼ����� | ||
| C�� | CH3CH2OOCCH3 ������� | D�� | 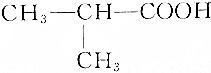 2-������ 2-������ |