题目内容
6.下列离子的电子层结构相同的一组是( )| A. | O2-、F-、Na+、Mg2+ | B. | Na+、Mg2+、S2-、Cl- | ||
| C. | F-、Cl-、Br-、I- | D. | Na+、Mg2+、K+、Ca2+ |
分析 电子层结构相同的离子中电子数相等,阴阳离子电子层结构相同时,说明阳离子元素位于阴离子元素下一周期,据此分析解答.
解答 解:A.O2-、F-在第二周期,Na+、Mg2+在第三周期,核外都是10个电子,都具有2层的电子结构,故A正确;
B.Na+、Mg2+在第三周期,核外有10个电子,电子层为2层,S2-、Cl-也在第三周期,核外有18个电子,电子层为3层,故B错误;
C.F-、Cl-、Br-、I-是同主族元素对应的离子,电子层依次增加,故C错误;
D.Na+、Mg2+在第三周期,核外有10个电子,电子层为2层,K+、Ca2+在第四周期,核外有18个电子,电子层为3层,故D错误;
故选A.
点评 本题考查了原子结构和元素性质,明确原子核外电子排布及原子结构即可解答,电子层结构相同的离子中电子数相等,题目难度不大.

练习册系列答案
 天天练口算系列答案
天天练口算系列答案
相关题目
4.下列化学式只表示一种纯净物的是( )
| A. | C4H8 | B. | C4H10 | C. | C5H12 | D. | C2H4 |
1.下列有关化学用语表示正确的是( )
| A. | 乙酸的结构简式:C2H4O2 | B. | MgCl2的电子式: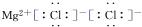 | ||
| C. | 中子数为8的碳原子:${\;}_{6}^{8}$C | D. | F-的结构示意图: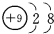 |
11.下列反应的离子方程式正确的是( )
| A. | 碳酸氢钙溶液跟稀硝酸反应:HCO3-+H+=H2O+CO2↑ | |
| B. | 饱和石灰水跟稀硝酸反应:Ca(OH)2+2H+=Ca2++2H2O | |
| C. | 钠与水反应:Na+H2O=Na++OH-+H2↑ | |
| D. | 稀硫酸滴在铜片上:Cu+2H+=Cu2++H2↑ |
18.下列对生产、生活中有关化学问题的分析中,正确的是( )
| A. | 镀锌铁制品,镀层破损后铁制品将彻底失去保护 | |
| B. | 由单质A转化为单质B时△H=+119 kJ•mol-1,可知单质B比单质A稳定 | |
| C. | 草木灰与铵态氮肥混合施用效果更好 | |
| D. | Na2CO3可做食用碱,NH4Cl溶液可去除铁锈 |
15.下列化学用语正确的是( )
| A. | HClO的电子式: | B. | 中子数为10的氧原子:${\;}_{8}^{18}$O | ||
| C. | 乙烯的结构简式 CH2CH2 | D. | CH4分子的球棍模型: |
16.下列各组粒子属于同位素的是( )
| A. | 35Cl和37Cl | B. | 40K和40Ca | C. | O2和O3 | D. | H2O和D2O |
 中填上所需的微粒。
中填上所需的微粒。