题目内容
11.下列反应的离子方程式正确的是( )| A. | 碳酸氢钙溶液跟稀硝酸反应:HCO3-+H+=H2O+CO2↑ | |
| B. | 饱和石灰水跟稀硝酸反应:Ca(OH)2+2H+=Ca2++2H2O | |
| C. | 钠与水反应:Na+H2O=Na++OH-+H2↑ | |
| D. | 稀硫酸滴在铜片上:Cu+2H+=Cu2++H2↑ |
分析 A.碳酸氢钙与稀硝酸反应生成硝酸钙、二氧化碳气体和水;
B.饱和石灰水中的氢氧化钙应该拆开,不能保留化学式;
C.2mol钠与水反应生成1mol氢气,该反应不满足电子守恒;
D.铜的活泼性较弱,稀硫酸不与铜反应.
解答 解:A.碳酸氢钙溶液跟稀硝酸反应生成硝酸钙、二氧化碳和水,反应的离子方程式为:HCO3-+H+=H2O+CO2↑,故A正确;
B.饱和石灰水跟稀硝酸反应中,氢氧化钙应该拆开,正确的离子方程式为:OH-+H+=H2O,故B错误;
C.钠与水反应生成氢氧化钠和氢气,正确的离子方程式为:2Na+2H2O=2Na++2OH-+H2↑,故C错误;
D.Cu的活泼性较弱,稀硫酸滴在铜片上,二者不发生反应,故D错误;
故选A.
点评 本题考查了离子方程式的正误判断,为高考的高频题,题目难度中等,注意掌握离子方程式正误判断常用方法:检查反应能否发生,检查反应物、生成物是否正确,检查各物质拆分是否正确,如难溶物、弱电解质等需要保留化学式,检查是否符合守恒关系(如:质量守恒和电荷守恒等)等;试题侧重基础知识的考查,有利于培养学生的灵活应用能力.

练习册系列答案
 优等生题库系列答案
优等生题库系列答案
相关题目
9.氢化铵(NH4H)与氯化铵的结构相似,又知NH4H与水反应有氢气放出,下列叙述不正确的是( )
| A. | NH4H是离子化合物,含有离子键和共价键 | |
| B. | NH4H与水反应时,NH4H是还原剂 | |
| C. | 每反应1molNH4H,转移2mol电子 | |
| D. | NH4H投入少量的水中,有两种气体产生 |
下列除杂方案错误的是
选项 | 被提纯的物质 | 杂质 | 除杂试剂 | 除杂方法 |
A | CO(g) | CO2(g) | NaOH溶液、浓H2SO4 | 洗气 |
B | NH4Cl(aq) | Fe3+(aq) | NaOH溶液 | 过滤 |
C | Cl2(g) | HCl(g) | 饱和食盐水、浓H2SO4 | 洗气 |
D | Na2CO3(s) | NaHCO3(s) | — | 灼烧 |
6.下列离子的电子层结构相同的一组是( )
| A. | O2-、F-、Na+、Mg2+ | B. | Na+、Mg2+、S2-、Cl- | ||
| C. | F-、Cl-、Br-、I- | D. | Na+、Mg2+、K+、Ca2+ |
16.科学家预言,燃料电池将是21 世纪获得电能的重要途径.近几年开发的甲醇燃料电池是采用铂作电极,电池中的质子交换膜只允许H+和水分子通过.其工作原理的示意图如下.下列说法错误的是( )
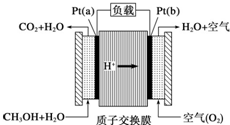

| A. | a 是负极,b 是正极 | |
| B. | b 极的电极反应是O2+4H++4e-=2H2O | |
| C. | 放电过程中,电子流动方向为:a→b→质子交换膜→a | |
| D. | 当电路上通过2 mol 电子消耗的CH3OH 为1/3mol |
3.ClO2是一种消毒杀菌剂,实验室可通过下列反应制得 ClO2:2KClO3+H2C2O4+H2SO4=2ClO2↑+K2SO4+2CO2↑+2H2O 下列说法正确的是( )
| A. | KClO3在反应中是还原剂 | |
| B. | ClO2是氧化产物 | |
| C. | H2C2O4在反应中被氧化 | |
| D. | 1molKClO3参加反应,有 2mol 电子转移 |
20.在一定温度下的定容容器中,当下列哪些物理量不再发生变化时,表明反应( )
A(s)+2B(g)?C(g)+D(g)已达到平衡状态的是
①混合气体的压强 ②混合气体的密度 ③B的物质的量浓度
④混合气体总物质的量 ⑤v(B)正与v(D)逆的比值为2:1 ⑥混合气体总质量.
A(s)+2B(g)?C(g)+D(g)已达到平衡状态的是
①混合气体的压强 ②混合气体的密度 ③B的物质的量浓度
④混合气体总物质的量 ⑤v(B)正与v(D)逆的比值为2:1 ⑥混合气体总质量.
| A. | ①③④⑤ | B. | ②③⑤⑥ | C. | ②③④⑤ | D. | ①②③⑥ |
1.下列物质属于强电解质的是( )
| A. | 碳酸钙 | B. | 盐酸 | C. | 酒精 | D. | 醋酸 |