题目内容
14.下列两种溶液混合后,所得溶液中各离子浓度关系不 正确的是( )| A. | 0.1 mol/L的NaOH溶液与0.1 mol/L的CH3COOH溶液等体积混合c(Na+)>c(OH-)>c(CH3COO-)>c(H+) | |
| B. | 常温下,0.01 mol/L的NaOH溶液与pH=2的CH3COOH溶液等体积混合c(CH3COO-)>c(Na+)>c(H+)>c(OH-) | |
| C. | 常温下,0.1 mol/L的CH3COOH溶液与0.1 mol/L的NaOH溶液混合后使pH=7,c(CH3COO-)═c(Na+)>c(H+)=c(OH-) | |
| D. | 0.1 mol/L的CH3COOH溶液和0.1 mol/L的CH3COONa溶液等体积混合c(CH3COO-)+c(OH-)═c(Na+)+c(H+) |
分析 A.反应后溶质为醋酸钠,由于水解程度较小,则c(CH3COO-)>c(OH-);
B.醋酸为弱酸,混合液中醋酸过量,混合液呈酸性,则c(H+)>c(OH-),结合电荷守恒判断溶液中各离子浓度大小;
C.pH=7,则c(H+)=c(OH-),结合电荷守恒可知c(CH3COO-)=c(Na+);
D.根据混合液中的核电荷数判断.
解答 解:A.0.1 mol/L的NaOH溶液与0.1 mol/L的CH3COOH溶液等体积混合,恰好反应生成醋酸钠,醋酸根离子部分水解,溶液层减小,则c(OH-)>c(H+),结合电荷守恒可知c(Na+)>c(CH3COO-),由于水解程度较小,则c(CH3COO-)>c(OH-),溶液中离子浓度大小为:c(Na+)>c(CH3COO-)>c(OH-)>c(H+),故A错误;
B.常温下,0.01 mol/L的NaOH溶液与pH=2的CH3COOH溶液等体积混合,由于醋酸为弱酸,则pH=2的醋酸中醋酸的浓度大于0.01mol/L,所以混合液中醋酸过量,混合液学生酸性,则c(H+)>c(OH-),结合电荷守恒可知c(CH3COO-)>c(Na+),溶液中离子浓度大小为:c(CH3COO-)>c(Na+)>c(H+)>c(OH-),故B正确;
C.常温下,0.1 mol/L的CH3COOH溶液与0.1 mol/L的NaOH溶液混合后使pH=7,则c(H+)=c(OH-),结合电荷守恒可知:c(CH3COO-)=c(Na+),溶液中离子浓度大小为:c(CH3COO-)=c(Na+)>c(H+)=c(OH-),故C正确;
D.0.1mol/L的CH3COOH溶液和0.1 mol/L的CH3COONa溶液等体积混合,溶液中一定满足电荷守恒:c(CH3COO-)+c(OH-)=c(Na+)+c(H+),故D正确;
故选A.
点评 本题考查了离子浓度大小比较,题目难度中等,明确盐的水解原理、弱电解质的电离平衡及其影响为解答关键,注意掌握电荷守恒、物料守恒的含义及在判断离子浓度大小中的应用方法,试题培养了学生的分析能力及灵活应用能力.

 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案| A. | 灯光变暗;二者电离常数相同 | B. | 灯光变暗;电离常数醋酸大于氨水 | ||
| C. | 灯光变亮;电离常数醋酸小于氨水 | D. | 灯光变亮;电离常数醋酸等于氨水 |
| A. | NiOOH | B. | Ni(OH)2 | C. | Cd | D. | Cd(OH)2 |
| A. | 1 L 1mol/L NaHCO3溶液中自由移动的离子总数为3NA | |
| B. | 常温常压下,1.06g Na2CO3含有Na+数目为0.02NA | |
| C. | 1 mol Na2O2与CO2反应电子转移为2 NA | |
| D. | 40g NaOH溶解在1 L水中,得到溶液的物质的量浓度为1 mol/L |
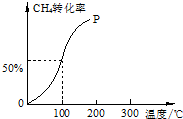 以CH4和H2O为原料,通过下列反应来制备甲醇.
以CH4和H2O为原料,通过下列反应来制备甲醇.