题目内容
图表法、图象法是常用的科学研究方法.
(1)图(A)是短周期某主族元素X的电离能所示情况.则X元素位于周期表的第 族.
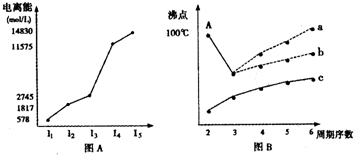
(2)图B是研究部分元素的氢化物的沸点变化规律的图象,折线c可以表达出第 族元素氢化物的沸点的变化规律.
(1)图(A)是短周期某主族元素X的电离能所示情况.则X元素位于周期表的第

(2)图B是研究部分元素的氢化物的沸点变化规律的图象,折线c可以表达出第
考点:元素电离能、电负性的含义及应用
专题:元素周期律与元素周期表专题
分析:(1)因第三和第四电离能之间发生突变,所以该元素最外层有3个电子,在ⅢA族;
(2)线c逐渐上升,表明没有氢键的影响,是第ⅣA族元素氢化物的沸点变化规律.
(2)线c逐渐上升,表明没有氢键的影响,是第ⅣA族元素氢化物的沸点变化规律.
解答:
解:(1)因第三和第四电离能之间发生突变,所以该元素最外层有3个电子,处于ⅢA族,故答案为:ⅢA;
(2)线c逐渐上升,表明没有氢键的影响,第ⅣA族元素氢化物之间不能形成氢键,所以符合第ⅣA族元素氢化物的沸点变化规律,故答案为:ⅣA.
(2)线c逐渐上升,表明没有氢键的影响,第ⅣA族元素氢化物之间不能形成氢键,所以符合第ⅣA族元素氢化物的沸点变化规律,故答案为:ⅣA.
点评:本题考查元素周期律、分子结构与性质,涉及电离能与氢键对物质性质的影响等,难度不大,注意理解电离能与化合价关系.

练习册系列答案
 七星图书口算速算天天练系列答案
七星图书口算速算天天练系列答案 初中学业考试导与练系列答案
初中学业考试导与练系列答案
相关题目
下列关于金属腐蚀的叙述正确的是( )
A、本质是:M+nH2O=M(OH)n+
| ||
| B、电化学腐蚀必须在酸性条件下进行 | ||
| C、化学腐蚀比电化学腐蚀更普遍 | ||
| D、本质是:M-ne-=Mn+ |
短周期的两种元素A和B,它们的离子A-和B2+具有相同的电子层结构,下列说法中正确的是( )
| A、原子序数A>B |
| B、电子总数A>B |
| C、离子半径A->B2+ |
| D、原子半径A>B |
关于HCl、H2SO4、HNO3三大强酸的说法正确的是( )
| A、都是含氧酸 |
| B、都属于强电解质 |
| C、都容易挥发 |
| D、都能与金属Mg发生置换反应 |
1gN2含a个分子,则阿伏加德罗常数的数值可表示为( )
A、
| ||
| B、a | ||
| C、28a | ||
D、
|