题目内容
9.某有机物在氧气里充分燃烧,生成的CO2和H2O的物质的量之比为1:1,由此可以得出该有机物( )| A. | 分子中C、H、O的个数之比为1:2:3 | B. | 分子中肯定不含氧原子 | ||
| C. | 分子中C和H的个数之比为1:2 | D. | 分子中可能含有氧原子 |
分析 某有机物在氧气里充分燃烧,生成的CO2和H2O的物质的量之比为1:1,说明有机物分子中C、H原子数目之比为1:2,该有机物可能为烃,也可能为烃的含氧衍生物.
解答 解:某有机物在氧气里充分燃烧,生成的CO2和H2O的物质的量之比为1:1,说明有机物分子中C、H原子数目之比为1:2,该有机物可能为烃,也可能为烃的含氧衍生物,不能确定是否含有元素,故AB错误,CD正确,故选CD.
点评 本题考查有机物分子式确定,利用原子守恒确定有机物分子中C、H原子个数之比,理解掌握燃烧法确定有机物分子式方法.

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目
17.化学教材中,常借助示意图表达实验装置的要点、阐述化学过程的原理等.下列有关示意图表现的内容一定不正确的是( )
| A. | 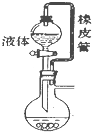 橡皮管能使液体顺利流下 | B. | 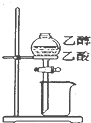 分离乙醇和乙酸 | ||
| C. | 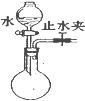 检查装置气密性 | D. | 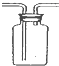 收集氨气 |
4.实验是研究化学的基础,下图中所示的实验方法、装置或操作完全正确的是( )
| A. | 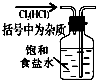 除杂 | B. | 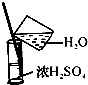 稀释 | ||
| C. |  制气 | D. | 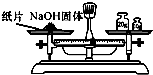 称量 |
14.下列物质既能与金属钠反应放出气体,又能与纯碱作用放出气体的是( )
| A. | CH3CH2OH | B. | H2O | C. | C6H12O6 | D. | CH3COOH |
1.(1)常温下,浓度均为0.1mol•L-1的下列五种钠盐溶液的pH如表
上述盐溶液中的阴离子,结合H+能力最强的是CO32-,根据表中数据,浓度均为0.01mol•L-1的下列四种酸的溶液分别稀释100倍,pH变化最大的是C(填编号).
A.HCN B.HClO C.CH3COOH D.H2CO3
(2)碳酸氢钠是一种强(填“强”或“弱”)电解质,写出HCO3-水解的离子方程式:HCO3-+H2O?H2CO3+OH-,常温下,0.1mol•L-1NaHCO3溶液的pH大于8,则溶液中Na+、HCO3-、H2CO3、CO32-、OH- 五种微粒的浓度由大到小的顺序为:c(Na+)>c(HCO3-)>c(OH-)>c(H2CO3)>c(CO32-).
(3)实验室中常用NaOH来进行洗气和提纯.
几种离子开始沉淀时的pH如下表:
当向含相同浓度Cu2+、Mg2+、Fe2+离子的溶液中滴加NaOH溶液时,Cu2+;(填离子符号)先沉淀,要使0.2mol/L硫酸铜溶液中Cu2+沉淀较为完全(使Cu2+浓度降至原来的千分之一),则应向溶液里加入氢氧化钠溶液使溶液pH为6.(KspCu(OH)2=2×10-20mol2•L-2)
(4)难溶电解质FeS在水溶液中存在着溶解平衡:FeS(s)?Fe2+(aq)+S2-(aq),在一定温度Ksp=c(Fe2+)c(S2-)=6.25×10-18,在该温度下,氢硫酸饱和溶液中存在c2(H+)c(S2-)=1.0×10-22.将适量FeCl2投入氢硫酸饱和溶液中,欲使溶液中c(Fe2+)=1.0mol/L,应调节溶液的pH=2.4(已知lg2=0.3)
| 溶质 | CH3COONa | NaHCO3 | Na2CO3 | NaClO | NaCN |
| pH | 8.8 | 9.7 | 11.6 | 10.3 | 11.1 |
A.HCN B.HClO C.CH3COOH D.H2CO3
(2)碳酸氢钠是一种强(填“强”或“弱”)电解质,写出HCO3-水解的离子方程式:HCO3-+H2O?H2CO3+OH-,常温下,0.1mol•L-1NaHCO3溶液的pH大于8,则溶液中Na+、HCO3-、H2CO3、CO32-、OH- 五种微粒的浓度由大到小的顺序为:c(Na+)>c(HCO3-)>c(OH-)>c(H2CO3)>c(CO32-).
(3)实验室中常用NaOH来进行洗气和提纯.
几种离子开始沉淀时的pH如下表:
| 离子 | Fe2+ | Cu2+ | Mg2+ |
| pH | 7.6 | 5.2 | 10.4 |
(4)难溶电解质FeS在水溶液中存在着溶解平衡:FeS(s)?Fe2+(aq)+S2-(aq),在一定温度Ksp=c(Fe2+)c(S2-)=6.25×10-18,在该温度下,氢硫酸饱和溶液中存在c2(H+)c(S2-)=1.0×10-22.将适量FeCl2投入氢硫酸饱和溶液中,欲使溶液中c(Fe2+)=1.0mol/L,应调节溶液的pH=2.4(已知lg2=0.3)
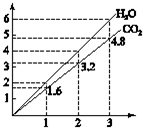 两种气态烃组成的混合气体,完全燃烧后得到CO2和H2O的物质的量随着混合烃物质的量的变化如图所示,则下列对混合烃的判断正确的是( )
两种气态烃组成的混合气体,完全燃烧后得到CO2和H2O的物质的量随着混合烃物质的量的变化如图所示,则下列对混合烃的判断正确的是( )