题目内容
19. 两种气态烃组成的混合气体,完全燃烧后得到CO2和H2O的物质的量随着混合烃物质的量的变化如图所示,则下列对混合烃的判断正确的是( )
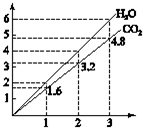
两种气态烃组成的混合气体,完全燃烧后得到CO2和H2O的物质的量随着混合烃物质的量的变化如图所示,则下列对混合烃的判断正确的是( )①可能有C2H4 ②一定没有C2H6 ③一定有C3H8
④一定有CH4 ⑤可能有C2H6 ⑥可能有C2H2.
| A. | ②⑤⑥ | B. | ④⑥ | C. | ①②④ | D. | ②③ |
分析 由图可知两种气态烃的平均组成为C1.6H4,根据碳原子平均数可知,混合气体一定含有CH4,由氢原子平均数可知,另一气态烃中氢原子数目为4,碳原子数目大于1.6,一般不超过4,据此判断.
解答 解:由图可知两种气态烃的平均组成为C1.6H4,根据碳原子平均数可知,混合气体一定含有CH4,由氢原子平均数可知,另一气态烃中氢原子数目为4,碳原子数目大于1.6,一般不超过4,故一定没有C2H2、C3H8、C2H6可能有C2H4,
故选C.
点评 本题考查烃混合物分子式确定,难度较大,注意利用平均分子组成判断烃的组成,常用方法有:1、平均碳法 2、平均氢法 3、平均碳氢分子式法 4、平均式量法.

练习册系列答案
相关题目
9.某有机物在氧气里充分燃烧,生成的CO2和H2O的物质的量之比为1:1,由此可以得出该有机物( )
| A. | 分子中C、H、O的个数之比为1:2:3 | B. | 分子中肯定不含氧原子 | ||
| C. | 分子中C和H的个数之比为1:2 | D. | 分子中可能含有氧原子 |
10.用NA表示阿伏加德罗常数的值.下列判断正确的是( )
| A. | 标准状况下,22.4 L苯中含有的分子数目为NA | |
| B. | 常温常压下,28g乙烯中含有碳碳双键数目为NA | |
| C. | 0.5mol•L-1K2SO4溶液中含有K+数目为NA | |
| D. | 28g铁与足量氯气反应失去的电子数目为NA |
14.已知X、Y、Z均为短周期元素,它们之间可形成X2Z和YZ2两种化合物,X、Y、Z的原子序数依次增大,X原子K层的电子数只有一个,Y位于X的下一周期,它的最外层电子数比K层多2个,而Z原子核外的最外层电子数比次外层少2个,请回答下列问题;
(1)它们的元素符号分别为:XH,YC,ZS.
(2)用价层电子对互斥理论判断:
(3)N2O双称笑气,N2O与YZ2具有相似的分子结构,请分析原因:二者互为等电子体.
(1)它们的元素符号分别为:XH,YC,ZS.
(2)用价层电子对互斥理论判断:
| 物质 | 分子的价层电子对数 | 中心原子的杂化轨道类型 | 分子的立体构型名称 |
| X2Z | V形 | ||
| YZ2 |
4.下列有关Al2(SO4)3溶液的叙述正确的是( )
| A. | 该溶液中Na+、NH4+、CO32-、Cl-可以大量共存 | |
| B. | 通入CO2气体产生白色沉淀 | |
| C. | 与Na2S反应的离子方程式:Al3++S2-→Al2S3↓ | |
| D. | 与过量浓氨水反应的离子方程式:Al3++3NH3+3H2O→Al(OH)3↓+3NH4+ |
11.有四种试剂:①AgNO3 ②HNO3 ③新制Cu(OH)2 ④碘水.为依次鉴别葡萄糖溶液、淀粉溶液、食盐溶液、鸡蛋清溶液,加入上述试剂的正确顺序是( )
| A. | ④②①③ | B. | ①③②④ | C. | ③②④① | D. | ③④①② |
8.下列有关实验现象或叙述中,不正确的是( )
| A. | 氢气在Cl2中燃烧,发出苍白色火焰 | |
| B. | 铵盐与碱共热产生气体能使干燥的红色石蕊试纸变蓝 | |
| C. | 实验室制氯气用饱和食盐水除去氯化氢 | |
| D. | 铜丝在Cl2中燃烧,生成棕黄色烟 |
9.下列实验操作能达到实验目的是( )
| 实验操作 | 实验目的 | |
| A | 苯和溴水混合后加入铁粉 | 制溴苯 |
| B | 向工业酒精中加入无水硫酸铜 | 确定工业酒精中是否含有水 |
| C | 电石与水反应,制得的气体直接通入酸性KMnO4溶液 | 检验制得的气体是否为乙炔 |
| D | 将氯乙烷与NaOH溶液共热后冷却,再滴入AgNO3溶液 | 检验氯乙烷中的氯原子 |
| A. | A | B. | B | C. | C | D. | D |
 .
.