题目内容
周期不同的短周期元素X、Y组成的化合物A,是良好的耐热冲击材料.已知A的化学式为XY,且X的阳离子和Y的阴离子具有相同的核外电子排布.
(1)X的单质既可与盐酸反应,又可与NaOH溶液反应,X的离子结构示意图为 .
(2)X的硫酸盐溶液与过量NaOH溶液反应的离子方程式为 .
(3)一定条件下,A和水缓慢作用生成含Y的化合物Z,Z分子含有10个电子.
①Z与H2O2反应,其产物之一是Y的单质,Y的单质的结构式为 ;
②A的化学式是 .
(4)X的单质、石墨和二氧化钛(TiO2)按比例混合,高温下反应得到的化合物均由两种元素组成,且都是新型陶瓷材料(在火箭和导弹上有重要应用),其反应的化学方程式是 .
(1)X的单质既可与盐酸反应,又可与NaOH溶液反应,X的离子结构示意图为
(2)X的硫酸盐溶液与过量NaOH溶液反应的离子方程式为
(3)一定条件下,A和水缓慢作用生成含Y的化合物Z,Z分子含有10个电子.
①Z与H2O2反应,其产物之一是Y的单质,Y的单质的结构式为
②A的化学式是
(4)X的单质、石墨和二氧化钛(TiO2)按比例混合,高温下反应得到的化合物均由两种元素组成,且都是新型陶瓷材料(在火箭和导弹上有重要应用),其反应的化学方程式是
考点:位置结构性质的相互关系应用
专题:元素周期律与元素周期表专题
分析:(1)单质既可与盐酸反应,又可与NaOH溶液反应判断为两性元素Al;
(2)硫酸铝溶液与过量NaOH溶液生成偏铝酸盐;
(3)元素X、Y不同周期,都属于短周期元素,X的阳离子和Y的阴离子具有相同的核外电子排布,则Y在第二周期,A的化学式为XY,一定条件下,A和水缓慢作用生成含Y的气体化合物Z,Z分子含有10个电子,则Y为N,Z为NH3;
(4)根据元素守恒和电子得失守恒写出化学方程式.
(2)硫酸铝溶液与过量NaOH溶液生成偏铝酸盐;
(3)元素X、Y不同周期,都属于短周期元素,X的阳离子和Y的阴离子具有相同的核外电子排布,则Y在第二周期,A的化学式为XY,一定条件下,A和水缓慢作用生成含Y的气体化合物Z,Z分子含有10个电子,则Y为N,Z为NH3;
(4)根据元素守恒和电子得失守恒写出化学方程式.
解答:
解:(1)X的单质既可与盐酸反应,又可与NaOH溶液反应,X为Al元素,X的原子结构示意图为 ,
,
故答案为: ;
;
(2)铝盐与过量NaOH溶液反应转化为偏铝酸盐,发生的离子反应方程式为:Al3++4OH-═AlO2-+2H2O,
故答案为:Al3++4OH-═AlO2-+2H2O;
(3)元素X、Y不同周期,都属于短周期元素,X的阳离子和Y的阴离子具有相同的核外电子排布,则Y在第二周期,A的化学式为XY,一定条件下,A和水缓慢作用生成含Y的气体化合物Z,Z分子含有10个电子,则Y为N,Z为NH3,
①Y单质为N2,结构式为N三N,
故答案为:N三N;
②X为Al,Y为N,A由短周期元素X、Y组成,则A为AlN,
故答案为:AlN;
(4)X的单质为Al、石墨和二氧化钛(TiO2)按比例混合,高温下反应得到的化合物均由两种元素组成,且都是新型陶瓷材料(在火箭河导弹上有重要应用)耐高温材料,生成产物为氧化铝,推断另一种只有碳化钛;依据原子守恒写出化学方程式,反应的化学方程式是:4Al+3TiO2+3C
2Al2O3+3TiC,
故答案为:4Al+3TiO2+3C
2Al2O3+3TiC.
 ,
,故答案为:
 ;
;(2)铝盐与过量NaOH溶液反应转化为偏铝酸盐,发生的离子反应方程式为:Al3++4OH-═AlO2-+2H2O,
故答案为:Al3++4OH-═AlO2-+2H2O;
(3)元素X、Y不同周期,都属于短周期元素,X的阳离子和Y的阴离子具有相同的核外电子排布,则Y在第二周期,A的化学式为XY,一定条件下,A和水缓慢作用生成含Y的气体化合物Z,Z分子含有10个电子,则Y为N,Z为NH3,
①Y单质为N2,结构式为N三N,
故答案为:N三N;
②X为Al,Y为N,A由短周期元素X、Y组成,则A为AlN,
故答案为:AlN;
(4)X的单质为Al、石墨和二氧化钛(TiO2)按比例混合,高温下反应得到的化合物均由两种元素组成,且都是新型陶瓷材料(在火箭河导弹上有重要应用)耐高温材料,生成产物为氧化铝,推断另一种只有碳化钛;依据原子守恒写出化学方程式,反应的化学方程式是:4Al+3TiO2+3C
| ||
故答案为:4Al+3TiO2+3C
| ||
点评:本题考查位置、结构、性质关系的应用,熟悉Al的性质、氧化还原反应、10电子微粒是解答本题的关键,难度不大,N元素的推断是解答本题的难点和易错点.

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目
3NO2十H2O═2HNO3十NO为工业上氨催化氧化法制硝酸的反应之一,该反应中NO2的作用是( )
| A、只作氧化剂 |
| B、作催化剂 |
| C、既作氧化剂又作还原剂 |
| D、作干燥剂 |
下列关于物质的量浓度表述正确的是( )
| A、0.2 mol?L-1 Na2SO4溶液中含有SO42-物质的量为0.2 mol |
| B、50mL 2 mol?L-1 NaCl溶液和100mL 0.5mol?L-1MgCl2溶液中,Cl-的物质的量浓度相等 |
| C、用1 L水吸收22.4 L氯化氢(标况下)所得盐酸的浓度是1 mol?L-1 |
| D、10 g 98%的硫酸(密度为1.84g?cm-3)与10mL 18.4mol?L-1的硫酸的浓度是相同的 |
下列说法正确的是( )
| A、硫酸、纯碱、碳酸钠和生石灰分别属于酸、碱、盐和氧化物 |
| B、生石灰与水混合的过程只发生物理变化 |
| C、可用丁达尔效应区分溶液与胶体 |
| D、CuSO4?5H2O是一种混合物 |
在标准状况下,将X气体VL溶于水中,得到2mol/L的溶液500mL,则气体的体积V为( )
| A、44.8L |
| B、22.4L |
| C、11.2L |
| D、33.6L |
如图为元素周期表的一部分.X、Y、Z、W均为短周期元素,若W原子的最外层电子数是其次外层电子数的
.则下列说法中正确的是( )
| 7 |
| 8 |
| X | Y | |
| Z | W |
| A、Y单质可与Z的氢化物的水溶液反应,使溶液pH升高 |
| B、含氧酸的酸性:W>Z |
| C、原子半径由大到小的排列顺序是Z>Y>X |
| D、X的单质中有一种为白色蜡状固体 |
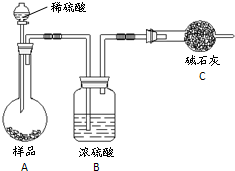
 锌与不同浓度的硫酸反应时,硫酸可以被还原为SO2,也可被还原为氢气.为了验证这一事实,某同学拟用如图装置进行实验(实验时压强为101kPa,温度为0℃):
锌与不同浓度的硫酸反应时,硫酸可以被还原为SO2,也可被还原为氢气.为了验证这一事实,某同学拟用如图装置进行实验(实验时压强为101kPa,温度为0℃):