题目内容
11.将浓硫酸在下列变化中的性质用编号填在横线上.A.酸性 B.难挥发性 C.吸水性 D.脱水性 E.强氧化性 F.催化剂
(1)浓硫酸作气体干燥剂C
(2)蔗糖中滴入浓硫酸变黑D
(3)用铝槽车装运浓硫酸E
(4)热的浓硫酸溶解CuA、E.
分析 浓硫酸具有吸水性,可用作干燥剂,具有脱水性,可使纸脱水碳化,具有强氧化性,可使铝、铁在常温下钝化,以此解答该题.
解答 解:(1)浓硫酸具有吸水性,作气体干燥剂,故答案为:C;
(2)蔗糖中滴入浓硫酸变黑,体现浓硫酸的脱水性,故答案为:D;
(3)冷浓H2SO4中放入铝片没有明显现象,金属产生钝化现象,在铝表面生成一层致密的氧化物薄膜,阻止了进一步反应,可铝槽车装运浓硫酸体现浓硫酸的强氧化性,故答案为:E;
(4)浓硫酸和铜在加热条件下反应,体现浓硫酸的酸性和强氧化性,故答案为:A、E.
点评 本题综合考查浓硫酸的性质,为高考常见题型和高频考点,注意浓硫酸的特性,学习中注意相关基础知识的积累,题目难度不大.

练习册系列答案
相关题目
1.下列表示物质结构的化学用语正确的是( )
| A. | Cl-离子的结构示意图: | B. | HF的电子式: | ||
| C. | 8个中子的碳原子的核素符号:12C | D. | CO2的结构式:O=C=O |
2.下列关于电解质的说法,正确的是( )
| A. | 氯气不导电,属于非电解质 | |
| B. | 乙酸是有机物,属于非电解质 | |
| C. | 在水溶液和熔融状态下都能够导电的物质才属于电解质 | |
| D. | KCl和Al2O3在熔融状态下均导电,都属于电解质 |
19.下列仪器使用正确的是( )
| A. | 在表面皿蒸发浓缩NaCl溶液 | |
| B. | 用带玻璃塞的试剂瓶盛盐酸 | |
| C. | 使用漏斗、滤纸、玻璃棒等进行过滤实验 | |
| D. | 坩埚、试管是能用酒精灯直接加热的仪器 |
6.下列各组溶液中H+ 浓度最大的是( )
| A. | 0.15 mol/L的盐酸 | B. | 0.10mol/L的硫酸 | ||
| C. | 0.15 mol/L的醋酸 | D. | 0.10mol/L的氢硫酸 |
16.Al、Fe、Cu都是重要的金属元素,下列说法正确的是( )
| A. | 三者对应的氧化物均为碱性氧化物 | |
| B. | 三者的单质放置在空气中均只生成氧化物 | |
| C. | 常温下三者加入浓硫酸中均无明显现 | |
| D. | Fe2O3与Fe3O4互为同素异形体 |
3.有机物 A 的结构简式如图,下列有关 A 的性质叙述中,错误的是( )


| A. | A 与金属钠完全反应时,两者物质的量之比为 1:3 | |
| B. | A 与氢氧化钠完全反应时,两者物质的量之比为 1:1 | |
| C. | A 能与碳酸钠溶液反应 | |
| D. | A 既能与羧酸反应,又能与醇反应 |
20.下列反应过程中的能量变化与右图一致的是( )
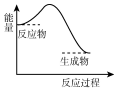

| A. | CaCO3$\frac{\underline{\;高温\;}}{\;}$CaO+CO2↑ | |
| B. | 2Al+Fe2O3$\frac{\underline{\;高温\;}}{\;}$2Fe+Al2O3 | |
| C. | Ba(OH)2•8H2O+2NH4Cl$\frac{\underline{\;研磨\;}}{\;}$BaCl2+2NH3↑+10H2O | |
| D. | 2H2O$\frac{\underline{\;电解\;}}{\;}$2H2↑+O2↑ |
14.能正确表示下列反应的离子方程式是( )
| A. | 将SO2通入Fe3+溶液中:2Fe3++SO2+2H2O═2Fe2++SO42-+4H+ | |
| B. | NaClO溶液与FeCl2溶液混合:Fe2++2ClO-+2H2O═Fe(OH)2↓+2HClO | |
| C. | 将氯化亚铁溶液和稀硝酸混合:Fe2++4H++NO3-═Fe3++2H2O+NO↑ | |
| D. | 将磁性氧化铁溶于盐酸:Fe3O4+8H+═3Fe3++4H2O |