��Ŀ����
18��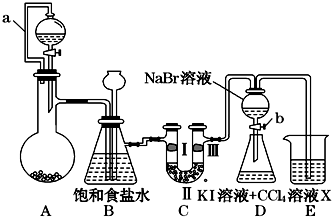 ijͬѧ�����ͼ��ʾ��ʵ�鷽����
ijͬѧ�����ͼ��ʾ��ʵ�鷽������1��Aװ�õķ�Һ©����ʢװŨ���ᣬ��ƿ�����Ϊ�ظ���أ�K2Cr2O7������ԭ������CrCl3��д��A�����ӷ���ʽ��Cr2O72-+14H++6Cl-�T2Cr3++3Cl2��+7H2O��
��2����ʵ��Ŀ�����Ʊ�������̽�����������ʵ�������ʣ�Bװ���м������ã��ֱ��dz�ȥ�����е��Ȼ��⡢��ȫƿ�����ʵ�������װ���Ƿ��������ȥa���ܵĺ�����������˳��������ƿ��
��3��װ��C�Ĺ�����̽���������Ե������Ƿ�һ����Ư���ԣ���������Լ�����Ǣڣ�
| �� | �� | �� | �� | |
| �� | ʪ��ĺ�ֽ�� | ����ĺ�ֽ�� | ����ĺ�ֽ�� | ʪ��ĺ�ֽ�� |
| �� | ��ʯ�� | Ũ���� | �轺 | �Ȼ��� |
| �� | ʪ��ĺ�ֽ�� | ����ĺ�ֽ�� | ����İ�ֽ�� | ����ĺ�ֽ�� |
��5��Dװ�ý���ʵ��ʱ�������Բ��㣬����û���ų��������嵥����KI��Ӧ�ĸ��ţ����ʵ���ҺX�Ǣ٢ܢ� ���Ӣ�����������Һ������������Һ��������������Һ���Ȼ�������Һ�����⻯����Һ��̼��������Һ��ѡ��
���� ��1�����������֪�ظ�����ܹ�����Ũ����������������������ԭΪCrCl3��������Ӧ��Ԫ�ػ��ϼ۱仯������������ԭ��Ӧ��ʧ�����غ㡢ԭ�Ӹ����غ������д����ʽ��
��2��ʵ��Ŀ��Ϊ���Ʊ�������̽�����������ʵ�������ʣ�Ũ�����ӷ���B��������ã���B�Ľṹ����B������ȫƿ��a�������ӷ�Һ©����Բ����ƿ������Һ��˳�����£�����a����Ũ�����˳��������ƿ��
��3����֤�����Ƿ����Ư���ԣ�Ҫ��֤����������Ư���ԣ�ʪ�����ɫ�����У�������ˮ��Ӧ���ɴ��������Ư���ԣ�
��4�����Dװ�÷�Һ©���ڷ�Ӧ���ɵ����ܹ��û����⻯����Һ�еĵ����ӣ�����֤����ķǽ����Աȵ��ǿ��������Ȼ�̼��Һ���Ϻ�ɫ��
��5������������ǿ�ڵ����ӣ��ܹ��û��ⵥ�ʣ������ж���������������Eװ�����գ�����xӦΪ�ܹ���������Ӧ�����������µ���Ⱦ�����Һ�壮
��� �⣺��1�����������֪�ظ�����ܹ�����Ũ����������������������ԭΪCrCl3����Ӧ�и�Ԫ�ػ��ϼ۱仯Ϊ��+7��+3����������Ԫ�ػ��ϼ۱仯��-1��0��Ҫʹ��ʧ�����غ㣬�ظ����ϵ��Ϊ1������ϵ��Ϊ6������ԭ�Ӹ����غ㣬��Ӧ����ʽ��K2Cr2O7+14HCl=2CrCl3+3Cl2��+2KCl+7H2O�����ӷ���ʽ��Cr2O72-+14H++6Cl-�T2Cr3++3Cl2��+7H2O��
�ʴ�Ϊ��Cr2O72-+14H++6Cl-�T2Cr3++3Cl2��+7H2O��
��2 ��ʵ��Ŀ��Ϊ���Ʊ�������̽�����������ʵ�������ʣ�Ũ�����ӷ���B��������ã���B�Ľṹ����B������ȫƿ��a�������ӷ�Һ©����Բ����ƿ������Һ��˳�����£�
�ʴ�Ϊ���Ʊ�������̽�����������ʵ�������ʣ� ����ȫƿ�����ʵ�������װ���Ƿ������Ũ�����˳��������ƿ��
��3��װ��C��ʵ��Ŀ������֤�����Ƿ����Ư���ԣ���֤�����Ƿ����Ư���ԣ�Ҫ��֤����������Ư���ԣ�ʪ�����ɫ�����У�������ˮ��Ӧ���ɴ��������Ư���ԣ��Լ���Ϣٲ���֤�������������Ư���ԣ��Լ���Ϣۢ����õ��Ǹ���İ�ɫֽ��������֤������������Ư���ԣ��Լ���Ϣ��Ȼ��Ʋ��Ǹ�������������������е�ˮ������������֤�������������Ư���ԣ��Լ���Ϣڴ�B �г�����ʪ��������ܹ�ʹ���и���ĺ�ֽ����ɫ��֤��ʪ���������Ư���ԣ�����Ũ��������Ϊ�����������ͨ����ʱ������ĺ�ֽ������ɫ����֤�������������Ư���ԣ�
�ʴ�Ϊ���ڣ�
��4������⻯�ط�Ӧ�����ӷ���ʽΪ��2I-+Br2=I2+2Br-������������Ϊ��ʵ����ϣ�������ʹ����Һ��������ƿ���رջ���������ƿ���²�Һ����Ϻ�ɫ��
�ʴ�Ϊ��ʵ����ϣ�������ʹ����Һ��������ƿ���رջ���������ƿ���²�Һ����Ϻ�ɫ����5������������ǿ�ڵ����ӣ��ܹ��û��ⵥ�ʣ�����Dװ�ý���ʵ��ʱû���ų��������嵥����KI��Ӧ�ĸ��ţ�
�����ж���������������Eװ�����գ�������������Һ ������������Һ ��������������Һ ���Ȼ�������Һ�����⻯����Һ ��̼��������Һ��������������Ӧ�����Ǣ�����������Һ ��������������Һ��������Ӧʱ�����ɶ�����������⻯����Һ��������Ӧʱ���������������壬������������ⶼ���ж������壬��Ⱦ���������Բ���������������Һ��
�ʴ�Ϊ��û���ų��������嵥����KI��Ӧ�ĸ��ţ��٢ܢޣ�
���� ���⿼�����������Ʊ������ӡ����ʼ��顢β������װ�õķ�����ע����ȷʵ��װ�ü�ʵ��ԭ���ǽ��Ĺؼ�����Ŀ�Ѷ��еȣ�

| A�� | KOH��Һ��������ˮ��Һ | B�� | Na2CO3��Һ��HCl��Һ | ||
| C�� | NaHCO3��Һ��HCl��Һ | D�� | �����NaAlO2��Һ |
| A�� | ������ˮ���������H+�����ʵ���Ũ������$\frac{1}{10}$�ı� | |
| B�� | �ס���������Һ���ʵ���Ũ��֮��Ĺ�ϵΪ��c���ף�=10c���ң� | |
| C�� | �кͺ��е����ʵ���NaOH����Һ����ס���������������V��֮���ϵΪ��10V���ף���V���ң� | |
| D�� | ���е�c��OH-��Ϊ���е�c��OH-����10�� |
| A�� | ϡ�����̼������Һ | B�� | �Ȼ�����Һ������������Һ | ||
| C�� | ϡ�����ƫ��������Һ | D�� | ̼������Һ���Ȼ�����Һ |
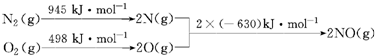
д���÷�Ӧ���Ȼ�ѧ����ʽ��N2��g��+O2��g��=2NO��g����H=+183KJ/mol��
��2��ͨ�����ǰѲ�1molij��ѧ�������յ��������ɸû�ѧ���ļ��ܣ����ܵĴ�С���Ժ�����ѧ����ǿ����Ҳ���Թ��㻯ѧ��Ӧ�ķ�Ӧ�ȣ���H������ѧ��Ӧ�ġ�H���ڷ�Ӧ�ж��Ѿɻ�ѧ���ļ���֮���뷴Ӧ���γ��»�ѧ���ļ���֮�͵IJ
| ��ѧ�� | Si-O | Si-Cl | H-H | H-Cl | Si-Si | Si-C |
| ����/kJ•mol-1 | 460 | 360 | 436 | 431 | 176 | 347 |
��3������ʯ[��Ҫ�ɷ�Ca5��PO4��3F]�ڸ������Ʊ����ף�P4�����Ȼ�ѧ����ʽΪ��4Ca5��PO4��3F��s��+21SiO2��s��+30C��s���T3P4��g��+20CaSiO3��s��+30CO��g��+SiF4��g����H
��֪��ͬ�����£�
4Ca5��PO4��3F��s��+3SiO2��s���T6Ca3��PO4��2��s��+2CaSiO3��s��+SiF4��g����H1
2Ca3��PO4��2��s��+10C��s���TP4��g��+6CaO��s��+10CO��g����H2
SiO2��s��+CaO��s���TCaSiO3��s����H3
�á�H1����H2�͡�H3��ʾ��H����H=��H1+3��H2+18��H3��
��4����H2O2��H2SO4�Ļ����Һ���ܳ�ӡˢ��·�������ĩ�е�ͭ����֪��
��Cu��s��+2H+��aq���TCu2+��aq��+H2��g����H1=+64.39kJ•mol-1
��2H2O2��l���T2H2O��l��+O2��g����H2=-196.46kJ•mol-1
��H2��g��+$\frac{1}{2}$O2��g���TH2O��l����H3=-285.84kJ•mol-1
��H2SO4��Һ�У�Cu��H2O2��Ӧ����Cu2+��H2O���Ȼ�ѧ����ʽΪCu��s��+H2O2��l��+2H+��aq��=Cu2+��aq��+2H2O��l����H=-319.6KJ/mol��
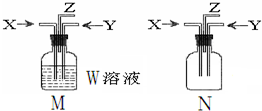 ������ͼM��N����װ�ý������ʵ�飬�����й�˵����ȷ���ǣ�������
������ͼM��N����װ�ý������ʵ�飬�����й�˵����ȷ���ǣ�������| ѡ�� | ����װ�� | ���� | ���� |
| A | M | W��BaCl2��X��CO2 Y��SO2 | M���а�ɫ�������� |
| B | M | W������ʳ��ˮ����ͨ��X��CO2����ͨ��Y��NH3 | M���Ƶ�С�մ� |
| C | N | X��NH3������Y��Cl2 | Z�����а��̲��� |
| D | N | X��NH3Y��O2 | Z�����к���ɫ���� |
| A�� | A | B�� | B | C�� | C | D�� | D |
| A�� | �ô����������������ƻ�̼���� | |
| B�� | �ò�����պȡ��Һ������ʪ���pH��ֽ�ϲⶨ��Һ��pHֵ | |
| C�� | ��NaOH��Һϴ�Ӳ����ղ�˿���ٽ�����ɫ��Ӧ | |
| D�� | ��ȡ��Ͳ����ҺҺ�����������Ӷ������¶���ƫ�� |
| A�� | �ڢܢݢۢ٢� | B�� | �ۢڢܢ٢ݢ� | C�� | �ۢܢڢݢ٢� | D�� | �ڢܢۢݢ٢� |
| A�� | ���ǵؿ��к������Ľ���Ԫ�� | |
| B�� | ����������������Һ��Ӧ��������NaOH��Һ��Ӧ | |
| C�� | �ڳ����£������ܺ�������Ӧ | |
| D�� | �ڻ�ѧ��Ӧ�У�������ʧȥ���ӣ��ǻ�ԭ�� |