题目内容
3.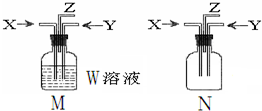 利用如图M、N两个装置进行相关实验,下列有关说法正确的是( )
利用如图M、N两个装置进行相关实验,下列有关说法正确的是( )| 选项 | 所用装置 | 描述 | 结论 |
| A | M | W:BaCl2;X:CO2 Y:SO2 | M中有白色沉淀生成 |
| B | M | W:饱和食盐水;先通入X:CO2,再通入Y:NH3 | M中制得小苏打 |
| C | N | X:NH3 Y:Cl2 | Z出口有白烟产生 |
| D | N | X:NH3Y:O2 | Z出口有红棕色气体 |
| A. | A | B. | B | C. | C | D. | D |
分析 A.弱酸不能制取强酸;
B.二氧化碳在水中的溶解度较小;
C.氯气与氨气反应生成氯化氢和氮气;
D.氨气与氧气常温下不反应.
解答 解:A.二氧化碳、二氧化硫与氯化钡不反应,无白色沉淀,故A错误;
B.二氧化碳在水中的溶解度较小,应先通入氨气,故B错误;
C.氯气与氨气反应生成氯化氢和氮气,生成的氯化氢会与氨反应生成氯化铵,故C正确;
D.氨气与氧气常温下不反应,无二氧化氮生成,故D错误.
故选C.
点评 本题考查化学实验方案的评价,为高频考点,涉及物质的反应等,侧重实验基本操作和实验原理的考查,注意装置的作用及实验的操作性、评价性分析,题目难度不大.

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目
14.医学研究证明,用放射性$\stackrel{135}{53}$I治疗肿瘤可收到一定疗效,下列有关$\stackrel{135}{53}$I叙述正确的是( )
| A. | $\stackrel{135}{53}$I是碘的一种同素异形体 | |
| B. | $\stackrel{135}{53}$I是一种新发现的元素 | |
| C. | $\stackrel{135}{53}$I位于元素周期表中第四周期ⅦA族 | |
| D. | $\stackrel{135}{53}$I核内的中子数与核外电子数之差为29 |
11.实验室需用480毫升0.1mol•L-1的硫酸铜溶液,若用胆矾(CuSO4•5H2O)或无水硫酸铜配制,下列操作中正确的是( )
| A. | 取12.0 g胆矾溶于480m L水中 | |
| B. | 取8.0 g CuSO4溶于480m L水 | |
| C. | 取12.5 g胆矾溶于水,再转入500mL容量瓶中,加水至刻度 | |
| D. | 取12.5 g胆矾加热除去结晶水,再放入500mL容量瓶中,加水至刻度 |
18.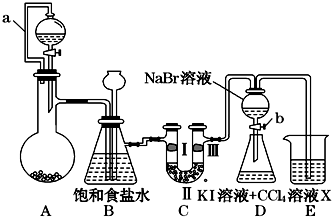 某同学设计如图所示的实验方案:
某同学设计如图所示的实验方案:
(1)A装置的分液漏斗里盛装浓盐酸,烧瓶里固体为重铬酸钾(K2Cr2O7),还原产物是CrCl3,写出A中离子方程式:Cr2O72-+14H++6Cl-═2Cr3++3Cl2↑+7H2O.
(2)本实验目的是制备氯气并探究氯气等物质的相关性质,B装置有几个作用,分别是除去氯气中的氯化氢、安全瓶,检测实验过程中装置是否堵塞.拆去a导管的后果可能是酸不能顺利滴入烧瓶.
(3)装置C的功能是探究有氧化性的物质是否一定有漂白性,下列最佳试剂组合是②.
(4)证明溴的非金属性比碘强的实验操作和现象是实验完毕,打开活塞b,使少量液体流入锥形瓶,关闭活塞,振荡锥形瓶,下层液体呈紫红色.
(5)D装置进行实验时存在明显不足,它是没有排除氯气对溴单质与KI反应的干扰,合适的溶液X是①④⑥ (从①氢氧化钠溶液②亚硫酸钠溶液③亚硫酸氢钠溶液④氯化亚铁溶液⑤硫氢化钠溶液⑥碳酸氢钠溶液中选择).
 某同学设计如图所示的实验方案:
某同学设计如图所示的实验方案:(1)A装置的分液漏斗里盛装浓盐酸,烧瓶里固体为重铬酸钾(K2Cr2O7),还原产物是CrCl3,写出A中离子方程式:Cr2O72-+14H++6Cl-═2Cr3++3Cl2↑+7H2O.
(2)本实验目的是制备氯气并探究氯气等物质的相关性质,B装置有几个作用,分别是除去氯气中的氯化氢、安全瓶,检测实验过程中装置是否堵塞.拆去a导管的后果可能是酸不能顺利滴入烧瓶.
(3)装置C的功能是探究有氧化性的物质是否一定有漂白性,下列最佳试剂组合是②.
| ① | ② | ③ | ④ | |
| Ⅰ | 湿润的红纸条 | 干燥的红纸条 | 干燥的红纸条 | 湿润的红纸条 |
| Ⅱ | 碱石灰 | 浓硫酸 | 硅胶 | 氯化钠 |
| Ⅲ | 湿润的红纸条 | 干燥的红纸条 | 干燥的白纸条 | 干燥的红纸条 |
(5)D装置进行实验时存在明显不足,它是没有排除氯气对溴单质与KI反应的干扰,合适的溶液X是①④⑥ (从①氢氧化钠溶液②亚硫酸钠溶液③亚硫酸氢钠溶液④氯化亚铁溶液⑤硫氢化钠溶液⑥碳酸氢钠溶液中选择).
8.C、N、S都是重要的非佥属元素,下列说法正确的是( )
| A. | 三者对应的氧化物均为酸性氧化物 | |
| B. | 三者的单质直接与氧气反应都能生成两种及以上氧化物 | |
| C. | 三者对应氢化物的水溶液可能呈中性、碱性、酸性 | |
| D. | C02、N02、S02都能与H20反应,其反应类型相同 |
12.欲除去下列物质中的少量杂质,请填写所用方法及反应的离子方程式.
| 欲除去的少量杂质 | 方法 | 反应的离子方程式 |
| (1)Na2CO3溶液中的NaHCO3 | ||
| (2)NaCl溶液中的Na2CO3 | ||
| (3)NaHCO3溶液中的Na2CO3 |