题目内容
12.下列反应是氧化还原反应的是( )| A. | CO2+Ca(OH)2=CaCO3↓+H2O | B. | SO3+H2O=H2SO4 | ||
| C. | 2KMnO4=K2MnO4+MnO2+O2↑ | D. | 2NaHCO3=Na2CO3+CO2↑+H2O |
分析 氧化还原反应的实质是电子转移,特征为化合价升降,所以有元素的化合价变化的反应一定为氧化还原反应,根据各反应中是否存在元素化合价变化进行判断.
解答 解:A.CO2+Ca(OH)2=CaCO3↓+H2O为复分解反应,复分解反应中不存在化合价变化,一定不属于氧化还原反应,故A错误;
B.反应SO3+H2O=H2SO4中不存在元素化合价变化,不属于氧化还原反应,故B错误;
C.2KMnO4=K2MnO4+MnO2+O2↑中存在Mn、O元素化合价变化,属于氧化还原反应,故C正确;
D.2NaHCO3=Na2CO3+CO2↑+H2O中不存在元素化合价变化,不属于氧化还原反应,故D错误;
故选C.
点评 本题考查氧化还原反应,侧重氧化还原反应的判断,明确反应中元素的化合价变化及常见的反应即可解答,题目难度不大.

练习册系列答案
 小学教材全测系列答案
小学教材全测系列答案 小学数学口算题卡脱口而出系列答案
小学数学口算题卡脱口而出系列答案
相关题目
7.下列事实一定能说明HF是弱酸的是( )
①常温下NaF溶液的pH大于7
②用HF溶液做导电性实验,灯泡很暗
③常温下0.1mol/L的HF溶液的pH为2.3
④HF能与Na2CO3溶液反应,产生CO2气体
⑤HF与水能以任意比混溶
⑥1mol/L的HF水溶液能使紫色石蕊试液变红.
①常温下NaF溶液的pH大于7
②用HF溶液做导电性实验,灯泡很暗
③常温下0.1mol/L的HF溶液的pH为2.3
④HF能与Na2CO3溶液反应,产生CO2气体
⑤HF与水能以任意比混溶
⑥1mol/L的HF水溶液能使紫色石蕊试液变红.
| A. | ①③ | B. | ②③⑤ | C. | ④⑥ | D. | ①②⑤ |
17.咖啡酸具有止血、镇咳、祛痰等疗效,其结构简式为有关咖啡酸的说法中不正确的是( )
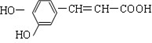

| A. | 咖啡酸可以发生还原、取代、加聚等反应 | |
| B. | 1 mol咖啡酸最多能消耗3 mol的NaHCO3 | |
| C. | 1 mol咖啡酸可与4 mol H2 发生加成反应 | |
| D. | 咖啡酸与FeCl3 溶液可以发生显色反应 |
4.下列防止金属腐蚀的做法不可行的是( )
| A. | 在某些工具的机械转动部位刷油漆以防锈 | |
| B. | 自行车的钢圈和车铃上镀上一层铬,既耐腐蚀又美观耐磨 | |
| C. | 自行车车辐条上的镀锌层部分破损,还可以为铁提供保护 | |
| D. | 钢铁在潮湿的环境中更易生锈,要在电线外面包上一层塑料层以防锈 |
1.下列装置或操作不能达到目的是( )
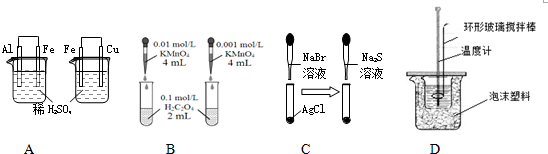

| A. | 依据左烧杯中铁表面有气泡,右边烧杯中铜表面有气泡,判断活动性:Al>Fe>Cu | |
| B. | 依据褪色快慢比较浓度对反应速率的影响 | |
| C. | 依据白色固体先变为淡黄色,后变为黑色(Ag2S),判断溶解性:AgCl>AgBr>Ag2S | |
| D. | 用该装置测定中和热 |
2.把a、b、c、d四块金属片浸入稀硫酸,分别用导线两两连接,可以组成原电池.a、b相连时,a为负极;c、d相连时,电流方向为d→c;a、c相连时,c极产生大量气泡;b、d相连时,d极上发生氧化反应.这四种金属的活动性由强到弱的顺序是( )
| A. | a b c d | B. | a c d b | C. | c a b d | D. | b d c a |