题目内容
取100mL 18.3mol•L﹣1 的H2SO4与Zn反应,当Zn完全溶解时,生成的气体(可使品红褪色)在标准状况下的体积为22.4L.将所得的溶液稀释成1L,测得溶液H+的浓度为1mol•L﹣1,则所生成的气体中SO2与H2的体积比约为( )
A.1:2 B.2:1 C.1:4 D.4:1
练习册系列答案
相关题目
19.下列说法正确的是( )
| A. | 25℃时,对于pH相同的弱碱ROH和MOH(前者的电离平衡常数Kb较小),加水稀释后溶液的pH仍相同,则后者稀释的倍数更大 | |
| B. | 25℃时,0.1mol•L-1的HA溶液中$\frac{c(O{H}^{-})}{c({H}^{+})}$=1×10-8,则该溶液中由水电离出的c(H+)=1×10-3mol•L-1 | |
| C. | 25℃时,等物质的量浓度、等体积的NH4HSO4溶液和NaOH溶液混合:c(Na+)=c(SO${\;}_{4}^{2-}$)>c(NH${\;}_{4}^{+}$)>c(H+)>c(OH-) | |
| D. | 25℃时,沉淀溶解平衡:BaSO4(s)?Ba2+(aq)+SO${\;}_{4}^{2-}$(aq)的Ksp为1.1×10-10,说明BaSO4是弱电解质 |
5.下列说法正确的是( )
| A. | 甲烷的燃烧热为△H=-890.3 kJ/mol,则甲烷燃烧的热化学方程式可表示为CH4(g)+2O2(g)═CO2(g)+2H2O(g)△H=-890.3 kJ/mol | |
| B. | 已知H2O(l)═H2O(g)△H=+44 kJ/mol,则2 g H2(g)完全燃烧生成液态水比生成气态水多释放22 kJ的能量 | |
| C. | 常温下,反应C(s)+CO2(g)═2CO(g)不能自发进行,则该反应的△H<0 | |
| D. | 1 mol NaOH分别和1 mol CH3COOH、1 mol HNO3反应,后者比前者△H小 |
12.下列反应是氧化还原反应的是( )
| A. | CO2+Ca(OH)2=CaCO3↓+H2O | B. | SO3+H2O=H2SO4 | ||
| C. | 2KMnO4=K2MnO4+MnO2+O2↑ | D. | 2NaHCO3=Na2CO3+CO2↑+H2O |
9.下列有关实验现象的描述中,正确的是( )
| A. | 金属钠在氯气中燃烧,有白雾生成 | |
| B. | 铜在氯气中燃烧,生成蓝色的氯化铜颗粒 | |
| C. | 红热的铁丝在氧气中剧烈燃烧,火星四射,生成黑色固体 | |
| D. | 氢气在氯气中燃烧产生大量的白烟 |
10.下列电离方程式错误的是( )
| A. | (NH4)2SO4溶于水:(NH4)2SO4═2NH4++SO42- | |
| B. | H3PO4溶于水:H3PO4?3H++PO43- | |
| C. | HF溶于水:HF?H++F- | |
| D. | NaHS溶于水:NaHS═Na++HS- |


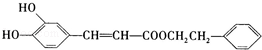 是一种天然抗癌药物,在一定条件下能发生如下转化:
是一种天然抗癌药物,在一定条件下能发生如下转化: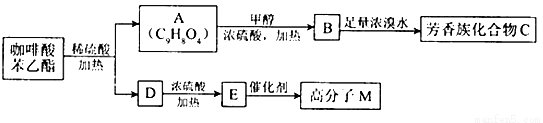
 条件下1molA最多能与1mol氢气加成
条件下1molA最多能与1mol氢气加成