题目内容
4.下列防止金属腐蚀的做法不可行的是( )| A. | 在某些工具的机械转动部位刷油漆以防锈 | |
| B. | 自行车的钢圈和车铃上镀上一层铬,既耐腐蚀又美观耐磨 | |
| C. | 自行车车辐条上的镀锌层部分破损,还可以为铁提供保护 | |
| D. | 钢铁在潮湿的环境中更易生锈,要在电线外面包上一层塑料层以防锈 |
分析 钢铁易发生电化学腐蚀,铁发生电化学腐蚀的条件是:水和氧气,为防止铁被腐蚀,应该隔绝空气和水中的一种或两种,或将被保护的金属作原电池正极或电解池阴极,据此分析解答.
解答 解:A.在某些工具的机械转动部位刷油漆,能隔绝空气和水,但转动部位漆易脱落,应该涂油,故A错误;
B.自行车的钢圈和车铃上镀上一层铬,能隔绝空气和水,且Cr不易发生腐蚀,所以能防止铁生锈,故B正确;
C.在自行车车辐条上的镀锌,Fe、Zn和水、氧气构成原电池,Zn易失电子作负极、Fe作正极,所以被保护,故C正确;
D.在电线外面包上一层塑料层,能隔绝空气和水,所以能防锈,故D正确;
故选A.
点评 本题考查金属的腐蚀与防护,明确原电池原理是解本题关键,防止金属被腐蚀的方法有:涂油漆、作原电池正极、作电解池阴极、改变金属结构等,题目难度不大.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
2.下列各组数据关系中,前者比后者大的是( )
| A. | 常温常压下,0.1mol/L的KOH溶液和0.1mol/L的醋酸溶液中,由水电离的OH-浓度 | |
| B. | 常温常压下,0.1mol/L的KOH溶液和0.1mol/L的盐酸溶液中,由水电离的OH-浓度 | |
| C. | 25℃,100mL0.1mol/L醋酸溶液与10 mL 1 mol/L醋酸溶液中的k(HAc) | |
| D. | 100mL0.1mol/L醋酸溶液与10 mL 1 mol/L醋酸溶液中H+的数目 |
12.下列反应是氧化还原反应的是( )
| A. | CO2+Ca(OH)2=CaCO3↓+H2O | B. | SO3+H2O=H2SO4 | ||
| C. | 2KMnO4=K2MnO4+MnO2+O2↑ | D. | 2NaHCO3=Na2CO3+CO2↑+H2O |
19.有关下列电化学装置的说法中正确的是( )
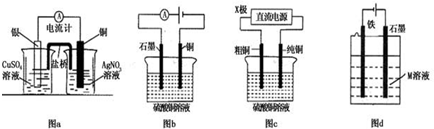

| A. | 图a是原电池装置,且较长时间内,电流计会显示有稳定电流产生 | |
| B. | 图b 电解足量硫酸铜溶液一段时间后,加入适量CuCO3固体,可以使硫酸铜溶液恢复到原浓度 | |
| C. | 图c中的X极若为负极,则该装置可实现粗铜的精炼 | |
| D. | 图d中若M是海水,该装置是通过“牺牲阳极保护法”使铁不被腐蚀 |
9.下列有关实验现象的描述中,正确的是( )
| A. | 金属钠在氯气中燃烧,有白雾生成 | |
| B. | 铜在氯气中燃烧,生成蓝色的氯化铜颗粒 | |
| C. | 红热的铁丝在氧气中剧烈燃烧,火星四射,生成黑色固体 | |
| D. | 氢气在氯气中燃烧产生大量的白烟 |
16.下列反应的离子方程式书写正确的是( )
| A. | 大理石和盐酸的反应:CO32ˉ+2H+═CO2↑+H2O | |
| B. | KI溶液中加入硫酸酸化的过氧化氢溶液:2I-+H2O2═I2+2OH- | |
| C. | 三氯化铁溶液与铁反应:Fe3++Fe═2Fe2+ | |
| D. | 二氧化硅与氢氧化钠溶液反应:SiO2+2OHˉ═SiO32ˉ+H2O |
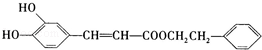 是一种天然抗癌药物,在一定条件下能发生如下转化:
是一种天然抗癌药物,在一定条件下能发生如下转化: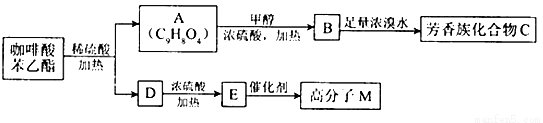
 条件下1molA最多能与1mol氢气加成
条件下1molA最多能与1mol氢气加成