题目内容
1.NA表示阿伏加德罗常数的值,下列说法正确的是( )| A. | 标准状况下,22.4 L二氯甲烷的分子数约为NA个 | |
| B. | 盛有SO2的密闭容器中含有NA个氧原子,则SO2的物质的量为0.5 mol | |
| C. | 17.6 g丙烷中所含的极性共价键为4NA个 | |
| D. | 在过氧化钠与水的反应中,每生成0.1 mol氧气,转移电子的数目为0.4NA |
分析 A、标况下二氯甲烷为液态;
B、1个二氧化硫分子中含2个氧原子;
C、求出丙烷的物质的量,然后根据1mol丙烷中含8mol极性共价键来分析;
D、过氧化钠和水反应中,氧元素的价态由-1价变为0价.
解答 解:A、标况下二氯甲烷为液态,故不能根据气体摩尔体积来计算其物质的量和含有的分子个数,故A错误;
B、1个二氧化硫分子中含2个氧原子,故当含有NA个氧原子时,二氧化硫分子的个数为0.5NA个,即0.5mol,故B正确;
C、17.6g丙烷的物质的量为n=$\frac{17.6g}{44g/mol}$=0.4mol,而1mol丙烷中含8mol极性共价键,故0.4mol丙烷中含3.2NA条共价键,故C错误;
D、过氧化钠和水反应中,氧元素的价态由-1价变为0价,故当生成0.1mol氧气时,转移0.2NA个电子,故D错误.
故选B.
点评 本题考查了阿伏伽德罗常数的有关计算,熟练掌握公式的使用和物质的结构是解题关键,难度不大.

练习册系列答案
相关题目
9.下列各项中表达正确的是( )
| A. | 第VⅡA族元素形成的氢化物中沸点最高的是HI | |
| B. | 第三周期元素形成的简单离子中,半径最小的是Al3+ | |
| C. | 用电子式表示HCl形成过程: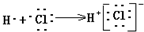 | |
| D. | 水分子很稳定性是因为水分子间易形成氢键 |
16.下列有关维生素C的说法中,正确的是( )
| A. | 如果人体缺少维生素C,易患夜盲症、干眼症等眼疾 | |
| B. | 维生素C属于脂溶性维生素,主要存在于新鲜水果和蔬菜中 | |
| C. | 维生素C具有较强的还原性,能使酸性高锰酸钾溶液褪色 | |
| D. | 富含维生素C的食物应在高温下烹调,才能充分提高维生素C的功能 |
10.用如图装置完成相关实验,不合理的是( )
| A. | 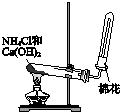 制备并收集氨气 | B. |  制备氯气 | ||
| C. | 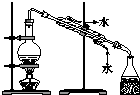 蒸馏海水得到淡水 | D. | 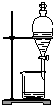 分离Na2CO3溶液与CH3COOC2H5 |
11.如图是某同学画的氮元素基态原子核外电子排布图,该电子排布图违背了下列哪个原理( )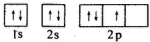

| A. | 洪特规则 | B. | 泡利原理 | C. | 能量最低原理 | D. | 洪特规则特例 |
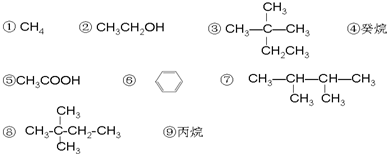
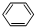 +Br2$\stackrel{FeBr_{3}}{→}$
+Br2$\stackrel{FeBr_{3}}{→}$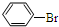 +HBr;
+HBr;