题目内容
下列各图均能表示甲烷的分子结构,哪一种更能反映其真实存在状况( ) 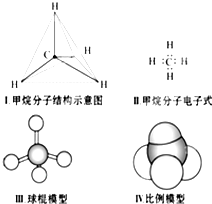

| A、Ⅰ | B、Ⅱ | C、Ⅲ | D、Ⅳ |
考点:电子式、化学式或化学符号及名称的综合,球棍模型与比例模型
专题:
分析:根据比例模型表示的是原子的相对大小及连接形式可知,甲烷的比例模型更能够反映其真实存在状况.
解答:
解:比例模型表示的是原子的相对大小及连接形式,所以甲烷的比例模型更接近分子的真实结构,所以Ⅳ正确,
故选D.
故选D.
点评:本题考查学生对甲烷分子结构的熟悉了解程度,题目难度不大,试题侧重基础知识的考查,意在培养学生的空间想象能力,有利于提高学生的学习兴趣和学习积极性.

练习册系列答案
相关题目
某矿石由前20号元素中的4种组成,其化学式为WYZX4.X、Y、Z、W分布在三个周期,原子序数依次增大,W、Y为金属元素,X原子的最外层电子数是次外层电子数的3倍,W能与冷水剧烈反应,Y、Z原子的最外层电子数之和与X、W原子的最外层电子数之和相等,Y、Z位于同周期,Z单质是一种良好的半导体.下列说法正确的是( )
| A、Y和W的最高价氧化物的水化物之间可以发生反应 |
| B、X和Y的单核离子半径:X<Y |
| C、由W和X形成原子个数比1:1的化合物不可能与H2O反应生成X的单质 |
| D、Y、Z的氧化物都有两性 |
某溶液由Na+、Cu2+、Ba2+、Fe3+、AlO2-、CO32-、SO42-、Cl-中的若干种离子组成,取适量该溶液进行如下实验:下列说法正确的是( )
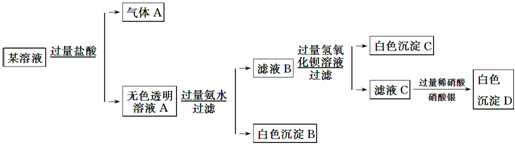

| A、原溶液中一定存在AlO2-、CO32-、SO42-、Cl-四种离子 |
B、气体A的化学式是CO2,其电子式为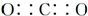 |
| C、原溶液中一定不存在的离子是Cu2+、Ba2+、Fe3+ |
| D、生成沉淀B的离子方程式为:Al3++3OH-=Al(OH)3↓ |
早在1807年化学家戴维用电解熔融氢氧化钠制得钠,反应原理为:4NaOH(熔融)=4Na+O2↑+2H2O;后来盖?吕萨克用铁与熔融氢氧化钠作用也制得钠,反应原理为:3Fe+4NaOH=Fe3O4+2H2↑+4Na↑.下列有关说法不正确的是( )
| A、电解熔融氢氧化钠制钠,阴极发生电极反应为:Na++e-=Na |
| B、盖?吕萨克法制钠原理是利用铁的还原性比钠强 |
| C、若戴维法与盖?吕萨克法制得等量的钠,则两反应中转移的电子总数比为1:2 |
D、目前工业上常用电解熔融氯化钠法制钠(如图),电解槽中石墨极为阳极,铁为阴极 |
设NA为阿伏加德罗常数的值,下列有关叙述正确的是( )
| A、28g乙烯所含共用电子对数目为4NA |
| B、0.5 mol1,3-丁二烯分子中含有C=C双键数为 NA |
| C、1 mol羟基所含的电子总数为9NA |
| D、标准状况下,11.2 L己烷所含分子数为0.5 NA |
下列关于胶体的叙述不正确的是( )
| A、利用丁达尔现象可以区别溶液和胶体 |
| B、胶体都可以发生丁达尔现象 |
| C、胶体粒子的大小都在1nm-100nm之间 |
| D、加热氢氧化铁胶体没有明显现象 |
下列各组离子因为生成难溶物而不能大量共存的是( )
| A、Cl-、Fe3+、NO3-、OH- |
| B、HCO3-、Cl-、Na+、H+ |
| C、Ba2+、Cl-、NO3-、K+ |
| D、NH4+、K+、OH-、Cl- |
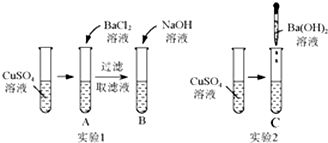 仔细分析如图中的实验:
仔细分析如图中的实验: