题目内容
设NA为阿伏加德罗常数的值,下列有关叙述正确的是( )
| A、28g乙烯所含共用电子对数目为4NA |
| B、0.5 mol1,3-丁二烯分子中含有C=C双键数为 NA |
| C、1 mol羟基所含的电子总数为9NA |
| D、标准状况下,11.2 L己烷所含分子数为0.5 NA |
考点:阿伏加德罗常数
专题:
分析:A、依据n=
计算物质的量结合乙烯分子结构计算共用电子对数;
B、1,3-丁二烯分子中含有2个碳碳双键;
C、羟基是中性原子团,羟基中含有9个电子;
D、标准状况,己烷不是气体,不能使用标况下的气体摩尔体积计算己烷的物质的量.
| m |
| M |
B、1,3-丁二烯分子中含有2个碳碳双键;
C、羟基是中性原子团,羟基中含有9个电子;
D、标准状况,己烷不是气体,不能使用标况下的气体摩尔体积计算己烷的物质的量.
解答:
解:A、28g乙烯物质的量为:
=1mol,所含共用电子对数目为6NA,故A错误;
B、1,3-丁二烯分子中含有2个碳碳双键,0.5mol 1,3-丁二烯分子中含有C=C双键数为NA,故B正确;
C、1 mol羟基-OH中含有9mol电子,所含的电子总数为9NA,故C正确;
D、标准状况,己烷不是气体,11.2 L己烷物质的量不是0.5mol,故D错误;
故选BC.
| 28g |
| 28g/mol |
B、1,3-丁二烯分子中含有2个碳碳双键,0.5mol 1,3-丁二烯分子中含有C=C双键数为NA,故B正确;
C、1 mol羟基-OH中含有9mol电子,所含的电子总数为9NA,故C正确;
D、标准状况,己烷不是气体,11.2 L己烷物质的量不是0.5mol,故D错误;
故选BC.
点评:本题考查阿伏加德罗常数的综合应用,题目难度中等,注意明确分子、原子、原子核内质子中子及核外电子的构成关系,熟练掌握物质的量与阿伏伽德罗常数、摩尔质量等物理量之间关系.

练习册系列答案
 寒假天地重庆出版社系列答案
寒假天地重庆出版社系列答案
相关题目
把0.05molNaOH固体分别加入到100mL液体中,溶液的导电能力变化不大的是( )
| A、自来水 |
| B、0.5mol?L-1醋酸 |
| C、0.5mol?L-1硝酸 |
| D、0.5mol?L-1NaCl溶液 |
下列各图均能表示甲烷的分子结构,哪一种更能反映其真实存在状况( ) 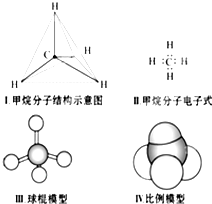

| A、Ⅰ | B、Ⅱ | C、Ⅲ | D、Ⅳ |
下列说法不正确的是( )
| A、淀粉溶液具有丁达尔效应 |
| B、光线通过胶体可以产生丁达尔效应的原因是光的散射 |
| C、胶体的分散质粒子可以通过滤纸孔隙,所以可以通过过滤操作分离溶液和胶体 |
| D、胶体属于介稳体系 |
能用H++OH-=H2O来表示的化学反应是( )
| A、氢氧化铜和稀盐酸反应 |
| B、氢氧化钡溶液滴入稀硫酸中 |
| C、氢氧化钠溶液与硝酸反应 |
| D、醋酸和氢氧化钾溶液 |
下列叙述正确的是( )
| A、NaCl溶液在电流的作用下电离出Na+ |
| B、离子化合物一定是电解质 |
| C、氨水呈弱碱性,故NH3是弱电解质 |
| D、溶于水电离出氢离子的化合物都是酸 |
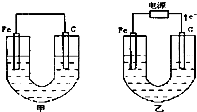 甲、乙两池电极材料都是铁棒与碳棒,请回答下列问题:
甲、乙两池电极材料都是铁棒与碳棒,请回答下列问题: