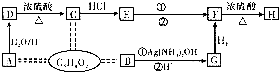
题目内容
(1)下列物质中,标准状况下体积最大的是 ,含原子个数最多的是 .
A.6g H2 B.0.8mol CO2 C.1.204×1024个H2S分子D.147gH2SO4 E.27mL水
(2)铁的相对原子质量为56,若阿伏加德罗常数取6.02×1023mol-1,则可估算一个铁原子的质量约为 g.
A.6g H2 B.0.8mol CO2 C.1.204×1024个H2S分子D.147gH2SO4 E.27mL水
(2)铁的相对原子质量为56,若阿伏加德罗常数取6.02×1023mol-1,则可估算一个铁原子的质量约为
考点:物质的量的相关计算
专题:
分析:根据n=
=
=
计算相关物理量.
| m |
| M |
| N |
| NA |
| V |
| Vm |
解答:
解:(1)A.6g H2的物质的量为
=3mol,
B.0.8mol CO2,
C.H2S的物质的量为
=2mol,
D.147g H3PO4的物质的量为
=1.5mol,
E.水的质量为27mL×1g/mL=27g,水的物质的量为
=1.5mol;
故物质的量最大的是:6g H2;
磷酸与水时液体,相同物质的量体积远远小于气体,根据V=nVm可知,气体的物质的量越大,体积越大,故体积最大的是6g H2;
氢气中含有原子为3mol×2=6mol,二氧化碳中含有原子为0.8mol×3=2.4mol,硫化氢中含有原子为2mol×3=6mol,
磷酸中含有原子为1.5mol×8=12mol,水中含有原子为1.5mol×3=4.5mol,故含有原子最多的是:147g H3PO4;
故答案为:A;D;
(2)铁的相对原子质量为56,则1molFe的质量为56g,若阿伏加德罗常数取6.02×1023mol-1,则可估算一个铁原子的质量约为
g,
故答案为:
.
| 6g |
| 2g/mol |
B.0.8mol CO2,
C.H2S的物质的量为
| 1.204×1024 |
| 6.02×1023mol-1 |
D.147g H3PO4的物质的量为
| 147g |
| 98g/mol |
E.水的质量为27mL×1g/mL=27g,水的物质的量为
| 27g |
| 18g/mol |
故物质的量最大的是:6g H2;
磷酸与水时液体,相同物质的量体积远远小于气体,根据V=nVm可知,气体的物质的量越大,体积越大,故体积最大的是6g H2;
氢气中含有原子为3mol×2=6mol,二氧化碳中含有原子为0.8mol×3=2.4mol,硫化氢中含有原子为2mol×3=6mol,
磷酸中含有原子为1.5mol×8=12mol,水中含有原子为1.5mol×3=4.5mol,故含有原子最多的是:147g H3PO4;
故答案为:A;D;
(2)铁的相对原子质量为56,则1molFe的质量为56g,若阿伏加德罗常数取6.02×1023mol-1,则可估算一个铁原子的质量约为
| 56 |
| 6.02×1023 |
故答案为:
| 56 |
| 6.02×1023 |
点评:本题考查物质的量的相关计算,为高频考点,侧重于学生的分析、计算能力的考查,注意把握相关计算公式的运用,难度中等.

练习册系列答案
相关题目
在Cl2+2NaOH=NaCl+NaClO+H2O反应中,氧化剂与还原剂的物质的量之比为( )
| A、1:2 | B、1:1 |
| C、2:1 | D、3:2 |
硫酸钾和硫酸铝的混合溶液,已知其中Al3+的浓度为0.4mol/L,硫酸根离子浓度为0.7mol/L,则K+的物质的量浓度为( )
| A、0.1 mol/L |
| B、0.15 mol/L |
| C、0.3 mol/L |
| D、0.2 mol/L |
把0.05molNaOH固体分别加入到100mL液体中,溶液的导电能力变化不大的是( )
| A、自来水 |
| B、0.5mol?L-1醋酸 |
| C、0.5mol?L-1硝酸 |
| D、0.5mol?L-1NaCl溶液 |
下列各图均能表示甲烷的分子结构,哪一种更能反映其真实存在状况( ) 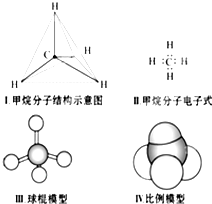

| A、Ⅰ | B、Ⅱ | C、Ⅲ | D、Ⅳ |
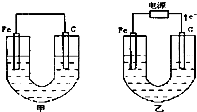 甲、乙两池电极材料都是铁棒与碳棒,请回答下列问题:
甲、乙两池电极材料都是铁棒与碳棒,请回答下列问题: