题目内容
12.某小组探究金属铜与一定物质的量浓度的HNO3反应,将制得的气体通过浓硫酸后被完全吸收,由此做出猜想:①NO2溶于浓硫酸或与浓硫酸反应;②NO溶于浓硫酸或与浓硫酸反应,并进行下列实验:实验一:将制得的纯净的NO2通入浓硫酸中,溶液变成棕黄色,加热浓硫酸,气体逸出,溶液颜色褪去;
实验二:将制得的纯净的NO通过浓硫酸后用排水集气法收集到足量无色气体,通入氧气后气体变成红棕色;
(1)由此得出的结论是NO2溶于浓硫酸但不与浓硫酸反应,NO不溶于浓硫酸也不与浓硫酸反应
(2)查阅资料得知:NO、NO2等体积通入浓硫酸中反应生成NOHSO4,气体被全部吸收,试写出此反应的化学方程式NO+NO2+2H2SO4=2NOHSO4+H2O
(3)为制得干燥的NO2,可将湿润的NO2通过干燥的CaCl2干燥.也可用Pb(NO3)2加热制得含有NO2的混合气体,并用冰盐水冷却后可得到纯净的液态NO2,试写出Pb(NO3)2加热的化学方程式2Pb(NO3)2$\frac{\underline{\;加热\;}}{\;}$2PbO+4NO2↑+O2↑
分析 (1)由实验一和实验二中的现象分析;
(2)NO、NO2等体积通入浓硫酸中反应生成NOHSO4,根据原子守恒书写方程式;
(3)NO2能溶于浓硫酸,NO2与无水氯化钙不反应;Pb(NO3)2加热分解生成NO2和PbO、O2.
解答 解:(1)实验一:将制得的纯净的NO2通入浓硫酸中,溶液变成棕黄色,加热浓硫酸,气体逸出,溶液颜色褪去,说明NO2溶于浓硫酸但不与浓硫酸反应;
实验二:将制得的纯净的NO通过浓硫酸后用排水集气法收集到足量无色气体,通入氧气后气体变成红棕色,说明NO不溶于浓硫酸也不与浓硫酸反应;
故答案为:NO2溶于浓硫酸但不与浓硫酸反应,NO不溶于浓硫酸也不与浓硫酸反应;
(2)NO、NO2等体积通入浓硫酸中反应生成NOHSO4,由原子守恒书写出方程式为NO+NO2+2H2SO4=2NOHSO4+H2O;
故答案为:NO+NO2+2H2SO4=2NOHSO4+H2O;
(3)能溶于浓硫酸,所以不能用浓硫酸干燥NO2,NO2与无水氯化钙不反应,所以可以用无水氯化钙干燥NO2;Pb(NO3)2加热分解生成NO2和PbO、O2,反应方程式为:2Pb(NO3)2$\frac{\underline{\;加热\;}}{\;}$2PbO+4NO2↑+O2↑;
故答案为:无水氯化钙;2Pb(NO3)2$\frac{\underline{\;加热\;}}{\;}$2PbO+4NO2↑+O2↑.
点评 本题考查了氮的氧化物的性质、干燥剂的选择、化学方程式等,题目难度中等,侧重于考查学生的分析能力和对题中信息的应用能力.

练习册系列答案
 学期复习一本通学习总动员期末加暑假延边人民出版社系列答案
学期复习一本通学习总动员期末加暑假延边人民出版社系列答案 芒果教辅暑假天地重庆出版社系列答案
芒果教辅暑假天地重庆出版社系列答案
相关题目
2.设NA为阿伏加德罗常数的值.下列说法正确的是( )
| A. | 17g羟基与17g NH3所含电子数均为10NA | |
| B. | lmolCl2溶于水转移电子数为NA | |
| C. | 1L0.1mol•L-1 NH4 HC03溶液中所含NH4+数为0.1NA | |
| D. | 标准状况下,11.2LN2和02混合气体中所含分子数为0.5NA |
20.硫酸亚铁铵又称莫尔盐,是浅绿色晶体.它在空气中比一般亚铁盐稳定,是常用的Fe2+试剂.某实验小组利用工业废铁屑制取莫尔盐,并测定其纯度.
已知:
①
②莫尔盐在乙醇溶剂中难溶.
Ⅰ.莫尔盐的制取

试分析:
(1)步骤2中加热方式 (填“直接加热”“水浴加热”或“沙浴”);必须在铁屑少量剩余时,进行热过滤,其原因是防止Fe2+被氧化,同时热过滤可防止硫酸亚铁以晶体形式析出.
(2)步骤3中包含的实验操作名称加热浓缩、冷却结晶.
(3)产品莫尔盐最后用b洗涤(填字母编号).
a.蒸馏水 b.乙醇 c.滤液
Ⅱ.为测定硫酸亚铁铵(NH4)2SO4FeSO46H2O晶体纯度,某学生取m g硫酸亚铁铵样品配制成500mL溶液,根据物质组成,甲、乙、丙三位同学设计了如下三个实验方案,请回答:
(甲)方案一:取20.00mL硫酸亚铁铵溶液用0.1000molL -1的酸性KMnO4溶液分三次进行滴定.
(乙)方案二:取20.00mL硫酸亚铁铵溶液进行如下实验.

(1)若实验操作都正确,但方案一的测定结果总是小于方案二,其可能原因为Fe2+已被空气部分氧化,验证推测的方法为:取少量硫酸亚铁铵溶液,加入少量KSCN溶液,若溶液变为血红色,说明Fe2+已被空气部分氧化.
(丙)方案三:(通过NH 4+测定)实验设计图如下所示.取20.00mL硫酸亚铁铵溶液进行该实验.

(2)①装置乙(填“甲”或“乙”)较为合理,判断理由是甲装置会出现倒吸.量气管中最佳试剂是 (填字母编号.如选“乙”则填此空,如选“甲”此空可不填).
a.水 b.饱和NaHCO3溶液 c.CCl4
②若测得NH3的体积为V L(已折算为标准状况下),则该硫酸亚铁铵晶体的纯度为$\frac{392V×25}{44.8m}$×100%.
已知:
①
 | 10 | 20 | 30 | 40 | 50 | 70 |
| (NH4)2SO4 | 73.3 | 75.4 | 78.0 | 81.0 | 84.5 | 91.9 |
| FeSO4•7H2O | 40.0 | 48.0 | 60.0 | 73.3 | - | - |
| (NH4)2SO4•FeSO4•6H2O | 18.1 | 21.2 | 24.5 | 27.9 | 31.3 | 38.5 |
Ⅰ.莫尔盐的制取

试分析:
(1)步骤2中加热方式 (填“直接加热”“水浴加热”或“沙浴”);必须在铁屑少量剩余时,进行热过滤,其原因是防止Fe2+被氧化,同时热过滤可防止硫酸亚铁以晶体形式析出.
(2)步骤3中包含的实验操作名称加热浓缩、冷却结晶.
(3)产品莫尔盐最后用b洗涤(填字母编号).
a.蒸馏水 b.乙醇 c.滤液
Ⅱ.为测定硫酸亚铁铵(NH4)2SO4FeSO46H2O晶体纯度,某学生取m g硫酸亚铁铵样品配制成500mL溶液,根据物质组成,甲、乙、丙三位同学设计了如下三个实验方案,请回答:
(甲)方案一:取20.00mL硫酸亚铁铵溶液用0.1000molL -1的酸性KMnO4溶液分三次进行滴定.
(乙)方案二:取20.00mL硫酸亚铁铵溶液进行如下实验.

(1)若实验操作都正确,但方案一的测定结果总是小于方案二,其可能原因为Fe2+已被空气部分氧化,验证推测的方法为:取少量硫酸亚铁铵溶液,加入少量KSCN溶液,若溶液变为血红色,说明Fe2+已被空气部分氧化.
(丙)方案三:(通过NH 4+测定)实验设计图如下所示.取20.00mL硫酸亚铁铵溶液进行该实验.

(2)①装置乙(填“甲”或“乙”)较为合理,判断理由是甲装置会出现倒吸.量气管中最佳试剂是 (填字母编号.如选“乙”则填此空,如选“甲”此空可不填).
a.水 b.饱和NaHCO3溶液 c.CCl4
②若测得NH3的体积为V L(已折算为标准状况下),则该硫酸亚铁铵晶体的纯度为$\frac{392V×25}{44.8m}$×100%.
7.甲醇是基本化工原料,甲醇及其可制得产品的沸点如下.
(1)在425℃、A12O3作催化剂,甲醇与氨气反应可以制得二甲胺,二甲胺显弱碱性,与盐酸反应生成(CH3)2NH2Cl,溶液中各离子浓度由大到小的顺序为c(Cl-)>c[(CH3)2NH2+]>c(H+)>c(OH-);
(2)甲醇合成二甲基甲酰胺的化学方程式为:2CH3OH+NH3+CO?(CH3)2NCHO+2H2O△H若该反应在常温下能自发进行,则该反应为放热反应(填“吸热”、“放热”).
(3)甲醇制甲醚的化学方程式为:2CH3OH?CH3OCH3+H2O△H.一定温度下,在三个体积均为1.0L 的恒容密闭容器中发生该反应.
①x/y=$\frac{1}{2}$;
②已知387℃时该反应的化学平衡常数K=4.若起始时向容器I中充入0.1mol CH3OH、0.15mol CH3OCH3和0.10mol H2O,则此时v正>v逆(填“>”、“<”或“=”)
(4)以甲醇为主要原料,电化学合成碳酸二甲酯工作原理如图所示.
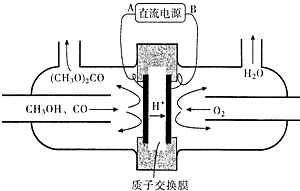
写出阳极的电极反应式2CH3OH+CO-2e-=(CH3O)2CO+2H+.
| 名称 | 甲醇 | 二甲胺 | 二甲基甲酰胺 | 甲醚 | 碳酸二甲酯 |
| 结构式 | CH3OH | (CH3)2NH | (CH3)2NCHO | CH3OCH | (CH3O)2CO |
| 沸点(℃) | 64.7 | 7.4 | 153℃ | -24.9 | 90℃ |
(2)甲醇合成二甲基甲酰胺的化学方程式为:2CH3OH+NH3+CO?(CH3)2NCHO+2H2O△H若该反应在常温下能自发进行,则该反应为放热反应(填“吸热”、“放热”).
(3)甲醇制甲醚的化学方程式为:2CH3OH?CH3OCH3+H2O△H.一定温度下,在三个体积均为1.0L 的恒容密闭容器中发生该反应.
| 容器编号 | 温度/℃ | 起始物质的量/mol | 平衡物质的量/mol | |
| CH3OH | CH3OCH3 | H2O | ||
| Ⅰ | 387 | 0.20 | x | |
| Ⅱ | 387 | 0.40 | y | |
| Ⅲ | 207 | 0.20 | 0.090 | 0.090 |
②已知387℃时该反应的化学平衡常数K=4.若起始时向容器I中充入0.1mol CH3OH、0.15mol CH3OCH3和0.10mol H2O,则此时v正>v逆(填“>”、“<”或“=”)
(4)以甲醇为主要原料,电化学合成碳酸二甲酯工作原理如图所示.

写出阳极的电极反应式2CH3OH+CO-2e-=(CH3O)2CO+2H+.
17.下表是元素周期表的一部分,针对表中的①~⑨种元素,填写下列空白:
(1)这些元素中,化学性质最不活泼的是Ar(填元素符号,下同).
(2)最高价氧化物的水化物中,酸性最强的化合物的化学式:HClO4,碱性最强的化合物的电子式: .
.
(3)最高价氧化物是两性氧化物的元素是Al.
(4)用电子式表示元素④与⑥形成化合物的过程: .
.
(5)①与⑦形成的化合物的电子式: ,该化合物是由极性(填“极性”或“非极性”)共价键形成的.
,该化合物是由极性(填“极性”或“非极性”)共价键形成的.
| 主族 周期 | ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | 0族 |
| 2 | ① | ② | ③ | |||||
| 3 | ④ | ⑤ | ⑥ | ⑦ | ⑧ | |||
| 4 | ⑨ |
(2)最高价氧化物的水化物中,酸性最强的化合物的化学式:HClO4,碱性最强的化合物的电子式:
 .
.(3)最高价氧化物是两性氧化物的元素是Al.
(4)用电子式表示元素④与⑥形成化合物的过程:
 .
.(5)①与⑦形成的化合物的电子式:
 ,该化合物是由极性(填“极性”或“非极性”)共价键形成的.
,该化合物是由极性(填“极性”或“非极性”)共价键形成的.
4.下列图象正确的是( )
| A. | 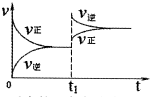 反应的正方向放热(t1时升温) | |
| B. | 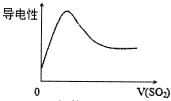 SO2气体通入氯水中 | |
| C. | 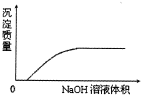 NaOH溶液滴加Ca(HCO3)2溶液中 | |
| D. | 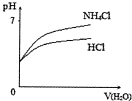 将PH相同的NH4Cl溶液和稀盐酸稀释时PH的变化 |
1.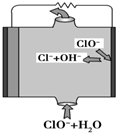 镁燃料电池具有比能量高、使用安全方便、原材料来源丰富、成本低等特点.一般研究的镁燃料电池可分为镁空气燃料电池、镁海水燃料电池、镁过氧化氢燃料电池和镁次氯酸盐燃料电池.其中,镁次氯酸盐燃料电池的工作原理如图所示,下列有关说法不正确的是( )
镁燃料电池具有比能量高、使用安全方便、原材料来源丰富、成本低等特点.一般研究的镁燃料电池可分为镁空气燃料电池、镁海水燃料电池、镁过氧化氢燃料电池和镁次氯酸盐燃料电池.其中,镁次氯酸盐燃料电池的工作原理如图所示,下列有关说法不正确的是( )
 镁燃料电池具有比能量高、使用安全方便、原材料来源丰富、成本低等特点.一般研究的镁燃料电池可分为镁空气燃料电池、镁海水燃料电池、镁过氧化氢燃料电池和镁次氯酸盐燃料电池.其中,镁次氯酸盐燃料电池的工作原理如图所示,下列有关说法不正确的是( )
镁燃料电池具有比能量高、使用安全方便、原材料来源丰富、成本低等特点.一般研究的镁燃料电池可分为镁空气燃料电池、镁海水燃料电池、镁过氧化氢燃料电池和镁次氯酸盐燃料电池.其中,镁次氯酸盐燃料电池的工作原理如图所示,下列有关说法不正确的是( )| A. | 放电过程中OH-移向正极 | |
| B. | 电池的总反应式为Mg+ClO-+H2O═Mg(OH)2+Cl- | |
| C. | 镁燃料电池中镁均为负极,发生氧化反应 | |
| D. | 镁过氧化氢燃料电池,酸性电解质中正极反应式为H2O2+2H++2e-═2H2O |
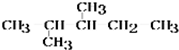
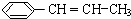 )在催化剂作用下生成聚苯丙烯的反应方程式:
)在催化剂作用下生成聚苯丙烯的反应方程式: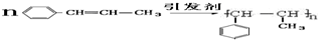
 +3HNO3$→_{△}^{浓硫酸}$
+3HNO3$→_{△}^{浓硫酸}$ +3H2O.
+3H2O.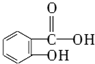 ,俗名水杨酸.
,俗名水杨酸. .
.