题目内容
 洋蓟素是一种新结构类型的抗乙型肝炎病毒和抗艾滋病病毒的化合物,其结构如图所示,有关洋蓟素的说法正确的是(连四个不同基团的碳属于手性碳)( )
洋蓟素是一种新结构类型的抗乙型肝炎病毒和抗艾滋病病毒的化合物,其结构如图所示,有关洋蓟素的说法正确的是(连四个不同基团的碳属于手性碳)( )| A、分子中含有6个手性碳原子 |
| B、一定条件下能发生酯化反应和消去反应 |
| C、不能与氯化铁溶液发生显色反应 |
| D、1 mol洋蓟素最多可与11 mol NaOH反应 |
考点:有机物的结构和性质
专题:有机物的化学性质及推断
分析:洋蓟素中含有的官能团有酚羟基、酯基、羟基、羧基、碳碳双键,所以应具有烯烃、酚、醇、酯、羧酸的性质,根据结构判断其性质.
解答:
解:A.有机物中共含有4个手性碳原子,如图所示 ,故A错误;
,故A错误;
B.该分子中含有醇羟基和羧基,所以一定条件下能发生酯化反应;因为含有醇羟基,且醇羟基的邻位的碳原子上有氢原子,所以还可以发生消去反应,故B正确;
C.该分子中含有酚羟基,所以应具有酚的性质,能和氯化铁发生显色反应,故C错误;
D.4mol酚羟基需4molNaOH,2mol酯基需2molNaOH,1mol羧基需1molNaOH,共需7molNaOH,故D错误.
故选B.
 ,故A错误;
,故A错误;B.该分子中含有醇羟基和羧基,所以一定条件下能发生酯化反应;因为含有醇羟基,且醇羟基的邻位的碳原子上有氢原子,所以还可以发生消去反应,故B正确;
C.该分子中含有酚羟基,所以应具有酚的性质,能和氯化铁发生显色反应,故C错误;
D.4mol酚羟基需4molNaOH,2mol酯基需2molNaOH,1mol羧基需1molNaOH,共需7molNaOH,故D错误.
故选B.
点评:本题考查有机物结构和性质,侧重于有机物结构和性质的综合应用,为高考常见题型,注意把握有机物的结构特点和官能团的性质,为解答该题的关键,题目难度不大.

练习册系列答案
相关题目
下列物质在一定条件下,可与CH4发生取代反应的是( )
| A、氧气 |
| B、溴水 |
| C、氯气 |
| D、酸性KMnO4溶液 |
Al与重氢氧化钠(NaOD)的水溶液反应,其中水中不含重氢.下列说法正确的是( )
| A、生成的氢气中只含有H2 |
| B、生成的氢气中只含有D2 |
| C、生成的氢气中含有H2、HD、D2 |
| D、以上判断都不正确 |
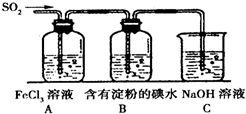 为探究SO2气体的还原性某兴趣小组设计了如装置图:
为探究SO2气体的还原性某兴趣小组设计了如装置图: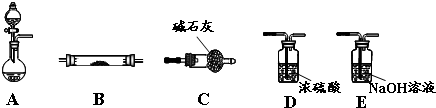

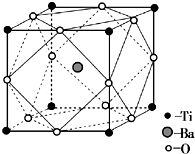 钛被誉为“未来世纪的金属”.试回答下列问题:
钛被誉为“未来世纪的金属”.试回答下列问题: