题目内容
7.下列说法正确的是( )| A. | 液态HCl、固体NaCl均不导电,所以HCl、NaCl均不是电解质 | |
| B. | SO2的水溶液能导电,所以SO2是电解质 | |
| C. | 蔗糖、酒精在水溶液里和熔融状态时均不导电,所以他们不是电解质 | |
| D. | 铜、石墨均导电,所以它们是电解质 |
分析 在水溶液里或熔融状态下能导电的化合物是电解质,在水溶液和熔融状态下都不能导电的化合物为非电解质,无论电解质和非电解质,都一定为化合物,单质和混合物一定不是电解质和非电解质,据此进行解答.
解答 解:A、液态HCl、固体NaCl溶于水得到的溶液均能导电,因此HCl、NaCl均是电解质,故A错误;
B、SO2的水溶液导电的原因是SO2与水反应生成的亚硫酸电离出的离子,不是SO2本身电离的离子,因此SO2属于非电解质,故B错误;
C、在水溶液和熔融状态下都不能导电的化合物为非电解质,因此蔗糖和酒精属于非电解质,故C正确;
D、铜、石墨属于单质,既不是电解质也不是非电解质,故D错误.
故选C.
点评 本题考查了电解质与非电解质的判断,题目难度不大,注意掌握电解质与非电解质的概念及区别,明确电解质、非电解质都一定为化合物,质和混合物一定不是电解质和非电解质.

练习册系列答案
相关题目
4.根据生活经验,下列物质pH大小正确的是( )
| A. | 白醋>酱油 | B. | 84消毒液>肥皂水 | ||
| C. | 人体胃液>人体血液 | D. | 厕所清洁剂>厨房清洁剂 |
5.现将2mol气体A与1mol气体B充入一个体积不变的容器内,发生反应:2A+B?C+3D+4E,达到平衡后气体A的浓度减少一半,发现少量液滴生成,在相同的温度下测得反应前后压强分别为6.06×106Pa和8.08×106Pa,又测得反应共放出热量QkJ,下列说法正确的是( )
| A. | 上述反应达到平衡后,其他的条件不变的情况下,升高温度,压强一定增大 | |
| B. | 在上述平衡体系中再加入1molA和0.5molB,平衡正向移动,A的转化率增大 | |
| C. | 该反应的热化学方程式2A(g)+B(g)?C(g)+3D(l)+4E(g)△H=-QkJ/mol | |
| D. | 该反应在任何温度下都可自发进行 |
15. 一定温度下,将1mol A和1mol B气体充入2L恒容密闭容器,发生反应:
一定温度下,将1mol A和1mol B气体充入2L恒容密闭容器,发生反应:
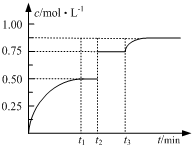
A(g)+B(g)?2C(g)+D(s)t1时达到平衡.在t2、t3时刻分别改变反应的一个条件,测得容器中气体C的浓度随时间变化如图所示.下列说法正确的是( )
 一定温度下,将1mol A和1mol B气体充入2L恒容密闭容器,发生反应:
一定温度下,将1mol A和1mol B气体充入2L恒容密闭容器,发生反应:A(g)+B(g)?2C(g)+D(s)t1时达到平衡.在t2、t3时刻分别改变反应的一个条件,测得容器中气体C的浓度随时间变化如图所示.下列说法正确的是( )
| A. | 若t1=2,则反应在0~2 min内的平均速率为v(A)=0.50 mol•(L•min)-1 | |
| B. | 若t3时刻升高了温度,则该反应的△H>0 | |
| C. | 若t1时刻后向体系中加入A、B、C各1 mol,则υ(正)>υ(逆) | |
| D. | 温度不变,若起始向容器中加入1 mol A、1 mol B、2 mol D,则达平衡时A的转化率小于50% |
12.在空气中能稳定存在的物质是( )
| A. | 石灰水 | B. | 氯水 | C. | 次氯酸钠 | D. | 食盐水 |
19.在蒸发皿中加热蒸干并灼烧下列物质的溶液,可以得到该物质固体的是( )
| A. | 硝酸铝 | B. | 碳酸氢钠 | C. | 硫酸镁 | D. | 亚硫酸钠 |
16.药物是人类抵御疾病的重要武器之一.下列有关药物的说法不正确的是( )
| A. | “胃得乐”(主要成分为碳酸镁)是一种抗酸药) | |
| B. | 鸦片、吗啡、海洛因等这些物质属于毒品 | |
| C. | 青霉素能抑制细菌细胞壁的生长,致使细菌因细胞破裂而死亡 | |
| D. | “阿司匹林”是一种重要的抗生素 |
17.NaHS、MgSO4、NaHSO4三种物质组成的混合物中,己知氧元素的质量分数为a%,则其中硫元素的质量分数为( )
| A. | a% | B. | 1-1.75% | C. | 4(l-a%)7 | D. | 3(l-a%)7 |
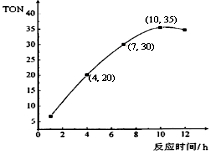 甲醇和CO2可直接合成DMC:2CH3OH(g)+CO2 (g)?CH3OCOOCH3 (g)+H2O(g),但甲醇转化率通常不会超过1%,制约该反应走向工业化生产.
甲醇和CO2可直接合成DMC:2CH3OH(g)+CO2 (g)?CH3OCOOCH3 (g)+H2O(g),但甲醇转化率通常不会超过1%,制约该反应走向工业化生产.