题目内容
12.四种短周期元素在周期表中的相对位置如表所示,其中 Z 元素原子核外电子总数是其 最外层电子数的 3 倍.下列说法中不正确的是( )| X | Y | |
| Z | W |
| A. | X、Y 均能形成不止一种氢化物 | |
| B. | YO 2是一种有毒气体,属于酸性氧化物 | |
| C. | Y 的最简单氢化物比 Z 的稳定性更强 | |
| D. | XW2中各原子最外层均达到 8e-稳定结构 |
分析 X、Y、Z、W均为短周期主族元素,由位置关系可知,X、Y处于第二周期,Z、W处于第三周期,Z元素原子核外电子总数是其最外层电子数的3倍,
设核外最外层电子数为x,
则有(2+8+x)=3x,
解得x=5,
则Z为P元素,故X为C元素、Y为N元素、W为S元素,以此解答该题.
解答 解:由以上分析可知X为C元素、Y为N元素、Z为P元素,W为S元素,
A.C与H可形成烃类混合物,N与H可形成NH3、N2H4等,故A正确;
B.NO2与水反应不仅仅生成硝酸,还生成NO,不是酸性氧化物,故B错误;
C.非金属性Y>Z,则Y 的最简单氢化物比 Z 的稳定性更强,故C正确;
D.CS2结构类似二氧化碳,各原子最外层均达到 8e-稳定结构,故D正确.
故选B.
点评 本题考查结构性质位置关系应用,为高频考点,侧重考查学生的分析能力,难度不大,根据位置判断元素所处的周期是推断关键,注意掌握元素周期表的结构与元素周期律.

练习册系列答案
相关题目
3.关于下列各装置图的叙述不正确的是( )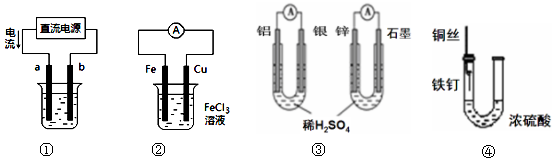

| A. | 用装置①精炼铜,则a极为粗铜,b为精铜,电解质溶液为CuSO4溶液 | |
| B. | 装置②的总反应是:Cu+2Fe3+=Cu2++2Fe2+ | |
| C. | 图③两个装置中通过导线的电子数相同时,消耗负极材料的物质的量不同 | |
| D. | 装置④中的铁钉几乎没被腐蚀 |
20.室温下,H2+Cl2$\stackrel{点燃}{→}$2HCl 生成 0.1mol HCl,下列说法正确的是( )
| A. | 生成 0.1 NA 根共价键 | B. | 消耗反应物总体积 2.24L | ||
| C. | 转移了 2 NA 个电子 | D. | 产物溶于水后,溶液 pH=1 |
7.以下关于中国化学史的表述错误的是( )
| A. | 杜康用高粱酿酒的原理是通过蒸馏法将高粱中的乙醇分离出来 | |
| B. | 蔡伦利用树皮、碎布(麻布)、麻头等原料精制出优质纸张 | |
| C. | 《本草纲目》中记载“(火药)乃焰消(KNO3)、硫磺、杉木炭所合,以为烽燧铳机诸药者”这是利用了KNO3的氧化性 | |
| D. | 英文的“中国”(China)又指“瓷器”,说明我国很早就应用化学技术制作陶瓷 |
17.下列有关实验能成功的是( )
| A. | 苯加到溴水中,将会和溴发生取代反应而使溴水褪色 | |
| B. | 用冷却结晶法来提纯含少量KCl杂质的KNO3晶体 | |
| C. | 将10%的葡萄糖溶液加到新制氢氧化铜悬浊液中,出现砖红色沉淀 | |
| D. | 进行淀粉水解实验时,为检验水解产物和水解程度,加液顺序为淀粉溶液→H2SO4溶液→NaOH溶液→碘水→新制Cu(OH)2悬浊液 |
4.下列叙述正确的是( )
| A. | 在中和热测定实验中,将碱缓慢倒入酸中,以确保酸碱充分反应 | |
| B. | 为除去蛋白质溶液中混有的(NH4)2SO4,将混合物装入半透膜袋,并放入流动的蒸馏水中 | |
| C. | 用排水集气法收集气体,能验证铜与稀硝酸的反应产物是NO | |
| D. | 向硝酸银溶液中先滴加少量氯化钠溶液,再加少量硫化钾溶液,试管中先有白色沉淀,后有黑色沉淀,则AgCl的溶解度大于Ag2S |
1.根据要求回答下列问题
(1)T0C时,向一容积为2升的密闭容器中充入2molA、0.6molC和一定量的B三种气体,一定条件下发生反应.其相关信息如下:图1中t0~t1阶段c(B)未画出;图2中t2、t3、t4改变的条件是温度、压强、催化剂中的一种
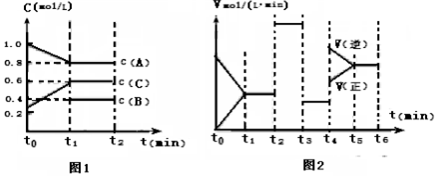
①B的起始物质的量为1mol;t2时刻改变的条件是加催化剂
②图2中各阶段平衡时对应的平衡常数如表所示:
K2> K4(填“>或<或.=”);其理由是t2-t4 平衡未移动,从图象知K4是温度升高平衡逆向移动后的常数,所以变小
③T0C时,该反应的平衡常数是0.84(保留两位小数);维持温度不变,在t1时刻再向该容器中加入1molA,0.5molB,0.3molC,重新达平衡后α(A)=20%
(2)硅是重要的半导体材料.工业上由粗制纯硅的过程如下:
Si(粗)$→_{460℃}^{Cl_{2}}$SiCl4$\stackrel{蒸馏}{→}$SiCl4(纯)$→_{1100℃}^{H_{2}}$Si(纯)
实验测得上述由SiCl4制纯硅的反应中,测得每生成1.12kg纯硅(Si的相对原子质量为28)需吸收aKJ热量,则该反应的热化学方程式SiCl4(g)+2H2(g)=Si(s)+4HCl(g)△=+Q/40 KJ/mol.
(1)T0C时,向一容积为2升的密闭容器中充入2molA、0.6molC和一定量的B三种气体,一定条件下发生反应.其相关信息如下:图1中t0~t1阶段c(B)未画出;图2中t2、t3、t4改变的条件是温度、压强、催化剂中的一种

①B的起始物质的量为1mol;t2时刻改变的条件是加催化剂
②图2中各阶段平衡时对应的平衡常数如表所示:
| 时间段 | t1~t2 | t2~t3 | t3~t4 | t5~t6 |
| 平衡常数 | K1 | K2 | K3 | K4 |
③T0C时,该反应的平衡常数是0.84(保留两位小数);维持温度不变,在t1时刻再向该容器中加入1molA,0.5molB,0.3molC,重新达平衡后α(A)=20%
(2)硅是重要的半导体材料.工业上由粗制纯硅的过程如下:
Si(粗)$→_{460℃}^{Cl_{2}}$SiCl4$\stackrel{蒸馏}{→}$SiCl4(纯)$→_{1100℃}^{H_{2}}$Si(纯)
实验测得上述由SiCl4制纯硅的反应中,测得每生成1.12kg纯硅(Si的相对原子质量为28)需吸收aKJ热量,则该反应的热化学方程式SiCl4(g)+2H2(g)=Si(s)+4HCl(g)△=+Q/40 KJ/mol.
2.除去FeCl2溶液中的FeCl3所需试剂是( )
| A. | Cl2 | B. | Cu | C. | Fe | D. | NaOH |
 .
.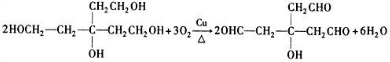 .
.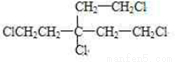 .
.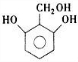 、
、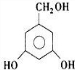 .
.