题目内容
12.2015年10月5日,诺贝尔奖官方推特消息,中国女药学家屠呦呦因创制新型抗疟药---青蒿素和双氢青蒿素 的贡献而获得诺贝尔生理学或医学奖.青蒿素结构简式如图,下列有关叙述正确的是( )
| A. | 青蒿素极易溶于水 | |
| B. | 1 mol青蒿素与足量NaOH溶液反应最多消耗4 mol NaOH | |
| C. | 青蒿素含有过氧键,有较强氧化性 | |
| D. | 青蒿素分子式为C15H21O5 |
分析 由结构简式可知分子式,含-COOC-、醚键及过氧键,结合酯、过氧化物的性质来解答.
解答 解:A.青蒿素含有酯基,难溶于水,故A错误;
B.只有酯基能与氢氧化钠发生反应,1 mol青蒿素与足量NaOH溶液反应最多消耗1 mol NaOH,故B错误;
C.青蒿素含有过氧键,具有过氧化氢的性质,有较强氧化性,故C正确;
D.由结构简式可知青蒿素的分子式为C15H22O5,故D错误.
故选C.
点评 本题考查有机物的结构与性质,为高频考点,把握官能团与性质的关系为解答的关键,侧重酯、酚性质的考查,题目难度中等.

练习册系列答案
相关题目
2. 室温时,向100mL0.1mol/LNH4HSO4溶液中滴加0.1mol/LNaOH溶液,溶液pH与NaOH溶液体积的关系曲线如图所示:对图中a、b、c、d四个点分析中,正确的是( )
室温时,向100mL0.1mol/LNH4HSO4溶液中滴加0.1mol/LNaOH溶液,溶液pH与NaOH溶液体积的关系曲线如图所示:对图中a、b、c、d四个点分析中,正确的是( )
 室温时,向100mL0.1mol/LNH4HSO4溶液中滴加0.1mol/LNaOH溶液,溶液pH与NaOH溶液体积的关系曲线如图所示:对图中a、b、c、d四个点分析中,正确的是( )
室温时,向100mL0.1mol/LNH4HSO4溶液中滴加0.1mol/LNaOH溶液,溶液pH与NaOH溶液体积的关系曲线如图所示:对图中a、b、c、d四个点分析中,正确的是( )| A. | a点水的电离程度最大 | B. | b点c(NH4+)=2c(SO42-) | ||
| C. | c点c(NH4+)+c(NH3•H2O)=c(Na+) | D. | d点c(NH4+)+c(Na+)=c(SO42-)+c(OH-) |
3.O3氧化海水中的I-是大气中碘的主要来源,将O3通入稀硫酸酸化的NaI溶液中进行模拟研究.
(1)为探究外界条件对I2生成速率的影响,做了如下三组实验,填写表中的空白处.
(2)为测定生成I2的量,用移液管取20.00mL反应后溶液于锥形瓶中,用 c mol•L-1的Na2S2O3标准液滴定,消耗V mLNa2S2O3溶液.
已知:①H2S2O3是一种弱酸;②2Na2S2O3+I2═Na2S4O6+2NaI
①该滴定实验中除烧杯、锥形瓶外,还需要的玻璃仪器是碱式滴定管;
②该实验中可选用淀粉(填物质名称)作指示剂.
③反应后溶液中碘的含量为6.35cVg•L-1.
④甲同学认为在滴定前应微热溶液,以排除溶液中溶解的O3和O2,不然会使滴定结果偏高(填“低”或“高”).
(1)为探究外界条件对I2生成速率的影响,做了如下三组实验,填写表中的空白处.
| 编号 | 实验目的 | 反应物 | 反应前 溶液的pH | 温度 |
| 1 | 对照组 | O3+NaI+H2SO4 | 5.2 | 25℃ |
| 2 | ①探究FeCl2对反应速率的影响 | O3+NaI+H2SO4+FeCl2 | 5.2 | 25℃ |
| 3 | 探究温度对反应速率的影响 | O3+NaI+H2SO4 | ②5.2 | 5℃ |
已知:①H2S2O3是一种弱酸;②2Na2S2O3+I2═Na2S4O6+2NaI
①该滴定实验中除烧杯、锥形瓶外,还需要的玻璃仪器是碱式滴定管;
②该实验中可选用淀粉(填物质名称)作指示剂.
③反应后溶液中碘的含量为6.35cVg•L-1.
④甲同学认为在滴定前应微热溶液,以排除溶液中溶解的O3和O2,不然会使滴定结果偏高(填“低”或“高”).
7.已知: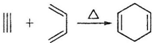 ,如果合成
,如果合成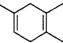 ,所用原始原料可以是( )
,所用原始原料可以是( )
 ,如果合成
,如果合成 ,所用原始原料可以是( )
,所用原始原料可以是( )| A. | 3-甲基-l,3-丁二烯和3-丁炔 | B. | 1,3-戊二烯和2-丁炔 | ||
| C. | 2,3-二甲基-1,3-戊二烯和乙炔 | D. | 2,3-二甲基-l,3-丁二烯和丙炔 |
4.某元素原子的核电荷数是电子层数的5倍,其质子数是最外层电子数的3倍,该元素的元素符号可能是( )
| A. | N | B. | Ne | C. | P | D. | C |
1.环己酮是一种重要的有机化工原料.实验室合成环己酮的反应如图1:
环己醇和环己酮的部分物理性质见下表:
现以20mL环己醇与足量Na2Cr2O7和硫酸的混合液充分反应,制得主要含环己酮和水的粗产品,然后进行分离提纯.其主要步骤有(未排序):
a.蒸馏、除去乙醚后,收集151℃~156℃馏分
b.水层用乙醚(乙醚沸点34.6℃,易燃烧)萃取,萃取液并入有机层
c.过滤
d.往液体中加入NaCl固体至饱和,静置,分液
e.加入无水MgSO4固体,除去有机物中少量水
回答下列问题:
(1)上述分离提纯步骤的正确顺序是dbeca.
(2)b中水层用乙醚萃取的目的是使水层中少量的有机物进一步被提取,提高产品的产量.
(3)以下关于萃取分液操作的叙述中,不正确的是ABC.
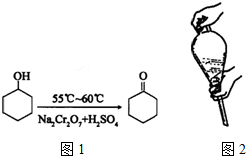
A.水溶液中加入乙醚,转移至分液漏斗,塞上玻璃塞,如图2用力振荡
B.振荡几次后需打开分液漏斗上口的玻璃塞放气
C.经几次振荡并放气后,手持分漏斗静置液体分层
D.分液时,需先将上口玻璃塞打开或玻璃塞上的凹槽对准漏斗上的小孔,再打开旋塞,待下层液体全部流尽时,再从上口倒出上层液体
(4)在上述操作d中,加入NaCl固体的作用是降低环己酮的溶解度;增加水层的密度,有利于分层.蒸馏除乙醚的操作中,采用的加热方式为水浴加热.
(5)蒸馏操作时,一段时间后发现未通冷凝水,应采取的正确方法是停止加热,冷却后通自来水.
(6)恢复至室温时,分离得到纯产品体积为12mL,则环己酮的产率约是60%(保留两位有效数字).

环己醇和环己酮的部分物理性质见下表:
| 物质 | 相对分子质量 | 沸点(℃) | 密度(g•cm-3、20℃) | 溶解性 |
| 环己醇 | 100 | 161.1 | 0.9624 | 能溶于水和醚 |
| 环己酮 | 98 | 155.6 | 0.9478 | 微溶于水,能溶于醚 |
a.蒸馏、除去乙醚后,收集151℃~156℃馏分
b.水层用乙醚(乙醚沸点34.6℃,易燃烧)萃取,萃取液并入有机层
c.过滤
d.往液体中加入NaCl固体至饱和,静置,分液
e.加入无水MgSO4固体,除去有机物中少量水
回答下列问题:
(1)上述分离提纯步骤的正确顺序是dbeca.
(2)b中水层用乙醚萃取的目的是使水层中少量的有机物进一步被提取,提高产品的产量.
(3)以下关于萃取分液操作的叙述中,不正确的是ABC.
A.水溶液中加入乙醚,转移至分液漏斗,塞上玻璃塞,如图2用力振荡
B.振荡几次后需打开分液漏斗上口的玻璃塞放气
C.经几次振荡并放气后,手持分漏斗静置液体分层
D.分液时,需先将上口玻璃塞打开或玻璃塞上的凹槽对准漏斗上的小孔,再打开旋塞,待下层液体全部流尽时,再从上口倒出上层液体
(4)在上述操作d中,加入NaCl固体的作用是降低环己酮的溶解度;增加水层的密度,有利于分层.蒸馏除乙醚的操作中,采用的加热方式为水浴加热.
(5)蒸馏操作时,一段时间后发现未通冷凝水,应采取的正确方法是停止加热,冷却后通自来水.
(6)恢复至室温时,分离得到纯产品体积为12mL,则环己酮的产率约是60%(保留两位有效数字).
2.在120℃时,某气态烃和CH4的混合气体10L,在足量90LO2中充分燃烧又恢复到120℃,测得气体体积为100L.则该气态烃可能为( )
| A. | C2H2 | B. | C2H4 | C. | C3H8 | D. | C2H6 |

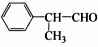 ,工业合成路线如下:
,工业合成路线如下: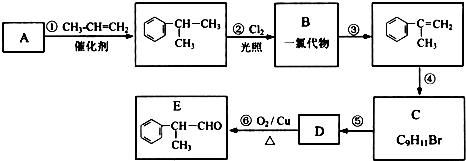
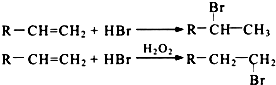 (R-代表烃基)
(R-代表烃基) 或
或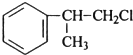 (任写一个),其官能团为氯原子.
(任写一个),其官能团为氯原子.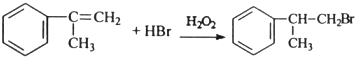 (必须有反应条件).
(必须有反应条件). .
.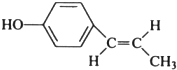 (只写反式结构).
(只写反式结构).