题目内容
某研究性学习小组将一定浓度的Na2CO3溶液滴入CuSO4溶液中得到蓝色沉淀.
甲同学认为两者反应只生成CuCO3一种沉淀;
乙同学认为这两者相互促进水解,只生成Cu(OH)2一种沉淀;
丙同学认为生成了CuCO3和Cu(OH)2两种沉淀.
(查阅资料知:CuCO3和Cu(OH)2均不带结晶水)
Ⅰ:按照乙同学的理解,向生成的沉淀中加入 试剂,若观察到 时,
就说明乙同学的猜想正确,则Na2CO3溶液和CuSO4溶液反应的离子方程式: .
Ⅱ:定量探究生成物的成分将沉淀通过 、洗涤的操作从溶液中分离出来,再低温干燥,然后定量分析沉淀物成分.
Ⅲ:若沉淀中CuCO3和Cu(OH)2两者都有,可通过下列所示装置的链接,进行定量分析来测定其质量(设每一装置中的反应或吸收均完全,反应前系统中存在的空气忽略不计).

(1)上述各装置连接顺序为: → → → → →;
(2)实验结束时要通入过量的空气,其作用是 .
(3)若沉淀样品的质量为m克,CO2吸收装置质量增加了n克,则沉淀中Cu(OH)2的质量分数为: .
(4)能证明甲同学说法正确的实验现象是 .
甲同学认为两者反应只生成CuCO3一种沉淀;
乙同学认为这两者相互促进水解,只生成Cu(OH)2一种沉淀;
丙同学认为生成了CuCO3和Cu(OH)2两种沉淀.
(查阅资料知:CuCO3和Cu(OH)2均不带结晶水)
Ⅰ:按照乙同学的理解,向生成的沉淀中加入
就说明乙同学的猜想正确,则Na2CO3溶液和CuSO4溶液反应的离子方程式:
Ⅱ:定量探究生成物的成分将沉淀通过
Ⅲ:若沉淀中CuCO3和Cu(OH)2两者都有,可通过下列所示装置的链接,进行定量分析来测定其质量(设每一装置中的反应或吸收均完全,反应前系统中存在的空气忽略不计).

(1)上述各装置连接顺序为:
(2)实验结束时要通入过量的空气,其作用是
(3)若沉淀样品的质量为m克,CO2吸收装置质量增加了n克,则沉淀中Cu(OH)2的质量分数为:
(4)能证明甲同学说法正确的实验现象是
考点:探究物质的组成或测量物质的含量,性质实验方案的设计
专题:实验探究和数据处理题
分析:Ⅰ.乙同学的认为:这两者相互促进水解反应,生成Cu(OH)2一种沉淀,加入盐酸无气体,则证明乙同学猜想正确;Na2CO3和CuSO4相互促进水解生成氢氧化铜沉淀、硫酸钠和二氧化碳;
Ⅱ.根据固体和液体的分离方法来提纯物质;
Ⅲ.(1)沉淀中CuCO3和Cu(OH)2两者都有,可进行定量分析来测定其质量,反应前系统中存在的空气忽略不计,可以利用装置C除去空气中的水蒸气和二氧化碳,通入后可以把反应生成的水蒸气和二氧化碳赶到后续装置完全吸收,减小实验误差,通过装置B吸收分解生成的水蒸气,通过装置D吸收生成的二氧化碳,装置E避免空气中的水蒸气和二氧化碳进入装置D产生测定误差;
(2)碱石灰可以吸收二氧化碳和水,实验结束时要通入过量的空气排出装置中滞留的H2O和CO2气体,以便完全吸收;
(3)CO2吸收装置质量增加了ng,就碳元素守恒计算得到碳酸铜质量,样品质量减去碳酸铜质量得到氢氧化铜质量,计算样品中含有的质量分数;
(4)CuCO3加热只会生成二氧化碳气体,不会产生水,据此判断.
Ⅱ.根据固体和液体的分离方法来提纯物质;
Ⅲ.(1)沉淀中CuCO3和Cu(OH)2两者都有,可进行定量分析来测定其质量,反应前系统中存在的空气忽略不计,可以利用装置C除去空气中的水蒸气和二氧化碳,通入后可以把反应生成的水蒸气和二氧化碳赶到后续装置完全吸收,减小实验误差,通过装置B吸收分解生成的水蒸气,通过装置D吸收生成的二氧化碳,装置E避免空气中的水蒸气和二氧化碳进入装置D产生测定误差;
(2)碱石灰可以吸收二氧化碳和水,实验结束时要通入过量的空气排出装置中滞留的H2O和CO2气体,以便完全吸收;
(3)CO2吸收装置质量增加了ng,就碳元素守恒计算得到碳酸铜质量,样品质量减去碳酸铜质量得到氢氧化铜质量,计算样品中含有的质量分数;
(4)CuCO3加热只会生成二氧化碳气体,不会产生水,据此判断.
解答:
解:Ⅰ.(1)乙同学的认为:这两者相互促进水解反应,生成Cu(OH)2一种沉淀,加入盐酸无气体,则证明乙同学猜想正确;Na2CO3和CuSO4相互促进水解生成氢氧化铜沉淀、硫酸钠和二氧化碳,离子方程式为:Cu2++CO32-+H2O═Cu(OH)2↓+CO2↑,
故答案为:稀盐酸、无气体产生、Cu2++CO32-+H2O═Cu(OH)2↓+CO2↑;
Ⅱ.将沉淀从溶液中分离出来,采用过滤的办法,将得到的固体物质洗涤干燥可以得到固体物质,故答案为:过滤;
Ⅲ.(1)通过装置的连接,进行定量分析来测定其质量,反应前系统中存在的空气忽略不计,可以利用装置C除去空气中的水蒸气和二氧化碳,通入后可以把反应生成的水蒸气和二氧化碳赶到后续装置完全吸收,减小实验误差,通过装置B吸收分解生成的水蒸气,通过装置D吸收生成的二氧化碳,装置E避免空气中的水蒸气和二氧化碳进入装置D产生测定误差;装置连接顺序为:C、A、B、D、E;
故答案为:C;A;B;D;E;
(2)实验结束时要通入过量的空气排出装置中滞留的H2O和CO2气体,以便完全吸收,故答案为:排出装置中滞留的H2O和CO2气体,以便完全吸收;
(3)若沉淀样品的质量为mg,CO2吸收装置质量增加了ng,CuCO3质量=
×124g/mol,则沉淀中Cu(OH)2的质量分数=
×100%=1-
;
故答案为:1-
.
(4)甲同学认为两者反应生成只有CuCO3一种沉淀,加热只会生成二氧化碳气体,不会产生水,所以B质量不变,D质量增加,可以得出结论,故答案为:B质量不变,D质量增加.
故答案为:稀盐酸、无气体产生、Cu2++CO32-+H2O═Cu(OH)2↓+CO2↑;
Ⅱ.将沉淀从溶液中分离出来,采用过滤的办法,将得到的固体物质洗涤干燥可以得到固体物质,故答案为:过滤;
Ⅲ.(1)通过装置的连接,进行定量分析来测定其质量,反应前系统中存在的空气忽略不计,可以利用装置C除去空气中的水蒸气和二氧化碳,通入后可以把反应生成的水蒸气和二氧化碳赶到后续装置完全吸收,减小实验误差,通过装置B吸收分解生成的水蒸气,通过装置D吸收生成的二氧化碳,装置E避免空气中的水蒸气和二氧化碳进入装置D产生测定误差;装置连接顺序为:C、A、B、D、E;
故答案为:C;A;B;D;E;
(2)实验结束时要通入过量的空气排出装置中滞留的H2O和CO2气体,以便完全吸收,故答案为:排出装置中滞留的H2O和CO2气体,以便完全吸收;
(3)若沉淀样品的质量为mg,CO2吸收装置质量增加了ng,CuCO3质量=
| n |
| 44 |
m-
| ||
| m |
| 31n |
| 11m |
故答案为:1-
| 31n |
| 11m |
(4)甲同学认为两者反应生成只有CuCO3一种沉淀,加热只会生成二氧化碳气体,不会产生水,所以B质量不变,D质量增加,可以得出结论,故答案为:B质量不变,D质量增加.
点评:本题考查了实验方案设计,明确实验原理是解本题关键,结合物质的性质来分析解答,知道常见物质的检验方法、实验装置连接顺序,同时考查学生分析问题、解决问题的能力以及思考问题缜密性,难度中等.

练习册系列答案
相关题目
常温下,用0.1000mol/L的HCl溶液滴定20.00mL 0.1000mol/L NH3?H2O溶液,滴定曲线如下图.下列说法不正确的是( )

| A、①溶液:c(C1-)>c(NH4+)>c(OH-)>c(H+) |
| B、②溶液:c(NH4+)=c(C1-)>c(OH-)=c(H+) |
| C、③溶液:c(H+)>c(NH3?H2O)>c(OH-) |
| D、滴定过程中可能出现:c(NH3?H2O)>c(NH4+)>c(OH-)>c(Cl-)>c(H+) |
生活是化学的源泉,下列有关生活中的化学叙述不正确的是( )
| A、铁强化酱油可通过膳食补充人体所需的铁元素 |
| B、变质的植物油有难闻的特殊气味,是由于植物油发生了水解反应 |
| C、一定浓度的双氧水可用于伤口的消毒 |
| D、蔬菜中含有维生素C,生吃新鲜蔬菜要比熟吃时维生素C的损失大 |
等量镁铝合金粉末分别与下列4种过量的溶液充分反应,放出H2最多的是( )
| A、2mol/L H2SO4溶液 |
| B、3mol/L CuSO4溶液 |
| C、6mol/L KOH溶液 |
| D、3mol/L Ba(OH)2溶液 |

 )是一种重要的有机合成中间体.写出以苯酚、甲苯为基本原料制取该化合物的合成路线流程图.请注意:1.可选用必要的无机原料;2.已知酚羟基一般不易直接与羧酸发生类似酯化的反应,以上C→D的方法可供参照.
)是一种重要的有机合成中间体.写出以苯酚、甲苯为基本原料制取该化合物的合成路线流程图.请注意:1.可选用必要的无机原料;2.已知酚羟基一般不易直接与羧酸发生类似酯化的反应,以上C→D的方法可供参照.


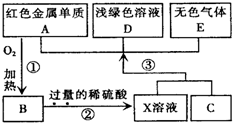 A、B、C、D、E为中学化学常见物质,其中A、C为金属单质,E为非金属单质,如图是它们之间的相互转化关系.请回答:
A、B、C、D、E为中学化学常见物质,其中A、C为金属单质,E为非金属单质,如图是它们之间的相互转化关系.请回答: