题目内容
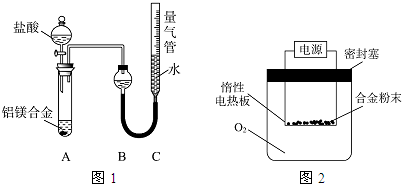
等量镁铝合金粉末分别与下列4种过量的溶液充分反应,放出H2最多的是( )
| A、2mol/L H2SO4溶液 |
| B、3mol/L CuSO4溶液 |
| C、6mol/L KOH溶液 |
| D、3mol/L Ba(OH)2溶液 |
考点:有关混合物反应的计算
专题:
分析:等量的镁铝合金分别与不同的溶液反应,根据电子守恒可知:当只有两种金属都和溶液反应,且都生成氢气,此时放出氢气的量最大,据此分析解答.
解答:
解:A.镁、铝都和稀硫酸反应生成氢气;
B.镁、铝都不能与硫酸铜溶液反应生成氢气;
C.镁不能和氢氧化钾反应,铝和氢氧化钾反应生成氢气;
D.镁不能和氢氧化钡溶液反应,铝和氢氧化钡溶液反应生成氢气;
根据以上分析知,生成氢气最多的是2mol/L H2SO4溶液,
故选A.
B.镁、铝都不能与硫酸铜溶液反应生成氢气;
C.镁不能和氢氧化钾反应,铝和氢氧化钾反应生成氢气;
D.镁不能和氢氧化钡溶液反应,铝和氢氧化钡溶液反应生成氢气;
根据以上分析知,生成氢气最多的是2mol/L H2SO4溶液,
故选A.
点评:本题考查金属的性质,题目难度不大,主要考查学生运用所学化学知识综合分析和解决实际问题的能力,该题溶液的浓度不是计算的数据,而是判断金属是否与溶液反应其生成氢气,认真审题为解答关键.

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目
除去下列物质中所含少量杂质(括号内为杂质),所选试剂和分离方法能达到实验目的是( )
| 混合物 | 试剂 | 分离方法 | |
| A | 乙烷(乙烯) | 高锰酸钾溶液 | 洗气 |
| B | 甲苯(苯酚) | 溴水 | 过滤 |
| C | 乙醇(水) | 氧化钙 | 蒸馏 |
| D | 乙酸乙酯(乙酸) | NaOH溶液 | 分液 |
| A、A | B、B | C、C | D、D |
下列说法正确的是( )
| A、向久置的氯水中滴入紫色石蕊试液,溶液将先变红后褪色 |
| B、欲除CO2中少量SO2气体,可将此混合气体通过盛饱和碳酸钠溶液的洗气瓶 |
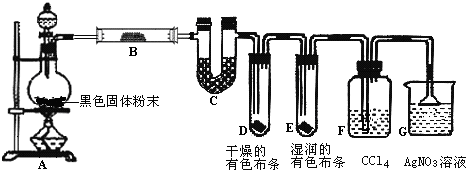
| C、氯气有漂白性,所以氯气能使有色布条褪色 |
| D、漂白粉的主要成分是CaCl2和Ca(ClO)2,应密封保存 |