题目内容
16.下列有关叙述正确的是( )| A. | ${\;}_{8}^{16}$O和${\;}_{8}^{18}$O中子数相同,质子数不同,互为同位素 | |
| B. | ${\;}_{9}^{19}$F-微粒质量数为19,电子数为9 | |
| C. | Na2O2晶体中阳离子与阴离子个数比为2:1 | |
| D. | MgCl2晶体中存在既存在离子键又存在共价键 |
分析 A.根据原子符号的含义、中子数=质量数-质子数以及同位素的含义;
B.阴离子中核外电子数=质子数+所带电荷数;
C.根据Na2O2为离子化合物,既含有离子键,又含有共价键,阴、阳离子个数之比为1:2;
D.MgCl2晶体无共价键.
解答 解:A.816O和818O的质子数都为8,中子数分别为16-8=8,18-8=10,即质子数相同,中子数不同,两者互为同位素,故A错误;
B.919F-的质子数为9,电子数为9+1=10,故B错误;
C.Na2O2为离子化合物,是由钠离子和过氧根离子构成的离子化合物,阴、阳离子个数之比为1:2,故C正确;
D.MgCl2晶体无共价键,只含离子键,故D错误.
故选C.
点评 本题考查了原子符号的含义以及阴离子中核外电子数=质子数+所带电荷数、离子化合物的组成与结构,难度中等,需要注意的是Na2O2为离子化合物,阴、阳离子个数之比为1:2.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
6.下列关于有机物沸点的说法中,错误的是( )
| A. | 直链烷烃中,碳原子数越多沸点越高 | |
| B. | 碳原子数相同的烷烃,支链越多沸点越高 | |
| C. | 相对分子质量相近的醇和烷烃相比,醇的沸点远远高于烷烃 | |
| D. | 碳原子数相同的醇,羟基越多沸点越高 |
7.PCl3可用于半导体生产的外延、扩散工序.有关物质的部分性质如下:
(一)制备:如图是实验室制备PCl3的装置(部分仪器已省略)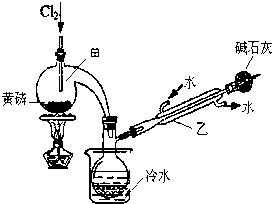
(1)仪器乙的名称冷凝管.
(2)实验室用漂白粉加浓盐酸制备Cl2的化学方程式:Ca(ClO)2+4HCl═CaCl2+2H2O+2Cl2↑.
(3)碱石灰的作用是吸收多余的Cl2,防止污染环境,且防止空气中的水分进入,影响产品纯度.
(4)向仪器甲中通入干燥Cl2之前,应先通入一段时间的CO2,其目的是排尽装置中的空气,防止O2和水与PCl3反应.
(二)提纯:
(5)粗产品中常含有POCl3、PCl5等.加入黄磷加热除去PCl5后,通过蒸馏(填实验操作名称),即可得到PCl3的纯品.
| 熔点/℃ | 沸点/℃ | 密度/g•mL-1 | 其他 | |
| 黄磷 | 44.1 | 280.5 | 1.82 | 2P(过量)+3Cl2$\frac{\underline{\;\;△\;\;}}{\;}$2PCl3;2P+5Cl2(过量)$\frac{\underline{\;\;△\;\;}}{\;}$2PCl5 |
| PCl3 | -112 | 75.5 | 1.574 | 遇水生成H3PO3和HCl,遇O2生成POCl3 |
| POCl3 | 2 | 105.3 | 1.675 | 遇水生成H3PO4和HCl,能溶于PCl3 |

(1)仪器乙的名称冷凝管.
(2)实验室用漂白粉加浓盐酸制备Cl2的化学方程式:Ca(ClO)2+4HCl═CaCl2+2H2O+2Cl2↑.
(3)碱石灰的作用是吸收多余的Cl2,防止污染环境,且防止空气中的水分进入,影响产品纯度.
(4)向仪器甲中通入干燥Cl2之前,应先通入一段时间的CO2,其目的是排尽装置中的空气,防止O2和水与PCl3反应.
(二)提纯:
(5)粗产品中常含有POCl3、PCl5等.加入黄磷加热除去PCl5后,通过蒸馏(填实验操作名称),即可得到PCl3的纯品.
4.常温常压下,下列各组物质的物理性质排列不正确的是( )
| A. | 密度:四氯化碳>乙酸乙酯>水 | |
| B. | 沸点:乙醇>丙烷>乙烷 | |
| C. | 在水中的溶解度:丙三醇>苯酚>1-氯丁烷 | |
| D. | 熔点:对二甲苯>邻二甲苯>间二甲苯 |
11.在一定温度下的定容容器中,发生反应:2A(g)+B(s)?C(g)+D(g),下列描述中能表明反应已达到平衡状态的是( )
①混合气体的压强不变
②混合气体的密度不变
③混合气体的平均相对分子质量不变
④C(g)的物质的量浓度不变
⑤容器内A、C、D三种气体的浓度之比为2:1:1
⑥单位时间内生成n molD,同时生成2n mol A
⑦单位时间内生成n molC,同时消耗n mol D.
①混合气体的压强不变
②混合气体的密度不变
③混合气体的平均相对分子质量不变
④C(g)的物质的量浓度不变
⑤容器内A、C、D三种气体的浓度之比为2:1:1
⑥单位时间内生成n molD,同时生成2n mol A
⑦单位时间内生成n molC,同时消耗n mol D.
| A. | ①②③ | B. | ②③④⑥ | C. | ②③⑤⑥⑦ | D. | ①③⑤⑦ |
5.下列说法不正确的是( )
| A. | 减压蒸馏可以防止炭化结焦 | |
| B. | 石油裂化的目的是提高汽油的产量和质量 | |
| C. | 石油的常压蒸馏,减压蒸馏以及煤的干馏都是物理变化 | |
| D. | 芳香烃的主要来源是石油的催化重整和煤的干馏 |
6.下列有关实验操作的叙述中正确的是( )
| A. | 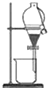 用于分离水和乙醇的混合物 | |
| B. | 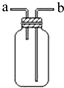 可用于H2,NH3,CO2,Cl2,HCl,NO2等气体收集 | |
| C. | 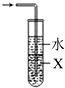 当X选用苯时可进行NH3和HCl的吸收,并防止倒吸 | |
| D. | 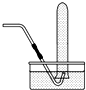 常用于实验室收集氧气、氢气等 |
