题目内容
 氯气是氯碱工业的主要产品之一,它是一种常用的消毒剂.请回答:
氯气是氯碱工业的主要产品之一,它是一种常用的消毒剂.请回答:(1)氯水中起杀菌消毒作用的物质是
(2)氯碱工业生产氯气的化学方程式为
(3)84消毒液(主要成分为NaClO)与氯气相比具有贮运方便等优点,用氯气与烧碱溶液反应制备84消毒液的离子方程式为
(4)二氧化氯是一种高效、广谱、安全的杀菌、保鲜剂.我国科学家研发了用氯气氧化亚氯酸钠(NaClO2)固体制备二氧化氯的方法,其化学方程式为
(5)饱和氯水与石灰石的反应是制取较浓HClO溶液的方法之一.某同学做了如下实验研究:
①在试管中加入过量的块状碳酸钙,再加入约20mL饱和氯水,充分反应,有少量气泡产生,溶液浅黄绿色褪去;
②过滤,将滤液滴在有色布条上,发现其比氯水的漂白性更强;
③为了确定反应产物,将滤液分为三份,分别进行以下实验:
第一份与石灰水混合,立即产生大量白色沉淀;
第二份与稀盐酸混合,立即产生大量无色气体;
将第三份加热,看到溶液变浑浊且有大量无色气体产生. 经检测,上述实验中产生的无色气体均为CO2.请回答:
①反应后所得的溶液漂白性增强的原因是
②依据上述实验可推知:②的滤液中的溶质除CaCl2、HClO外,还含有的溶质的化学式为
考点:氯气的化学性质,氯、溴、碘及其化合物的综合应用
专题:卤族元素
分析:(1)氯水中含HClO,具有强氧化性;
(2)电解食盐水生成氯气;
(3)氯气与烧碱溶液反应制备84消毒液,生成氯化钠、次氯酸钠和水;
(4)氯气氧化亚氯酸钠(NaClO2)固体制备二氧化氯的方法,还生成NaCl;
(5)①氯水中含盐酸和HClO,盐酸与碳酸钙反应;
②氯水中含盐酸、次氯酸,由第三份可知滤液中溶质加热,看到溶液变浑浊且有大量无色气体产生为CO2,以此解答.
(2)电解食盐水生成氯气;
(3)氯气与烧碱溶液反应制备84消毒液,生成氯化钠、次氯酸钠和水;
(4)氯气氧化亚氯酸钠(NaClO2)固体制备二氧化氯的方法,还生成NaCl;
(5)①氯水中含盐酸和HClO,盐酸与碳酸钙反应;
②氯水中含盐酸、次氯酸,由第三份可知滤液中溶质加热,看到溶液变浑浊且有大量无色气体产生为CO2,以此解答.
解答:
解:(1)氯水中含HClO,具有强氧化性,起杀菌消毒作用的物质是HClO,故答案为:HClO;
(2)氯碱工业生产氯气的化学方程式为2NaCl+2H2O
2NaOH+Cl2↑+H2↑,故答案为:2NaCl+2H2O
2NaOH+Cl2↑+H2↑;
(3)用氯气与烧碱溶液反应制备84消毒液的离子方程式为Cl2+2OH-═Cl-+ClO-+H2O,故答案为:Cl2+2OH-═Cl-+ClO-+H2O;
(4)氯气氧化亚氯酸钠(NaClO2)固体制备二氧化氯的方法,还生成NaCl,反应为Cl2+2NaClO2═2ClO2+2NaCl,故答案为:Cl2+2NaClO2═2ClO2+2NaCl;
(5)①氯水中存在平衡移动,碳酸钙消耗了氯水中的H+,使Cl2+H2O?H++Cl-+HClO平衡正向移动,HClO浓度大,漂白效果增强,
故答案为:碳酸钙消耗了氯水中的H+,使Cl2+H2O?H++Cl-+HClO平衡正向移动,HClO浓度大,漂白效果增强;
②氯水中含盐酸、次氯酸,由Ⅲ可知滤液中溶质加热,看到溶液变浑浊且有大量无色气体产生为CO2,则Ⅱ的滤液中的溶质除CaCl2、HClO外,还含有Ca(HCO3)2,第一份溶液与石灰水产生的白色沉淀的离子方程式为Ca2++HCO3-+OH-=CaCO3↓+H2O,
故答案为:Ca(HCO3)2;Ca2++HCO3-+OH-=CaCO3↓+H2O.
(2)氯碱工业生产氯气的化学方程式为2NaCl+2H2O
| ||
| ||
(3)用氯气与烧碱溶液反应制备84消毒液的离子方程式为Cl2+2OH-═Cl-+ClO-+H2O,故答案为:Cl2+2OH-═Cl-+ClO-+H2O;
(4)氯气氧化亚氯酸钠(NaClO2)固体制备二氧化氯的方法,还生成NaCl,反应为Cl2+2NaClO2═2ClO2+2NaCl,故答案为:Cl2+2NaClO2═2ClO2+2NaCl;
(5)①氯水中存在平衡移动,碳酸钙消耗了氯水中的H+,使Cl2+H2O?H++Cl-+HClO平衡正向移动,HClO浓度大,漂白效果增强,
故答案为:碳酸钙消耗了氯水中的H+,使Cl2+H2O?H++Cl-+HClO平衡正向移动,HClO浓度大,漂白效果增强;
②氯水中含盐酸、次氯酸,由Ⅲ可知滤液中溶质加热,看到溶液变浑浊且有大量无色气体产生为CO2,则Ⅱ的滤液中的溶质除CaCl2、HClO外,还含有Ca(HCO3)2,第一份溶液与石灰水产生的白色沉淀的离子方程式为Ca2++HCO3-+OH-=CaCO3↓+H2O,
故答案为:Ca(HCO3)2;Ca2++HCO3-+OH-=CaCO3↓+H2O.
点评:本题考查氯气及氯水的性质,为高频考点,注意把握氯水中的成分及化学平衡是解答本题的关键,侧重信息的抽取和应用能力的考查,题目难度中等.

练习册系列答案
相关题目
下列与有机物结构、性质相关的叙述错误的是( )
| A、甲烷与氯气反应生成一氯甲烷与苯和硝酸反应生成硝基苯的反应类型相同 |
| B、溴水、酸性高锰酸钾溶液均可用于鉴别乙烯和乙烷,也均可以除去乙烷中的乙烯 |
| C、核磁共振氢谱可以鉴别某些不同物质,质谱可快速、准确测定物质的分子量 |
| D、实验测得环己烷(l)、环己烯(l)和苯(l)的标准燃烧热分别为-3916 kJ/mol、-3747 kJ/mol和-3265 kJ/mol,可以证明在苯分子中不存在独立的碳碳双键 |
下列关于糖的说法不正确的是( )
| A、糖类是含有醛基或羰基的有机物物质 |
| B、淀粉和纤维素都是天然高分子化合物 |
| C、葡萄糖的分子式是C6H12O6,它是一种多羟基醛 |
| D、蔗糖和麦芽糖都是二糖,它们互为同分异构体 |
下列离子在溶液中能大量共存的是( )
| A、Fe3+、NH4+、SCN-、Cl- |
| B、Na+、H+、NO3-、SiO32-、 |
| C、OH-、Ba2+、Na+、AlO2- |
| D、Fe2+、NH4+、Cl- OH- |
在0.1mol?L-1的Na2CO3溶液中,下列关系正确的是( )
| A、C[Na+]>C[CO32-]>C[HCO3-]>C[OH-]>C[H+] |
| B、C[Na+]>C[CO32-]>C[OH-]>C[HCO3-]>C[H+] |
| C、C[Na+]+C[H+]=C[CO32-]+C[OH-]+C[HCO3-] |
| D、C[CO32-]+C[HCO3-]=0.1mol?L-1 |

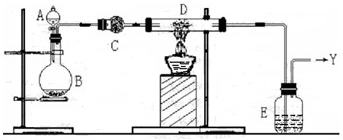 如图.B中盛装的是一种固体物质,当A中的溶液滴入B内反应一段时间后,所得产物经装置C即得纯净气体X,X分子中有10个电子,且该气体极易溶于水,一体积水能溶解700体积的该气体.D中盛装的是氧化铜,当X气体通过D时,氧化铜逐渐变成铜.最后从装置E中出来的气体是纯净的Y,Y是分子中含14个电子的单质气体.装置A、B、C、E中的药品从下列范围中选择.
如图.B中盛装的是一种固体物质,当A中的溶液滴入B内反应一段时间后,所得产物经装置C即得纯净气体X,X分子中有10个电子,且该气体极易溶于水,一体积水能溶解700体积的该气体.D中盛装的是氧化铜,当X气体通过D时,氧化铜逐渐变成铜.最后从装置E中出来的气体是纯净的Y,Y是分子中含14个电子的单质气体.装置A、B、C、E中的药品从下列范围中选择.