题目内容
在0.1mol?L-1的Na2CO3溶液中,下列关系正确的是( )
| A、C[Na+]>C[CO32-]>C[HCO3-]>C[OH-]>C[H+] |
| B、C[Na+]>C[CO32-]>C[OH-]>C[HCO3-]>C[H+] |
| C、C[Na+]+C[H+]=C[CO32-]+C[OH-]+C[HCO3-] |
| D、C[CO32-]+C[HCO3-]=0.1mol?L-1 |
考点:离子浓度大小的比较
专题:盐类的水解专题
分析:Na2CO3溶液中,有两步水解反应:①CO32-+H2O HCO3-+OH-;②HCO3-+H2O
HCO3-+OH-;②HCO3-+H2O H2CO3+OH-,其中以第一步水解为主,以此解答该题.
H2CO3+OH-,其中以第一步水解为主,以此解答该题.
 HCO3-+OH-;②HCO3-+H2O
HCO3-+OH-;②HCO3-+H2O H2CO3+OH-,其中以第一步水解为主,以此解答该题.
H2CO3+OH-,其中以第一步水解为主,以此解答该题.解答:
解:A、Na2CO3溶液中,有两步水解反应:①CO32-+H2O HCO3-+OH-;②HCO3-+H2O
HCO3-+OH-;②HCO3-+H2O H2CO3+OH-,其中以第一步水解为主,所以C[OH-]>C[HCO3-],故A错误;
H2CO3+OH-,其中以第一步水解为主,所以C[OH-]>C[HCO3-],故A错误;
B、Na2CO3溶液中,有两步水解反应:①CO32-+H2O HCO3-+OH-;②HCO3-+H2O
HCO3-+OH-;②HCO3-+H2O H2CO3+OH-,其中以第一步水解为主,所以C[OH-]>C[HCO3-],溶液呈碱性,所以C[OH-]>C[H+],故B正确;
H2CO3+OH-,其中以第一步水解为主,所以C[OH-]>C[HCO3-],溶液呈碱性,所以C[OH-]>C[H+],故B正确;
C、根据电荷守恒可知,C[Na+]+C[H+]=2C[CO32-]+C[OH-]+C[HCO3-],故C错误;
D、根据元素守恒可知,C[H2CO3]+C[CO32-]+C[HCO3-]=0.1mol?L-1,故D错误;
故选B.
 HCO3-+OH-;②HCO3-+H2O
HCO3-+OH-;②HCO3-+H2O H2CO3+OH-,其中以第一步水解为主,所以C[OH-]>C[HCO3-],故A错误;
H2CO3+OH-,其中以第一步水解为主,所以C[OH-]>C[HCO3-],故A错误;B、Na2CO3溶液中,有两步水解反应:①CO32-+H2O
 HCO3-+OH-;②HCO3-+H2O
HCO3-+OH-;②HCO3-+H2O H2CO3+OH-,其中以第一步水解为主,所以C[OH-]>C[HCO3-],溶液呈碱性,所以C[OH-]>C[H+],故B正确;
H2CO3+OH-,其中以第一步水解为主,所以C[OH-]>C[HCO3-],溶液呈碱性,所以C[OH-]>C[H+],故B正确;C、根据电荷守恒可知,C[Na+]+C[H+]=2C[CO32-]+C[OH-]+C[HCO3-],故C错误;
D、根据元素守恒可知,C[H2CO3]+C[CO32-]+C[HCO3-]=0.1mol?L-1,故D错误;
故选B.
点评:本题主要考查了盐类的水解,中等难度,解题的关键是理解二元素酸根水解的实质,答题时注意正确使用电解质溶液中的几个守恒关系.

练习册系列答案
相关题目
下列图示所表示的实验设计正确的是( )
A、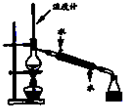 分离苯和甲苯 |
B、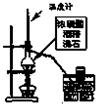 制备乙烯 |
C、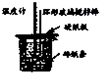 测定中和热 |
D、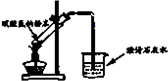 加入碳酸氢钠 |
25℃时,1mol/L的NH4Cl、CH3COONH4、NH4HSO4、NH3?H2O四种溶液中,测得c(NH4+)分别为a、b、c、d(单位为mol/L),下列判断正确的是( )
| A、a=b=c=d |
| B、a>b>d>c |
| C、d>a>c>b |
| D、c>a>b>d |
已知H2B在溶液中的电离方程式:H2B=H++HB-,HB-?H++B2-.下列叙述一定正确的是( )
| A、Na2B溶液存在:c (Na+)=2c (HB-)+2c(B2-)+2c(H2B) |
| B、NaHB溶液一定显酸性 |
| C、HB-的水解方程式:HB-+H2O?H2B+OH- |
| D、NaHB溶液与稀盐酸反应的离子方程式是:HB-+H+=H2B |
下列六种物质:①Na20 ②Na202③CaCl2溶液④Na2C03溶液⑤NaOH ⑥NaHC03中,不能与二氧化碳反应的是( )
| A、①④ | B、②③ | C、③⑥ | D、③④⑥ |
下列说法不正确的是( )
| A、增大压强,活化分子百分数不变,化学反应速率增大 |
| B、升高温度,活化分子百分数增大,化学反应速率增大 |
| C、加入反应物,活化分子百分数增大,化学反应速率增大 |
| D、使用催化剂,活化分子百分数增大,化学反应速率增大 |
 氯气是氯碱工业的主要产品之一,它是一种常用的消毒剂.请回答:
氯气是氯碱工业的主要产品之一,它是一种常用的消毒剂.请回答: