��Ŀ����
15��ij�о���ѧϰС��Ϊȷ��һ�ִ�ú����ȡ��Һ̬��X�Ľṹ���������̽����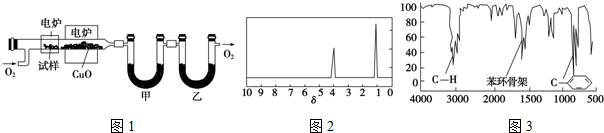
����һ������̼�⻯��������ͨ���ȵ�����ͭ���������������ɶ�����̼��ˮ������װ����ˮ�Ȼ��ƺ����������Ƶ����չ���ȫ���գ�2.12g�л���X��������������7.04g������̼��1.80gˮ��
�������ͨ������������֪X����Է�������Ϊ106��
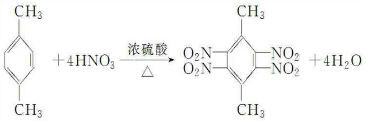
���������ú˴Ź����Dz��X��1H�˴Ź�������2���壬�����֮��Ϊ2��3����ͼ2��
�����ģ����ú�������Dz��X���ӵĺ��������ͼ3��
����գ�
��1��X�ķ���ʽΪC8H10��X������Ϊ�Զ��ױ���
��2��������е���������������Ϊ������
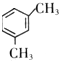
��3��д��X������Ũ�����Ũ�������ﷴӦ�Ļ�ѧ����ʽ��
 ��
����4��д��X��������������ͬ���칹��ṹ��ʽ
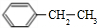 ��
�� ��
���ٷ����� �ڱ�����һ�ȴ���������
��5��X�Դ���Ϊ�ܼ��ڴ��������������������õ���һ����Ҫ�Ļ���ԭ��PTA���������ϵ�֪PTA���ܽ�ȣ�25��ʱ0.25g��50��ʱ0.97g��95��ʱ7.17g���õ��Ĵֲ�Ʒ���в��ֲ��������ʣ������ʵ�������ᴿPTA��ʵ�鷽�������ֲ�Ʒ����������ˮ�У����ȹ��ˣ���ȴ�ᾧ�����˳����壮
���� ��1����X�����ʵ���Ϊ$\frac{2.12g}{106g/mol}$=0.02mol�����ɶ�����̼Ϊ$\frac{7.04g}{44g/mol}$=0.16mol������ˮΪ$\frac{1.8g}{18g/mol}$=0.1mol���������N��C��=$\frac{0.16mol}{0.02mol}$=8��N��H��=$\frac{0.1mol��2}{0.02mol}$=10����X�ķ���ʽΪC8H10��X�ĺ�����ײⶨ���б��������ڱ���ͬϵ���1H�˴Ź�������2���壬�����֮��Ϊ2��3����XΪ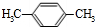 ��
��
��2��ͨ��������������Է��������ķ���Ϊ������
��3��X��Ũ���ᷢ��ȡ����Ӧ����������������������Hԭ��ȫ��Ϊ�ǻ�ȡ����
��4��X��ͬ���칹����������������ٷ��������ڱ�����һ�ȴ��������֣���������3��Hԭ�ӣ�Ϊ�ұ������ױ���
��5��PTA���ܽ�����¶����߶�����Ҵֲ�Ʒ�����ʲ�����ˮ�����Կ��Խϸ��¶��ܽ⣬���ȹ��ˣ��ᾧ�������壮
��� �⣺��1����X�����ʵ���Ϊ$\frac{2.12g}{106g/mol}$=0.02mol�����ɶ�����̼Ϊ$\frac{7.04g}{44g/mol}$=0.16mol������ˮΪ$\frac{1.8g}{18g/mol}$=0.1mol���������N��C��=$\frac{0.16mol}{0.02mol}$=8��N��H��=$\frac{0.1mol��2}{0.02mol}$=10����X�ķ���ʽΪC8H10��X�ĺ�����ײⶨ���б��������ڱ���ͬϵ���1H�˴Ź�������2���壬�����֮��Ϊ2��3����XΪ ������Ϊ�Զ��ױ���
������Ϊ�Զ��ױ���
�ʴ�Ϊ��C8H10���Զ��ױ���
��2�������ͨ������������֪X����Է����������÷�����Ϊ������
�ʴ�Ϊ��������
��3��X������Ũ�����Ũ�������ﷴӦ�Ļ�ѧ����ʽ�� ��
��
�ʴ�Ϊ�� ��
��
��4��X��ͬ���칹����������������ٷ��������ڱ�����һ�ȴ��������֣�����������ͬ���칹���У�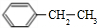 ��
�� ��
��
�ʴ�Ϊ��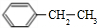 ��
�� ��
��
��5��PTA���ܽ�����¶����߶�����Ҵֲ�Ʒ�����ʲ�����ˮ���ᴿPTA��ʵ�鷽�������ֲ�Ʒ����������ˮ�У����ȹ��ˣ���ȴ�ᾧ�����˳����壬
�ʴ�Ϊ�����ֲ�Ʒ����������ˮ�У����ȹ��ˣ���ȴ�ᾧ�����˳����壮
���� ���⿼���л���ṹʽ��ȷ������������ͬ���칹����д�����ʵķ����ᴿ��ע���л����о���һ�㷽���벽�裬�Ѷ��еȣ�

 Ӣ�ŵ��ϵ�д�
Ӣ�ŵ��ϵ�д� ������������Ծ�ϵ�д�
������������Ծ�ϵ�д�| A�� | �����£�0.1mol/LNa2S��Һ�д��ڣ�c��OH-��=c��H+��+c��HS-��+c��H2S�� | |
| B�� | 0.1mol/LNaHCO3��Һ��0.1mol/LNaOH��Һ�������ϣ�������Һ�У�C��Na+����c��CO32-����c��HCO3- ����c��OH-����c��H+�� | |
| C�� | pH��ͬ�Ģ�CH3 COONa��NaHCO3��NaClO������Һ��c��Na+�����٣��ڣ��� | |
| D�� | ��0.1mol•L-1�İ�ˮ�м�����������粒��壬����Һ��$\frac{c��O{H}^{-}��}{c��N{H}_{3}•{H}_{2}O��}$���� |
| A�� | HCO3-+H2O?H3O-+CO32- | B�� | CO32-+H2O?HCO3-+OH- | ||
| C�� | NH3+H2O?NH3•H2O | D�� | HCO3-+OH-�TH2O+CO32- |
| A�� |  | B�� |  | C�� |  | D�� |  |
| A�� | NaHCO3 | B�� | CH3COONa | C�� | NaCl | D�� | NH4Cl |


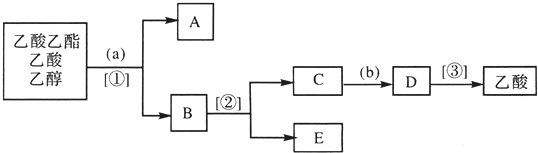
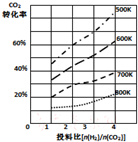 �о�CO2�����öԴٽ���̼���Ĺ���������Ҫ�����壮
�о�CO2�����öԴٽ���̼���Ĺ���������Ҫ�����壮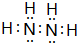 ��
��