题目内容
4. 研究CO2的利用对促进低碳社会的构建具有重要的意义.
研究CO2的利用对促进低碳社会的构建具有重要的意义.(1)已知拆开1molH2、1molO2和液态水中1molO-H键使之成为气态原子所需的能量分别为436kJ、496kJ和462kJ;CH3OH(g)的燃烧热为627kJ•mol-1则CO2(g)+3H2(g)═CH3OH(g)+H2O(l)△H=-93kJ•mol-1
(2)将燃煤废气中的CO2转化为二甲醚的反应原理为:2CO2(g)+6H2(g)═CH3OCH3(g)+3H2O(l)
①该反应平衡常数表达式K=$\frac{c(C{H}_{3}OC{H}_{3})}{{c}^{2}(C{O}_{2})×{c}^{2}({H}_{2})}$;
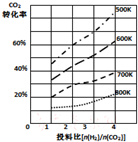
②已知在某压强下,该反应在不同温度、不同投料比时,CO2的转化率如图所示.该反应的△H<0(填“>”或“<”),若温度不变,减小反应投料比[$\frac{n({H}_{2})}{n(C{O}_{2})}$],则K将不变(填“增大”、“减小”或“不变”).
③某温度下,向体积一定的密闭容器中通入CO2(g)与H2(g)发生上述反应,当下列物理量不再发生变化时,能表明上述可逆反应达到化学平衡的是ABC;
A.二氧化碳的浓度 B.容器中的压强
C.气体的密度 D.CH3OCH3与H2O的物质的量之比.
分析 (1)设反应的反应热为xkJ•mol-1,根据甲醇的燃烧热写出:CH3OH(g)+$\frac{3}{2}$O2(g)=CO2(g)+2H2O(l)△H=-627kJ•mol-1 ,结合CO2(g)+3H2(g)=CH3OH(g)+H2O(l)△H=xkJ•mol-1利用盖斯定律可得:3H2(g)+$\frac{3}{2}$O2(g)=3H2O(l)△H=-627kJ•mol-1+kJ•mol-1,再依据焓变△H=反应物拆化学键吸收的能量-生成物形成化学键放出的能量计算得到;
(2)①根据平衡常数等于生成物的浓度幂之积除以反应物的浓度幂之积进行计算;
②根据温度对平衡的影响分析△H的符号;平衡常数K只与温度有关;
③当可逆反应达到平衡状态时,正逆反应速率相等,反应体现中各物质的物质的量、物质的量浓度及百分含量都不变,以及由此引起的一些物理量不变,据此分析解答;
解答 解:(1)设反应的反应热为xkJ•mol-1,根据甲醇的燃烧热写出:CH3OH(g)+$\frac{3}{2}$O2(g)=CO2(g)+2H2O(l)△H=-627kJ•mol-1 ,结合CO2(g)+3H2(g)=CH3OH(g)+H2O(l)△H=xkJ•mol-1利用盖斯定律可得:3H2(g)+$\frac{3}{2}$O2(g)=3H2O(l)△H=-627kJ•mol-1+xkJ•mol-1,即436kJ×3+496kJ×$\frac{3}{2}$-462kJ×6=-627kJ+xkJ,解得:x=-93;
故答案为:-93;
(2)①平衡常数等于生成物的浓度幂之积除以反应物的浓度幂之积,所以平衡常数K=$\frac{c(C{H}_{3}OC{H}_{3})}{{c}^{2}(C{O}_{2})×{c}^{2}({H}_{2})}$,故答案为:$\frac{c(C{H}_{3}OC{H}_{3})}{{c}^{2}(C{O}_{2})×{c}^{2}({H}_{2})}$;
②因为温度越高,CO2转化率越小,则平衡逆移,所以该反应正方向为放热反应,即△H<0,K只受温度影响,若温度不变,减小投料比,则K不变,
故答案为:<;不变;
③A.二氧化碳的浓度不变,则达到了平衡,故A选;
B.反应前后气体的系数和不相等,当容器内压强不再改变,则达到了平衡,故B选;
C.该反应是一个反应前后气体体积变化的可逆反应,容器的体积不变,但反应前后气体质量变化,气体的密度不发生变化,则达到了平衡,故C选;
D.任何时候CH3OCH3与H2O的物质的量之比不变,不能说明反应达到平衡,故D不选;
故答案为:ABC.
点评 本题主要考查了化学平衡的判断、化学平衡常数以及热化学方程式的书写,注意把握从键能的角度以及盖斯定律计算反应热的方法,第(1)问难度较大.

 培优三好生系列答案
培优三好生系列答案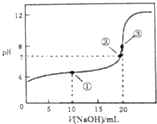 常温下,用0.1000mol•L-1NaOH溶液滴定20.00mL0.1000mol•L-1CH3COOH溶液所得曲线如图.下列说法正确的是( )
常温下,用0.1000mol•L-1NaOH溶液滴定20.00mL0.1000mol•L-1CH3COOH溶液所得曲线如图.下列说法正确的是( )| A. | 滴定过程中可能出现:c(CH3COOH)>c(CH3COO-)>c(H+)>c(Na+)>c(OH-) | |
| B. | ①处水的电离程度大于②处水的电离程度 | |
| C. | ②处加入的NaOH溶液恰好将CH3COOH中和 | |
| D. | ③处所示溶液:c(Na+)<c(CH3COO-) |
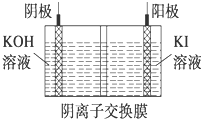 碘被称为“智力元素”,科学合理地补充碘可防治碘缺乏病,KI、KIO3曾先后用于加碘盐中.
碘被称为“智力元素”,科学合理地补充碘可防治碘缺乏病,KI、KIO3曾先后用于加碘盐中.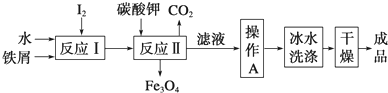
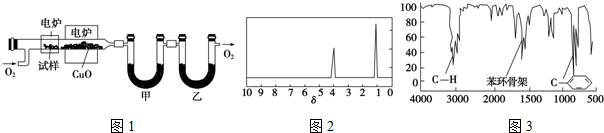
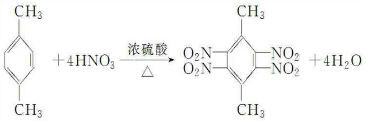 .
.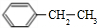 、
、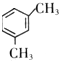 .
.
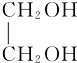 +O2$→_{△}^{Cu}$OHC-CHO+2H2O.
+O2$→_{△}^{Cu}$OHC-CHO+2H2O.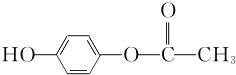 .
. .
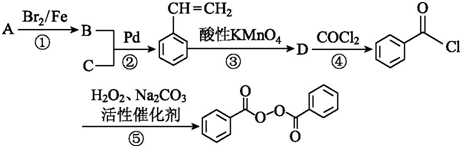
.
 ;
;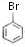 +CH2=CH2$\stackrel{Pd}{→}$
+CH2=CH2$\stackrel{Pd}{→}$ +HBr;
+HBr;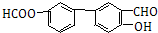 (苯环上基团位置可换);
(苯环上基团位置可换); )
)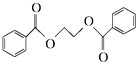 的流程图,无机物任选,注明反应条件.
的流程图,无机物任选,注明反应条件.