题目内容
18.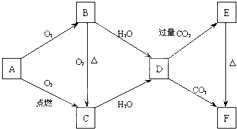 如图所示,A、B、C、D、E、F为金属钠或钠的化合物.
如图所示,A、B、C、D、E、F为金属钠或钠的化合物.(1)C的化学式为Na2O2;E的化学式为NaHCO3.
(2)D转化为F的化学方程式为2NaOH+CO2=Na2CO3+H2O.
(3)F溶液与Ca(OH)2溶液反应的离子方程式为:CO32-+Ca2+=CaCO3↓.
分析 A、B、C、D、E、F为金属钠或钠的化合物,A与氧气反应生成B,B与氧气在加热条件下得到C,而A与氧气在点燃条件下直接得到C,则A为Na,B为Na2O,C为Na2O2,Na2O、Na2O2均与水反应生成D,则D为NaOH,NaOH与过量二氧化碳反应生成E为NaHCO3,E加热分解得到F,且NaOH与二氧化碳反应也得到F,故F为Na2CO3,据此解答.
解答 解:A、B、C、D、E、F为金属钠或钠的化合物,A与氧气反应生成B,B与氧气在加热条件下得到C,而A与氧气在点燃条件下直接得到C,则A为Na,B为Na2O,C为Na2O2,Na2O、Na2O2均与水反应生成D,则D为NaOH,NaOH与过量二氧化碳反应生成E为NaHCO3,E加热分解得到F,且NaOH与二氧化碳反应也得到F,故F为Na2CO3.
(1)由上述分析可知,C的化学式为Na2O2,E的化学式为NaHCO3,故答案为:Na2O2;NaHCO3;
(2)D转化为F的化学方程式为:2NaOH+CO2=Na2CO3+H2O,故答案为:2NaOH+CO2=Na2CO3+H2O;
(3)Na2CO3溶液与Ca(OH)2溶液反应的离子方程式为:CO32-+Ca2+=CaCO3↓,故答案为:CO32-+Ca2+=CaCO3↓.
点评 本题考查无机物推断,涉及Na元素单质化合物性质与转化,根据反应条件进行推断,熟练掌握元素化合物性质.

练习册系列答案
相关题目
8.下列说法正确的是( )
| A. | 钠保存在煤油里的原因之一是它极易与氧气反应 | |
| B. | 铝在空气中很容易燃烧 | |
| C. | 镁表面的氧化膜疏松,不能保护内层金属 | |
| D. | 铁锈的主要成分是Fe3O4 |
10.下列反应的离子方程式错误的是( )
| A. | 碘水加到溴化钠溶液中:2Br-+I2═2I-+Br2 | |
| B. | 氯气溶于水:Cl2+H2O═2H++Cl-+ClO- | |
| C. | 大理石溶于醋酸:CaCO3+2CH3COOH═Ca2++2CH3COO-+CO2↑+H2O | |
| D. | FeBr2溶液中通入少量的Cl2:Cl2+2Fe2+═2Fe3++2Cl- |