题目内容
最近一份调查报告表明:我国每年约需医药中间体2000多种,需求量达250万吨以上,F就是一种重要的医药中间体,可以甲苯为原料合成,其路线如下:

已知:
请回答下列问题:
(1)有机物B的名称是 ;F中含氧官能团的名称是 .
(2)C中核磁共振氢谱显示有 个吸收峰;B→C的化学方程式是 ;E→F的化学方程式是
.
(3)写出同时符合下列条件的A的同分异构体的结构简式: (写出两个).
①分子中含有 ②苯环上有两个取代基,且处于对位
②苯环上有两个取代基,且处于对位
(4)甲苯除了具有上述用途之外,还可以和硝酸铵通过 反应(填反应类型)制取烈性炸药TNT(2,4,6三硝基甲苯).
(5)下列有关F的说法正确的是 (填字母)
A、分子式为C2H4BrNO2 B、属于卤代烃 C、不能与H2发生加成反应 D、既能和碱反应又能和酸反应.

已知:

请回答下列问题:
(1)有机物B的名称是
(2)C中核磁共振氢谱显示有
(3)写出同时符合下列条件的A的同分异构体的结构简式:
①分子中含有
 ②苯环上有两个取代基,且处于对位
②苯环上有两个取代基,且处于对位(4)甲苯除了具有上述用途之外,还可以和硝酸铵通过
(5)下列有关F的说法正确的是
A、分子式为C2H4BrNO2 B、属于卤代烃 C、不能与H2发生加成反应 D、既能和碱反应又能和酸反应.
考点:有机物的合成
专题:有机物的化学性质及推断
分析:由甲苯与A的分子式,结合D的结构简式可知,甲苯发生甲基对位的硝化反应生成A,则A为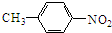 ,A发生信息中反应,硝基被还原为氨基生成B,则B的结构简式为
,A发生信息中反应,硝基被还原为氨基生成B,则B的结构简式为 ,结合D的结构可知,B中氨基中1个H原子被取代生成C为
,结合D的结构可知,B中氨基中1个H原子被取代生成C为 ,C被酸性高锰酸钾溶液氧化生成D,对比D、F的结构可知,D与液溴发生取代反应生成E为
,C被酸性高锰酸钾溶液氧化生成D,对比D、F的结构可知,D与液溴发生取代反应生成E为 ,E发生水解反应得到F,据此答题.
,E发生水解反应得到F,据此答题.
 ,A发生信息中反应,硝基被还原为氨基生成B,则B的结构简式为
,A发生信息中反应,硝基被还原为氨基生成B,则B的结构简式为 ,结合D的结构可知,B中氨基中1个H原子被取代生成C为
,结合D的结构可知,B中氨基中1个H原子被取代生成C为 ,C被酸性高锰酸钾溶液氧化生成D,对比D、F的结构可知,D与液溴发生取代反应生成E为
,C被酸性高锰酸钾溶液氧化生成D,对比D、F的结构可知,D与液溴发生取代反应生成E为 ,E发生水解反应得到F,据此答题.
,E发生水解反应得到F,据此答题.解答:
解:由甲苯与A的分子式,结合D的结构简式可知,甲苯发生甲基对位的硝化反应生成A,则A为 ,A发生信息中反应,硝基被还原为氨基生成B,则B的结构简式为
,A发生信息中反应,硝基被还原为氨基生成B,则B的结构简式为 ,结合D的结构可知,B中氨基中1个H原子被取代生成C为
,结合D的结构可知,B中氨基中1个H原子被取代生成C为 ,C被酸性高锰酸钾溶液氧化生成D,对比D、F的结构可知,D与液溴发生取代反应生成E为
,C被酸性高锰酸钾溶液氧化生成D,对比D、F的结构可知,D与液溴发生取代反应生成E为 ,E发生水解反应得到F,
,E发生水解反应得到F,
(1)B为 ,B的名称是对氨基甲苯;F中含氧官能团的名称是羧基,故答案为:对氨基甲苯;羧基;
,B的名称是对氨基甲苯;F中含氧官能团的名称是羧基,故答案为:对氨基甲苯;羧基;
(2)C为 ,C中核磁共振氢谱显示有5个吸收峰,B→C的化学方程式是
,C中核磁共振氢谱显示有5个吸收峰,B→C的化学方程式是 ,E→F的化学方程式是
,E→F的化学方程式是 ,
,
故答案为:5; ;
; ;
;
(3)A为 ,同时符合下列条件①分子中含有
,同时符合下列条件①分子中含有 ②苯环上有两个取代基,且处于对位,A的同分异构体的结构简式为
②苯环上有两个取代基,且处于对位,A的同分异构体的结构简式为 ,故答案为:
,故答案为: ;
;
(4)甲苯除了具有上述用途之外,还可以和硝酸铵通过取代(硝化)反应制取烈性炸药TNT(2,4,6三硝基甲苯),
故答案为:取代(硝化)反应;
(5)下列有关F的说法中,A、根据F的结构简式可知,分子式为C2H4BrNO2,故A正确; B、F中有氧和氮,不属于卤代烃,故B错误; C、F中有苯环,可以与H2发生加成反应,故C错误; D、F中有氨基和羧基,所以既能和碱反应又能和酸反应,故D正确;
故选AD.
 ,A发生信息中反应,硝基被还原为氨基生成B,则B的结构简式为
,A发生信息中反应,硝基被还原为氨基生成B,则B的结构简式为 ,结合D的结构可知,B中氨基中1个H原子被取代生成C为
,结合D的结构可知,B中氨基中1个H原子被取代生成C为 ,C被酸性高锰酸钾溶液氧化生成D,对比D、F的结构可知,D与液溴发生取代反应生成E为
,C被酸性高锰酸钾溶液氧化生成D,对比D、F的结构可知,D与液溴发生取代反应生成E为 ,E发生水解反应得到F,
,E发生水解反应得到F,(1)B为
 ,B的名称是对氨基甲苯;F中含氧官能团的名称是羧基,故答案为:对氨基甲苯;羧基;
,B的名称是对氨基甲苯;F中含氧官能团的名称是羧基,故答案为:对氨基甲苯;羧基;(2)C为
 ,C中核磁共振氢谱显示有5个吸收峰,B→C的化学方程式是
,C中核磁共振氢谱显示有5个吸收峰,B→C的化学方程式是 ,E→F的化学方程式是
,E→F的化学方程式是 ,
,故答案为:5;
 ;
; ;
;(3)A为
 ,同时符合下列条件①分子中含有
,同时符合下列条件①分子中含有 ②苯环上有两个取代基,且处于对位,A的同分异构体的结构简式为
②苯环上有两个取代基,且处于对位,A的同分异构体的结构简式为 ,故答案为:
,故答案为: ;
;(4)甲苯除了具有上述用途之外,还可以和硝酸铵通过取代(硝化)反应制取烈性炸药TNT(2,4,6三硝基甲苯),
故答案为:取代(硝化)反应;
(5)下列有关F的说法中,A、根据F的结构简式可知,分子式为C2H4BrNO2,故A正确; B、F中有氧和氮,不属于卤代烃,故B错误; C、F中有苯环,可以与H2发生加成反应,故C错误; D、F中有氨基和羧基,所以既能和碱反应又能和酸反应,故D正确;
故选AD.
点评:本题考查有机物的推断与合成,充分利用有机物的分子式与结构分析解答,注意官能团的引入、消除与衍变,需要学生熟练掌握官能团的性质与转化,难度中等.

练习册系列答案
相关题目
下列离子方程式正确的是( )
| A、金属钠与水反应:Na+2H2O=Na++2OH-+H2↑ |
| B、金属铝投入NaOH溶液中:Al+2OH-=AlO2-+H2↑ |
| C、稀硝酸中加入过量铁粉:Fe+4H++NO3-=Fe3++NO↑+2H2O |
| D、FeCl2酸性溶液放在空气中变质:4Fe2++4H++O2=4Fe3++2H2O |
下列溶液中微粒的物质的量浓度关系正确的是( )
| A、25℃时,等体积、等浓度的NaX和弱酸HX混合后的溶液中:c(Na+)>c(HX)>c(X-)>c(H+)>c(OH-) |
| B、常温下,pH≈5.5的0.1mol/LNaHC2O4溶液:c(Na+)>c(HC2O4-)>c(H2C2O4)>c(C2O42-) |
| C、0.1mol/LNaHS溶液:c(OH-)+c(S2-)=c(H+)+c(H2S) |
| D、室温下,向0.1mol/LNH4HSO4溶液中滴加NaOH溶液至中性:c(Na+)>c(SO42-)>c(NH4+)>c(OH-)=c(H+) |
在一定体积的密闭容器中放入3升气体R和5升气体Q,在一定条件下发生反应2R(气)+5Q(气)═4X(气)+nY(气),反应完全后,容器温度不变,混和气体的压强是原来的87.5%,则化学方程式中的n值是( )
| A、1 | B、2 | C、3 | D、4 |
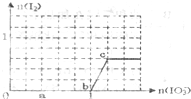 已知:还原性还原性HSO3->I-,氧化性IO3->I2.在含3mol NaHSO3的溶液中逐滴加入KIO3溶液.加入KIO3和析出I2的物质的量的关系曲线如图所示.下列说法正确的是( )
已知:还原性还原性HSO3->I-,氧化性IO3->I2.在含3mol NaHSO3的溶液中逐滴加入KIO3溶液.加入KIO3和析出I2的物质的量的关系曲线如图所示.下列说法正确的是( )| A、反应过程中的氧化产物均为SO3 |
| B、a点时剩余NaHSO3的物质的量为1.2 mol |
| C、b点时的还原产物可能是KI或NaI |
| D、当溶液中I-与I2的物质的量之比为1:1时,加入的KIO3为1.1mol |
反应Fe(s)+CO2(g)?FeO(s)+CO(g),700℃时平衡常数为1.47,900℃时平衡常数为2.15.下列说法正确的是( )
| A、升高温度该反应的正反应速率增大,逆反应速率减小 | ||
B、该反应的化学平衡常数表达式为K=
| ||
| C、绝热容器中进行该反应,温度不再变化,则达到化学平衡状态 | ||
| D、该反应的正反应是放热反应 |
 根据如图所示装置回答问题:
根据如图所示装置回答问题: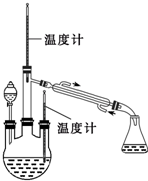 肼是重要的化工原料.某探究小组利用下列反应制取水合肼(N2H4?H2O).CO(NH2)+2NaOH+NaClO=Na2CO3+N2H4?H2O+NaCl
肼是重要的化工原料.某探究小组利用下列反应制取水合肼(N2H4?H2O).CO(NH2)+2NaOH+NaClO=Na2CO3+N2H4?H2O+NaCl
