题目内容
20.有机物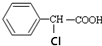 有多种同分异构体,其中属于酯类且氯原子直接连在苯环上的同分异构体有多少种(不考虑立体异构)( )
有多种同分异构体,其中属于酯类且氯原子直接连在苯环上的同分异构体有多少种(不考虑立体异构)( )| A. | 6种 | B. | 9种 | C. | 15种 | D. | 19种 |
分析  有多种同分异构体,含有酯基,如果苯环上有2个取代基则为:-Cl、-OOCCH3,-Cl、-CH2OOCH,-Cl、-COOCH3,如果苯环上有3个取代基则为:-Cl、-OOCH、-CH3,然后根据两个取代基分邻、间、对三种;含有两个或两个以上取代基的同分异构体书写,先将所有取代基拿下,分析母体对称性找出被一个取代基取代的产物种类,然后再分析各种一取代物的对称性,看第二个取代基可进入的位置,…,直至全部取代基都代入确定同分异构体.
有多种同分异构体,含有酯基,如果苯环上有2个取代基则为:-Cl、-OOCCH3,-Cl、-CH2OOCH,-Cl、-COOCH3,如果苯环上有3个取代基则为:-Cl、-OOCH、-CH3,然后根据两个取代基分邻、间、对三种;含有两个或两个以上取代基的同分异构体书写,先将所有取代基拿下,分析母体对称性找出被一个取代基取代的产物种类,然后再分析各种一取代物的对称性,看第二个取代基可进入的位置,…,直至全部取代基都代入确定同分异构体.
解答 解: 有多种同分异构体,含有酯基,如果苯环上有2个取代基则为:-Cl、-OOCCH3,-Cl、-CH2OOCH,-Cl、-COOCH3,2个取代基分为邻、间、对三种,所以共有9种;
有多种同分异构体,含有酯基,如果苯环上有2个取代基则为:-Cl、-OOCCH3,-Cl、-CH2OOCH,-Cl、-COOCH3,2个取代基分为邻、间、对三种,所以共有9种;
如果苯环上有3个取代基则为:-Cl、-OOCH、-CH3,
第一步:苯环上有1个-Cl时,只有1种结构;
第二步:苯环上有2个取代基:1个-Cl、1个-OOCH,把一个取代基置于1位,则另一个取代基有2、3、4三种连接方式,即有邻、间、对3种同分异构体;
第三步:环上有3个取代基:1个-Cl、1个-OOCH,1个-CH3,先将2个取代基分别定于邻、对、间三种位置,第三个取代基共有4+4+2=10种连接方式,故有10种同分异构体;
所以共有19种同分异构体,
故选D.
点评 本题主要考查了同分异构体的书写,苯环上的取代基种类和数目决定了同分异构体的种类,注意取代基的分类.

练习册系列答案
相关题目
10.下列有关实验的操作、现象和结论或解释 都正确的是( )
| 选项 | 操作 | 现象 | 结论或解释 |
| A | 用pH计或pH试纸分别测定饱和SO2水溶液和饱和CO2水溶液的pH值 | 饱和SO2水溶液的pH值小于饱和CO2水溶液 | 亚硫酸强于碳酸 |
| B | 向加热KClO3制氧气后的残余固体中加入浓H2SO4,继续加热 | 产生黄绿色气体 | 浓硫酸与残渣中的KCl发生反应生成了Cl2 |
| C | 加热装在试管中的NH4Cl晶体 | 试管底部的晶体消失,试管上部有晶体凝结. | NH4Cl晶体发生了升华. |
| D | 将一根较粗的铜丝在酒精灯火焰上加热到红热,然后趁热插入乙醇中一会儿取出. | 铜丝先变黑后又变红,乙醇中伴有刺激性气味产生. | 铜丝发生了几个反应,但铜丝前后的质量不变. |
| A. | A | B. | B | C. | C | D. | D |
8.纳米CdSe(硒化镉)可用作光学材料.在一定条件下,由Na2SO3和Se反应生成Na2SeSO3(硒代硫酸钠);再由CdCl2形成的配合物与Na2SeSO3反应制得CdSe纳米颗粒.流程图如下:
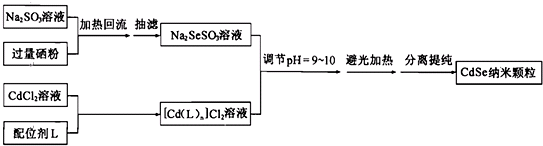
已知:①纳米颗粒通常指平均粒径为1~100nm的粒子
②CdSe纳米颗粒的大小影响会其发光性质.在一定配位剂浓度下,避光加热步骤中反应时间和温度对纳米颗粒平均粒径的影响,结果如图1所示;某温度下配位剂浓度对纳米颗粒平均粒径的影响,如图2所示:

则下列说法中正确的是( )

已知:①纳米颗粒通常指平均粒径为1~100nm的粒子
②CdSe纳米颗粒的大小影响会其发光性质.在一定配位剂浓度下,避光加热步骤中反应时间和温度对纳米颗粒平均粒径的影响,结果如图1所示;某温度下配位剂浓度对纳米颗粒平均粒径的影响,如图2所示:

则下列说法中正确的是( )
| A. | 在分离提纯CdSe时一般向溶液中加入丙酮,以增强溶剂极性,有利于CeSe的沉淀,提高收率 | |
| B. | 一般可用NaOH调节Na2SeSO3溶液的pH值,在此过程中会有HSe-和HSO3-生成 | |
| C. | 该纳米颗粒不能使用常压过滤或者减压过滤分离,因为其易在滤纸表面形成一层致密而厚实的膜,阻碍溶剂的通过 | |
| D. | 改变反应温度和反应时间,可以得到不同发光性质的CdSe纳米颗粒;且若要在60℃得到3.0 nm的CdSe纳米颗粒,可尝试降低配位剂浓度的方法 |
15.用酸式滴定管准确移取25.00mL某未知浓度的盐酸溶于一洁净的锥形瓶中,然后用0.20mol•L-1的氢氧化钠溶液(指示剂为酚酞)作为标准液来滴定.造成测定结果偏高的原因可能是( )
| A. | 用固体氢氧化钠配制标准溶液时其中混有Na2O杂质 | |
| B. | 滴定终点读数时,俯视滴定管的刻度,其它操作均正确 | |
| C. | 盛装未知液的锥形瓶用蒸馏水洗过,未用待测液润洗 | |
| D. | 滴定到终点读数时发现碱式滴定管尖嘴处悬挂一滴溶液 |
2.下列粒子半径大小的比较正确的是( )
| A. | Na+<Mg2+<Al3+<O2- | B. | S2->Cl->Na+>Al3+ | ||
| C. | Na<Mg<Al<S | D. | Cs<Rb<K<Na |
3.利用碳酸钠晶体(Na2CO3•10H2O)来配制0.5mol/L的Na2CO3溶液1000mL,假如其他操作均准确无误,下列情况会引起配制溶液的浓度偏高的是( )
| A. | 称取碳酸钠晶体66g | |
| B. | 定容时,俯视观察刻度线 | |
| C. | 移液时,对用于溶解碳酸钠晶体的烧杯没有进行冲洗 | |
| D. | 定容后,将容量瓶振荡均匀,静置时发现液面低于刻度线,于是又加入少量水至刻度线 |
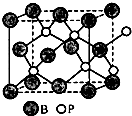 X、Y、Z、W、A五种元素,均位于周期表的前四周期,它们的核电荷数依次增加,且核电荷数之和为57.Y原子的L层p轨道中有2个电子,Z的原子核外有三个未成对电子,W与Y原子的价电子数相同,A原子的最外层电子数是最内层电子数的一半,其d轨道处于全充满状态.
X、Y、Z、W、A五种元素,均位于周期表的前四周期,它们的核电荷数依次增加,且核电荷数之和为57.Y原子的L层p轨道中有2个电子,Z的原子核外有三个未成对电子,W与Y原子的价电子数相同,A原子的最外层电子数是最内层电子数的一半,其d轨道处于全充满状态.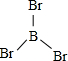 .
.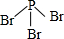 .
.
 .
. .
. .
.