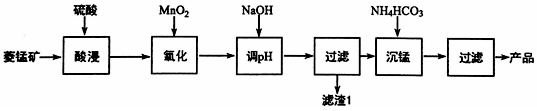
题目内容
6.《本草纲目》中记载“(火药)乃焰消(KNO3)、硫磺、杉木炭所合,以为烽燧铳机诸药者”.火药燃烧爆炸时发生的反应为:S(s)+2KNO3(s)+3C(s)═K2S(s)+N2(g)+3CO2(g)△H=x kJ•mol-1.已知:
①碳的燃烧热△H1=a kJ•mol-1
②S(s)+2K(s)═K2S(s)△H2=b kJ•mol-1
③2K(s)+N2(g)+3O2(g)═2KNO3(s)△H3=c kJ•mol-1
则x为( )
| A. | 3a+b-c | B. | c-3a-b | C. | a-b-c | D. | c-a-b |
分析 已知①C(s)+O2(g)=CO2 △H1=a kJ•mol-1
②S(s)+2K(s)═K2S(s)△H2=b kJ•mol-1
③2K(s)+N2(g)+3O2(g)═2KNO3(s)△H3=c kJ•mol-1
根据盖斯定律,①×3+②-③可得S(s)+2KNO3(s)+3C(s)═K2S(s)+N2(g)+3CO2(g),据此计算该反应的焓变△H.
解答 解:碳的燃烧热△H1=a kJ•mol-1,则碳燃烧的热化学方程式为:①C(s)+O2(g)=CO2 △H1=a kJ•mol-1,
②S(s)+2K(s)═K2S(s)△H2=b kJ•mol-1
③2K(s)+N2(g)+3O2(g)═2KNO3(s)△H3=c kJ•mol-1
根据盖斯定律,①×3+②-③可得S(s)+2KNO3(s)+3C(s)═K2S(s)+N2(g)+3CO2(g)△H=x=(a kJ•mol-1)×3+b kJ•mol-1-c kJ•mol-1=(3a+b-c)kJ•mol-1,
故选A.
点评 本题考查反应热与焓变的应用,题目难度不大,根据盖斯定律正确构造目标反应为解答关键,注意掌握盖斯定律的内容及应用方法,试题培养了学生的分析能力及灵活应用能力.

练习册系列答案
相关题目
17.日常生活中的许多现象或应用与化学反应有关,下列现象或应用与氧化还原反应有关的是( )
| A. | 铜铸塑像上出现铜绿[Cu2(OH)2CO3] | |
| B. | 灶具大理石板被食醋腐蚀变得不光滑 | |
| C. | 小苏打可用于治疗胃酸过多 | |
| D. | 用煤气灶燃烧天然气为炒菜提供热量 |
14.莽草酸可用于合成药物达菲,其结构简式如图,下列关于莽草酸的说法正确的是( )
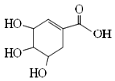

| A. | 分子式为C7H6O5 | B. | 分子中含有两种官能团 | ||
| C. | 1mol该有机物能与4molNaOH反应 | D. | 可发生加成和取代反应 |
1.将CO2通入下列物质的溶液中不与其反应的是( )
①Na2CO3 ②Ca(ClO)2 ③CaCO3④CaCl2.
①Na2CO3 ②Ca(ClO)2 ③CaCO3④CaCl2.
| A. | ①③④ | B. | ①和③ | C. | 只有② | D. | 只有④ |
11.生活离不开化学,下列说法正确的是( )
| A. | 氯化铵和草木灰混合使用,能增强化肥的肥效 | |
| B. | 二氧化硫和漂白粉混合使用,能增强漂白效果 | |
| C. | 浓盐酸和高锰酸钾混合使用,能增强高锰酸钾的氧化性 | |
| D. | 氢氧化钠固体和氧化钙混合使用,能增加吸水能力 |
18.下列各组元素的电负性大小顺序正确的是( )
| A. | S<N<O<F | B. | S<O<N<F | C. | Si<Na<Mg<Al | D. | Br<H<Zn |
15.下列反应的离子方程式正确的是( )
| A. | 把金属铁放入稀硫酸中:2Fe+6H+═2Fe3++3H2↑ | |
| B. | 将氢氧化铁放入盐酸中:Fe(OH)3+3H+═Fe3++3H2O | |
| C. | 氢氧化钡跟硫酸铜溶液反应:Ba2++SO42-═BaSO4↓ | |
| D. | 石灰石跟盐酸反应:CO32-+2H+═H2O+CO2↑ |
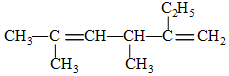 3,5-二甲基-2-乙基-1,4-己二烯.
3,5-二甲基-2-乙基-1,4-己二烯.