题目内容
17.日常生活中的许多现象或应用与化学反应有关,下列现象或应用与氧化还原反应有关的是( )| A. | 铜铸塑像上出现铜绿[Cu2(OH)2CO3] | |
| B. | 灶具大理石板被食醋腐蚀变得不光滑 | |
| C. | 小苏打可用于治疗胃酸过多 | |
| D. | 用煤气灶燃烧天然气为炒菜提供热量 |
分析 氧化还原反应的特征是元素的化合价的升降,如反应中无元素化合价的变化,则反应一定不是氧化还原反应,以此解答.
解答 解:A.Cu被腐蚀生成铜绿[Cu2(OH)2CO3],Cu元素化合价升高,被氧化,属于氧化还原反应,故A选;
B.大理石的主要成分为碳酸钙,与醋酸反应而被腐蚀,不是氧化还原反应,故B不选;
C.小苏打可用于治疗胃酸过多,是碳酸氢钠与盐酸反应,不属于氧化还原反应,故C不选;
D.天然气燃烧,是甲烷与氧气的反应,存在化合价的变化,是氧化还原反应,故D选.
故选AD.
点评 本题考查氧化还原反应,为高频考点,主要把握常见物质的性质以及反应类型的判断,从元素的化合价的角度判断反应是否属于氧化还原反应,难度不大.

练习册系列答案
相关题目
9.互为同系物的物质不具有( )
| A. | 相同的相对分子质量 | B. | 相同的通式 | ||
| C. | 相似的化学性质 | D. | 相似的结构 |
8.下列物质与常用危险化学品的类别不对应的是( )
| A. | 浓H2SO4、NaOH--腐蚀品 | B. | 酒精--易燃气体 | ||
| C. | KMnO4--氧化剂 | D. | 甲烷--易燃气体 |
5.在某钠盐溶液中,除Cl-之外可能还含有等物质的量的下列阴离子中的一种或多种:SO32-、CO32-、SiO32-、I-、NO3-、SO42-.在此溶液中加入过量盐酸,产生气泡,溶液颜色变深,但仍澄清,并且原溶液中的阴离子种类减少了3种.关于此溶液,下列说法正确的是( )
| A. | 原溶液中可能含有SiO32- | |
| B. | 生成的气体中一定有NO,可能含有CO2 | |
| C. | 溶液中减少的离子是SO32-、I-、NO3- | |
| D. | 原溶液中一定含有SO42- |
12.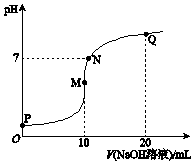 25℃时,向10mL 0.1mol•L-1 NH4HSO4溶液中逐滴滴入0.1mol•L-1 NaOH溶液,溶液的pH与NaOH溶液体积关系如图所示.下列选项正确的是( )
25℃时,向10mL 0.1mol•L-1 NH4HSO4溶液中逐滴滴入0.1mol•L-1 NaOH溶液,溶液的pH与NaOH溶液体积关系如图所示.下列选项正确的是( )
 25℃时,向10mL 0.1mol•L-1 NH4HSO4溶液中逐滴滴入0.1mol•L-1 NaOH溶液,溶液的pH与NaOH溶液体积关系如图所示.下列选项正确的是( )
25℃时,向10mL 0.1mol•L-1 NH4HSO4溶液中逐滴滴入0.1mol•L-1 NaOH溶液,溶液的pH与NaOH溶液体积关系如图所示.下列选项正确的是( )| A. | P点pH较低的主要原因是NH4+水解 | |
| B. | P、M、N、Q四点中,水的电离程度较大的是N点 | |
| C. | M点 c(Na+)>c(NH4+); N点 c(NH4+)+c(Na+)═2c(SO42-) | |
| D. | Q点 c(NH4+)+c(NH3•H2O)═c(Na+) |
2.其他条件不变,下列数据随温度升高的变化趋势一定正确的是( )
| A. | 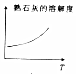 | B. |  | C. | 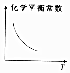 | D. | 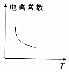 |
9.下列操作或仪器选用正确的是( )
| A. | 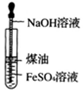 制取Fe(OH)2 | B. | 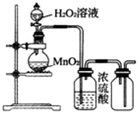 制取氧气 | ||
| C. |  滴定NaOH溶液 | D. | 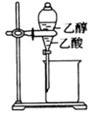 除去乙醇中的乙酸 |
6.《本草纲目》中记载“(火药)乃焰消(KNO3)、硫磺、杉木炭所合,以为烽燧铳机诸药者”.火药燃烧爆炸时发生的反应为:S(s)+2KNO3(s)+3C(s)═K2S(s)+N2(g)+3CO2(g)△H=x kJ•mol-1.
已知:
①碳的燃烧热△H1=a kJ•mol-1
②S(s)+2K(s)═K2S(s)△H2=b kJ•mol-1
③2K(s)+N2(g)+3O2(g)═2KNO3(s)△H3=c kJ•mol-1
则x为( )
已知:
①碳的燃烧热△H1=a kJ•mol-1
②S(s)+2K(s)═K2S(s)△H2=b kJ•mol-1
③2K(s)+N2(g)+3O2(g)═2KNO3(s)△H3=c kJ•mol-1
则x为( )
| A. | 3a+b-c | B. | c-3a-b | C. | a-b-c | D. | c-a-b |
7.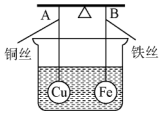 如图所示,杠杆AB两端分别挂有体积相同、质量相等的空心铜球和空心铁球,调节杠杆并使其在水中保持平衡,然后小心地向烧杯中央滴入浓CuSO4溶液,一段时间后,下列有关杠杆的偏向判断正确的是(实验过程中,不考虑铁丝反应及两球的浮力变化)( )
如图所示,杠杆AB两端分别挂有体积相同、质量相等的空心铜球和空心铁球,调节杠杆并使其在水中保持平衡,然后小心地向烧杯中央滴入浓CuSO4溶液,一段时间后,下列有关杠杆的偏向判断正确的是(实验过程中,不考虑铁丝反应及两球的浮力变化)( )
 如图所示,杠杆AB两端分别挂有体积相同、质量相等的空心铜球和空心铁球,调节杠杆并使其在水中保持平衡,然后小心地向烧杯中央滴入浓CuSO4溶液,一段时间后,下列有关杠杆的偏向判断正确的是(实验过程中,不考虑铁丝反应及两球的浮力变化)( )
如图所示,杠杆AB两端分别挂有体积相同、质量相等的空心铜球和空心铁球,调节杠杆并使其在水中保持平衡,然后小心地向烧杯中央滴入浓CuSO4溶液,一段时间后,下列有关杠杆的偏向判断正确的是(实验过程中,不考虑铁丝反应及两球的浮力变化)( )| A. | 杠杆为导体和绝缘体时,均为A端高B端低 | |
| B. | 杠杆为导体和绝缘体时,均为A端低B端高 | |
| C. | 当标杆为绝缘体时,A端低B端高;为导体时,A端高B端低 | |
| D. | 当标杆为绝缘体时,A端高B端低;为导体时,A端低B端高 |